Clear Sky Science · es
El contexto epigenético define la actividad transcripcional de las vías canónica y no canónica de NF-κB en el cáncer de páncreas
Por qué este estudio importa para los pacientes
El cáncer de páncreas es uno de los más letales, en parte porque sus células son expertas en detectar y responder a señales de peligro en su entorno. Este estudio examina dos de esas señales, llamadas TNFα y TWEAK, y muestra cómo activan distintos “modos de lectura” en el ADN de las células cancerosas. Comprender esos modos podría abrir nuevas vías para ralentizar el crecimiento tumoral, limitar la diseminación y hacer los tratamientos más eficaces.
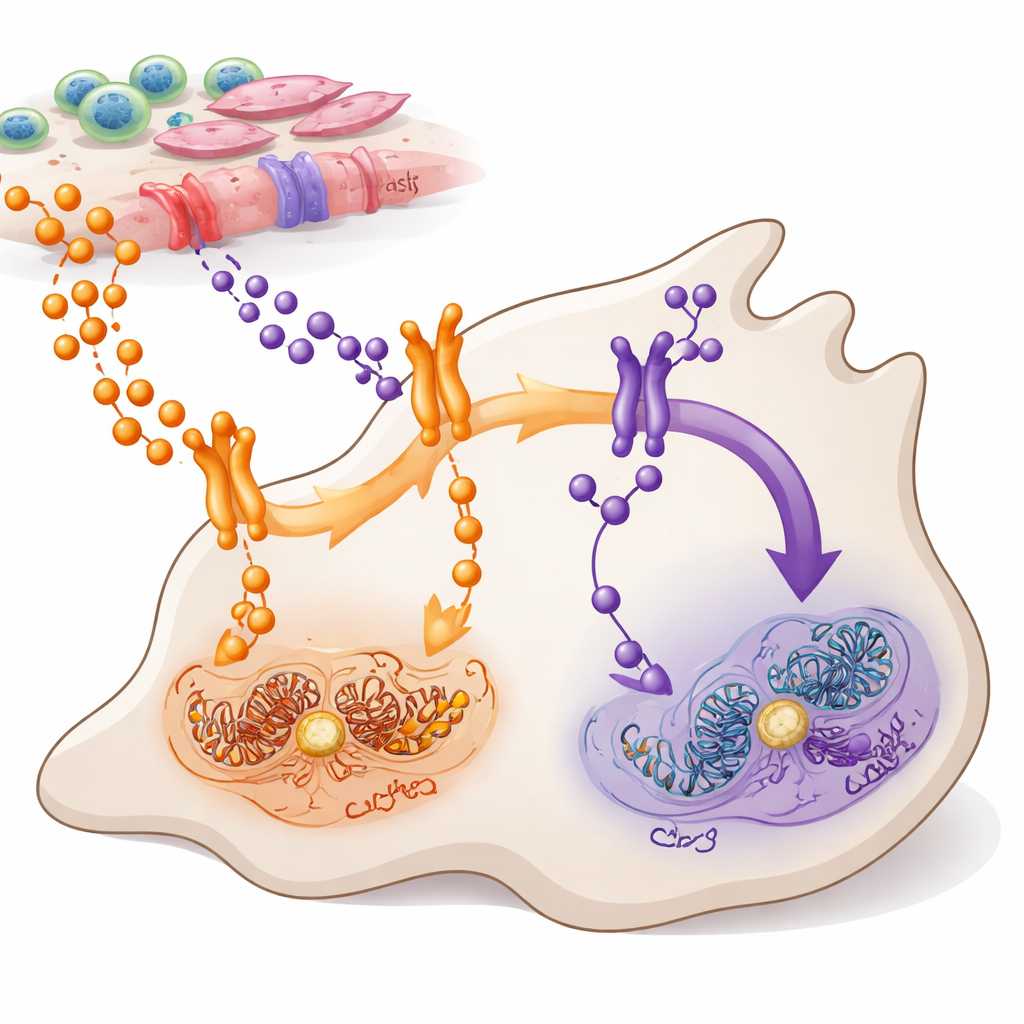
Dos rutas de mensaje hacia las células cancerosas
TNFα y TWEAK son pequeñas proteínas mensajeras liberadas por células dentro y alrededor de un tumor. Ambas se comunican con un importante sistema de control dentro de las células conocido como NF-κB, que ayuda a decidir si las células crecen, se mueven o mueren. Los autores se centraron en el adenocarcinoma ductal pancreático, la forma más común y agresiva de cáncer de páncreas, en la que NF-κB está anormalmente activo en la mayoría de los tumores. Cartografiaron qué células producen TNFα y TWEAK, qué células tienen sus receptores y cómo estas señales fluyen a través de dos ramas relacionadas de NF-κB—conocidas a menudo como la vía canónica (vía RELA) y la no canónica (vía RELB).
Quién envía las señales en el vecindario tumoral
Combinando secuenciación de ARN a nivel de célula única de miles de células de tumores de pacientes con microscopía avanzada, el equipo encontró que TNFα procede principalmente de células inmunitarias, especialmente macrófagos y ciertos linfocitos T y B. TWEAK, en cambio, lo producen un reparto más amplio: macrófagos, fibroblastos, células endoteliales y células estrelladas. Sus receptores también difieren. Las células tumorales y los fibroblastos cercanos expresan con fuerza el principal receptor de TNFα y el receptor clave de TWEAK. El análisis de redes sugirió que la señalización basada en TWEAK forma una red de comunicación más amplia y compleja entre células tumorales y de soporte, mientras que la señalización por TNFα está más focalizada en áreas ricas en células inmunitarias.
Diferentes profundidades de respuesta dentro de las células tumorales
En líneas celulares de cáncer de páncreas, los investigadores trataron las células con TNFα o TWEAK y midieron qué genes se activaban con el tiempo. TNFα desencadenó una ola rápida y amplia de actividad génica vinculada a inflamación, migración celular, remodelado tisular y supervivencia. TWEAK indujo un conjunto más pequeño y más lento de cambios que en gran parte se solapaban con los objetivos de TNFα en lugar de activar un programa único. Ambas señales podían promover la migración celular y, en ciertas condiciones, la muerte celular, pero TNFα tuvo un efecto más fuerte sobre el movimiento. Al examinar datos de tumores de pacientes del Cancer Genome Atlas, observaron que los tumores con niveles altos de TNFα o de TWEAK compartían muchos genes activados, confirmando estos patrones en cánceres humanos reales.
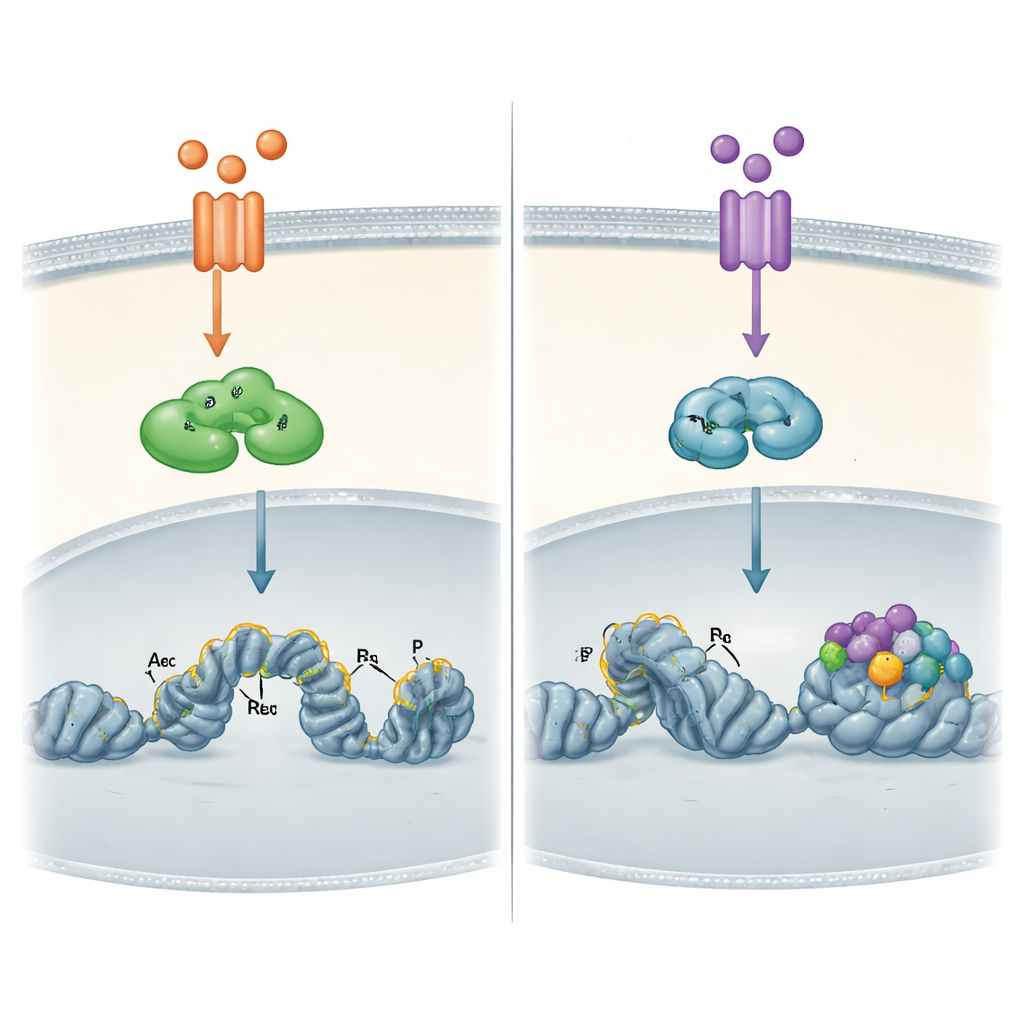
Cómo el paisaje del ADN moldea cada vía
Las diferencias más llamativas surgieron cuando los autores examinaron directamente la cromatina de las células cancerosas—la forma compacta del ADN y sus proteínas asociadas. Usando mapas de unión a escala genómica, mostraron que RELA activado por TNFα puede unirse no solo a regiones de ADN ya abiertas sino también a regiones más compactas y ayudarlas a “abrirse” añadiendo marcas químicas asociadas a interruptores activos. RELB, activado más tarde por TWEAK, se unió casi exclusivamente a sitios que ya eran accesibles y que estaban decorados con esas marcas activas. Esos sitios de RELB eran especialmente ricos en motivos de anclaje para otra familia de factores, AP-1, lo que sugiere que RELB depende de otras proteínas que preparan el terreno antes de poder actuar.
Qué significa esto para tratamientos futuros
Para un público no especialista, la conclusión clave es que TNFα y TWEAK usan la misma caja de herramientas NF-κB de formas muy distintas. TNFα, a través de RELA, actúa como un interruptor maestro capaz de forzar la apertura de secciones cerradas del ADN de la célula cancerosa y activar una amplia gama de genes implicados en crecimiento, supervivencia y diseminación. TWEAK, a través de RELB, se comporta más como un especialista que solo puede operar donde el ADN ya está abierto y donde hay cofactores como AP-1. Esta división del trabajo sugiere que fármacos que apunten a la remodelación de la cromatina, a AP-1 o a ramas específicas de NF-κB podrían disminuir selectivamente programas génicos perjudiciales en el cáncer de páncreas, al tiempo que preservan otras funciones.
Cita: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Palabras clave: cáncer de páncreas, señalización NF-kappaB, microambiente tumoral, regulación epigenética, TNF y TWEAK