Clear Sky Science · es
Aprovechar la piroptosis en la terapia del cáncer de mama: mecanismos inmunológicos y estrategias emergentes con biomateriales
Convertir la muerte celular en una nueva arma contra el cáncer de mama
El cáncer de mama sigue siendo uno de los tumores más frecuentes y tenaces en todo el mundo. Muchos tumores acaban evadiendo la cirugía, la quimioterapia e incluso las inmunoterapias modernas. Esta revisión explora una idea emergente: inducir deliberadamente una forma inflamatoria de muerte celular, la piroptosis, dentro de los tumores mamarios. Al hacer que las células cancerosas estallen de manera controlada e inflamatoria, los científicos esperan tanto matar el tumor directamente como despertar al sistema inmune para que se una al ataque.
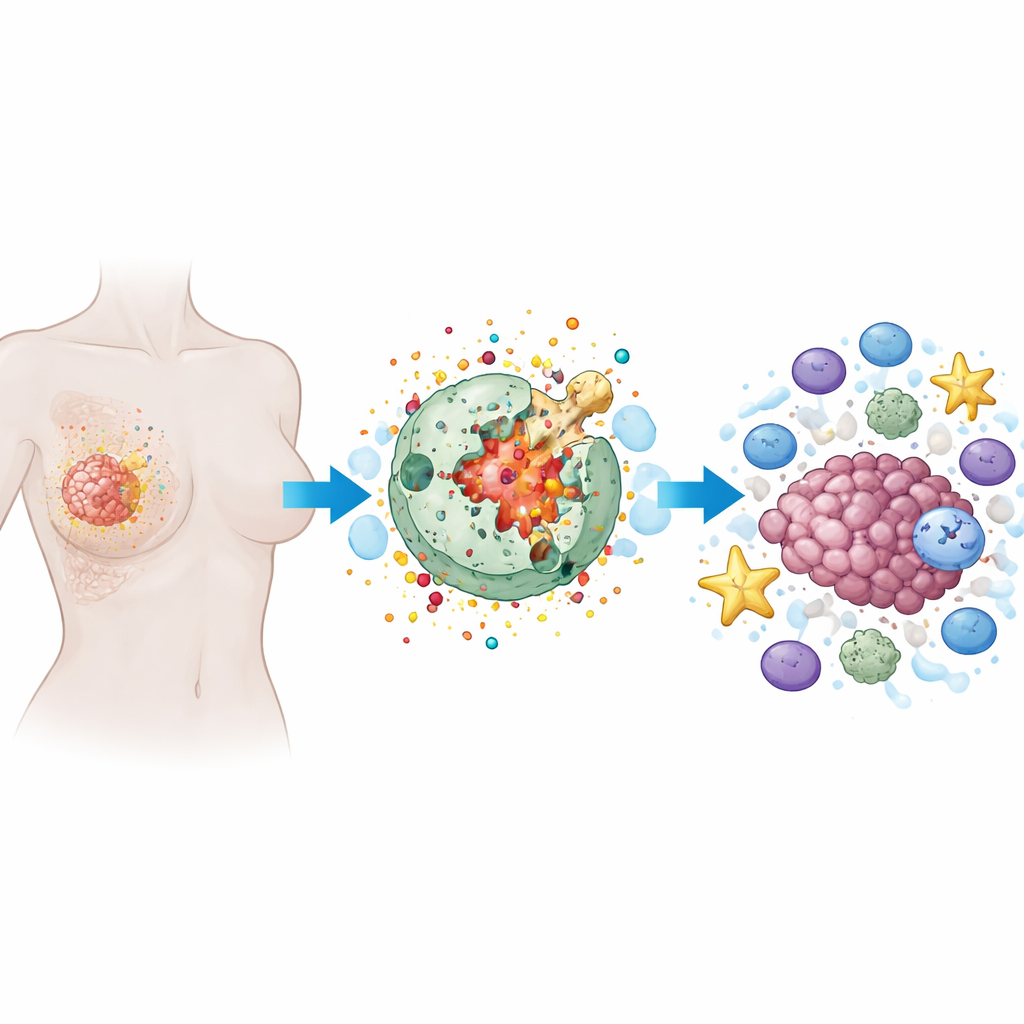
Cómo funciona una forma inflamatoria de muerte celular
La piroptosis es una forma programada de muerte celular en la que la célula se hincha, su membrana externa se llena de poros y finalmente se rompe, derramando su contenido. A diferencia de la muerte celular silenciosa y ordenada que observan muchas terapias, la piroptosis es ruidosa e inflamatoria. Proteínas especializadas, especialmente una familia llamada gasderminas, actúan como pequeñas cargas de demolición. Una vez cortadas por enzimas internas, las gasderminas perforan la membrana celular. Esto no solo destruye la célula cancerosa, sino que también libera señales de alarma y moléculas inflamatorias que pueden reclutar y activar células inmunitarias.
Por qué los tumores mamarios son un desafío especial
El cáncer de mama no es una sola enfermedad sino un conjunto de subtipos con comportamientos distintos. Algunos, como el cáncer de mama triple negativo, carecen de dianas terapéuticas comunes y con frecuencia resisten el tratamiento. Muchos tumores mamarios se consideran “fríos inmunológicamente”, es decir, contienen pocas células inmunes activas en su interior. La revisión explica cómo rasgos del microambiente tumoral mamario —incluidas las células estromales, las células inmunosupresoras y la falta local de oxígeno— pueden tanto preparar el terreno para la piroptosis como, si se controlan mal, convertir su inflamación en combustible para el crecimiento y la diseminación tumoral. Esta naturaleza de doble filo hace que la precisión sea especialmente importante.
Los interruptores de gasdermina dentro de las células tumorales
Un tema central del artículo es cómo distintas proteínas gasdermina actúan como interruptores moleculares dentro de las células del cáncer de mama. Versiones como GSDMD y GSDME pueden convertir señales procedentes de la quimioterapia, la radiación o células inmunitarias atacantes en una piroptosis completa. Otras, como GSDMC y algunas formas de GSDMB, suelen estar elevadas en tumores agresivos y pueden tanto promover como restringir la enfermedad según cómo se activen. Muchos cánceres de mama silencian químicamente GSDME, atenuando la piroptosis y la activación inmunitaria. Restaurar o desencadenar selectivamente las gasderminas adecuadas podría determinar si una terapia simplemente mata a unas pocas células o convierte todo el tumor en una vacuna in situ que alerta al sistema inmune.
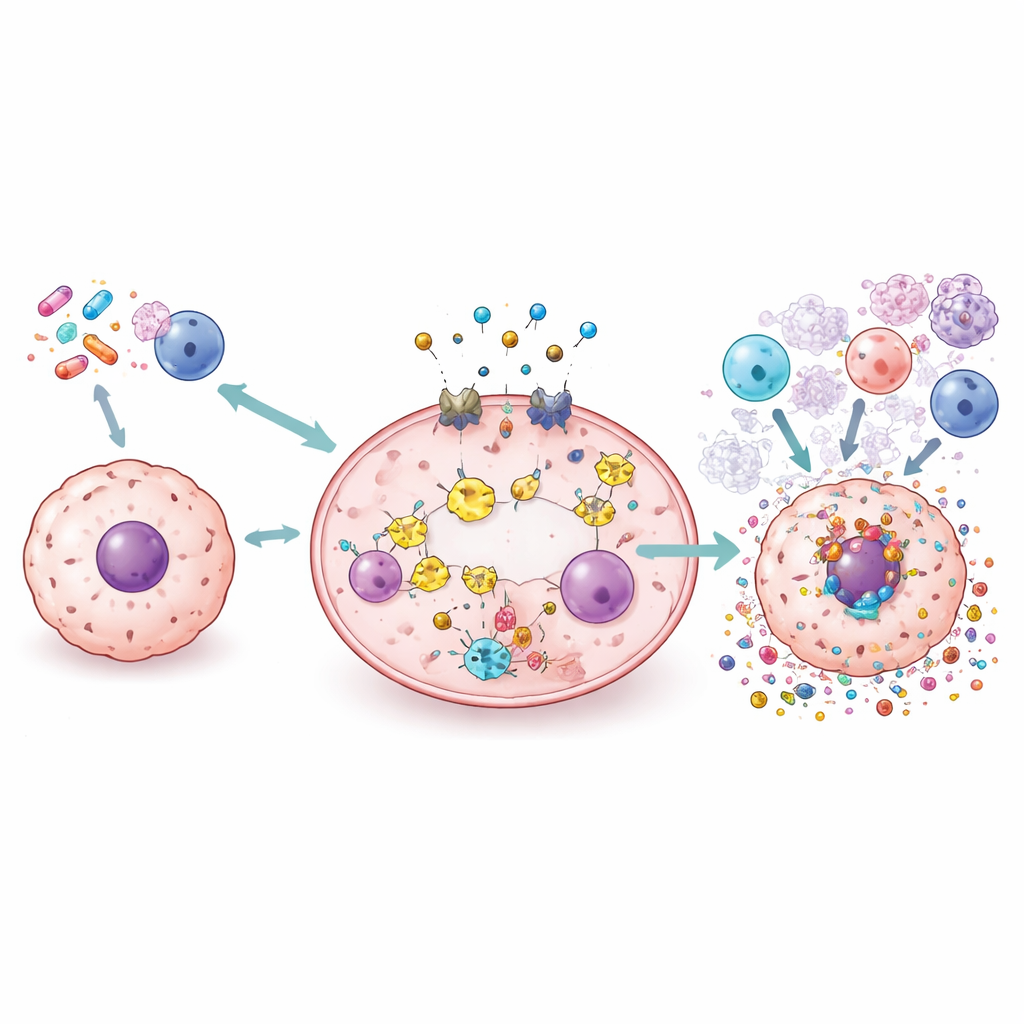
Nuevas herramientas: fármacos, nanopartículas, virus y radiación
La revisión repasa una amplia gama de estrategias en estudio para aprovechar la piroptosis de forma segura. Fármacos estándar como el cisplatino y la doxorrubicina pueden reconvertirse o reformularse para empujar a las células cancerosas hacia la explosión mediada por gasderminas en lugar de una muerte silenciosa. Pequeñas moléculas pueden bien amplificar o bloquear partes de la vía para matizar la inflamación. Se diseñan nanopartículas y transportadores biomiméticos para entregar quimioterapia, iones de cobre o moléculas activadas por luz directamente en los tumores, donde desencadenan piroptosis preservando los tejidos sanos. También se pueden diseñar virus oncolíticos y la radioterapia, o combinarse con otros agentes, para provocar piroptosis y remodelar el paisaje inmune tumoral, lo que potencialmente hace que los fármacos inhibidores de puntos de control inmunitario sean más eficaces.
Equilibrar beneficios potentes con riesgos reales
Dado que la piroptosis es muy inflamatoria, las mismas reacciones que ayudan al sistema inmune a combatir el cáncer también pueden dañar tejidos normales o incluso promover el crecimiento tumoral si se vuelven crónicas. Los autores destacan biomarcadores tempranos —como firmas génicas, patrones de metilación, fragmentos de proteínas gasdermina en sangre y perfiles de citocinas— que pueden ayudar a identificar qué pacientes son más propensos a beneficiarse y quién corre mayor riesgo de peligrosas “tormentas de citocinas”. Se están explorando diseños avanzados de nanomedicina, combinaciones de fármacos cuidadosamente elegidas y monitorización en tiempo real de marcadores inflamatorios para mantener la respuesta efectiva pero controlada.
Lo que esto podría significar para futuros pacientes
En términos sencillos, esta revisión sostiene que hacer que las células cancerosas “mueran en voz alta” podría transformar la atención del cáncer de mama. Al desencadenar piroptosis en un subconjunto preciso de células tumorales, los médicos podrían tanto reducir el volumen tumoral como despertar una respuesta inmune potente y duradera, convirtiendo tumores fríos en calientes y más sensibles a las inmunoterapias modernas. Sin embargo, la piroptosis es un aliado volátil: si se libera de forma demasiado amplia o prolongada, puede empeorar la inflamación u favorecer células resistentes. La investigación futura se centrará en cartografiar quién se beneficiará, perfeccionar sistemas de administración dirigidos y realizar ensayos clínicos que combinen enfoques inductores de piroptosis con agentes inmunitarios. Si se resuelven estos retos, aprovechar la piroptosis podría añadir una dimensión nueva y potente al tratamiento del cáncer de mama.
Cita: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Palabras clave: piroptosis, cáncer de mama, gasdermina, microambiente tumoral, nanomedicina