Clear Sky Science · es
Dinámica absoluta y estática relativa: la relación entre la glucólisis y la fosforilación oxidativa en el desarrollo del cáncer
Por qué importan las decisiones energéticas del cáncer
Las células cancerosas se parecen a atletas de resistencia extremos: deben abastecerse constantemente para crecer, diseminarse y evadir tratamientos. Esta revisión explica cómo las células tumorales recurren a dos sistemas energéticos principales—uno rápido y otro eficiente—y, más importante, cómo los combinan y alternan entre ellos. Comprender estas estrategias energéticas cambiantes ofrece una nueva forma de abordar el diagnóstico y el tratamiento del cáncer a lo largo de todo el curso de la enfermedad.
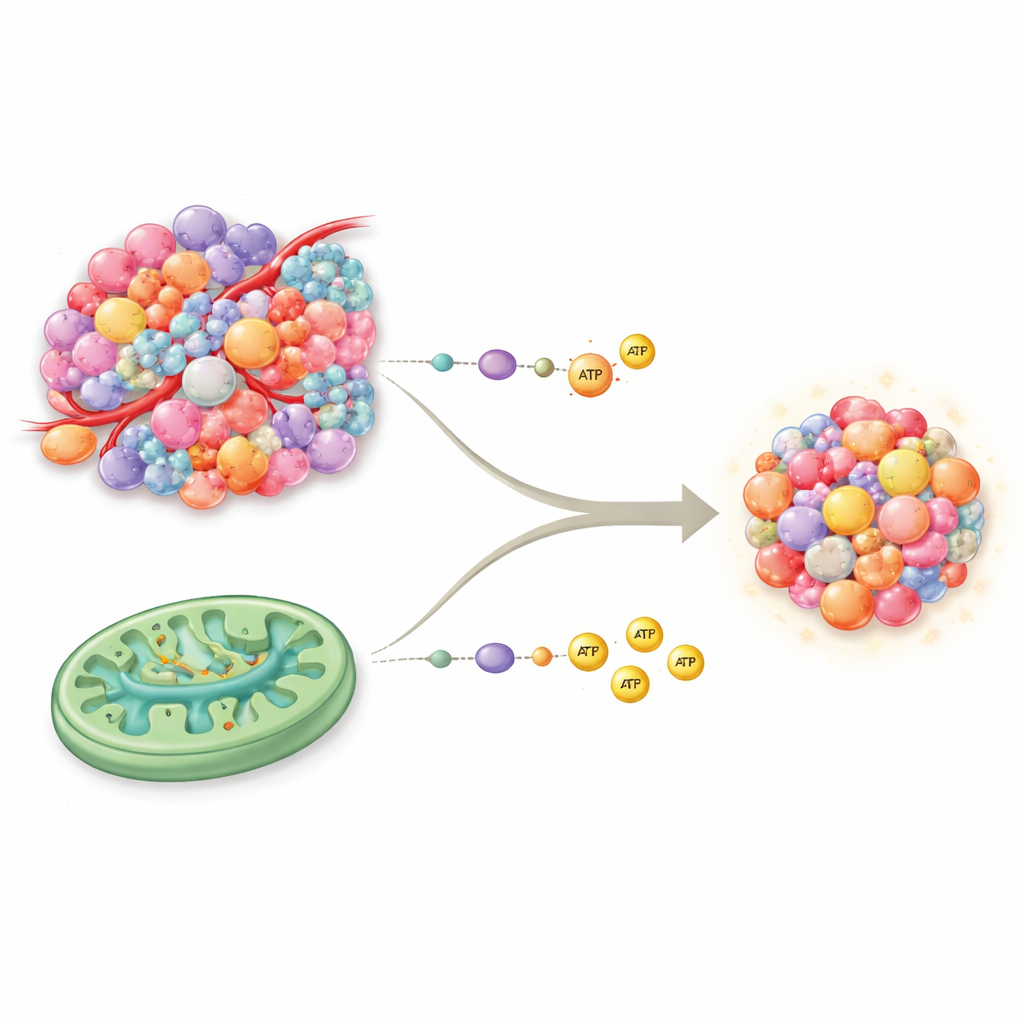
Dos vías principales para producir energía
Nuestras células suelen generar energía mediante dos rutas centrales. La glucólisis es el sistema rápido, como efectivo en mano, que descompone el azúcar con rapidez pero produce relativamente poca energía por unidad. La fosforilación oxidativa, u OXPHOS, ocurre en las mitocondrias y funciona más como una central de alta eficiencia, produciendo mucha más energía pero requiriendo buen suministro de oxígeno y nutrientes. Durante décadas se pensó que el cáncer dependía casi exclusivamente de la glucólisis incluso en presencia de oxígeno—un patrón conocido como efecto Warburg. Nuevas evidencias cuestionan esta visión simple: muchos tumores tienen mitocondrias plenamente funcionales y pueden usar OXPHOS y el ciclo del ácido tricarboxílico (TCA) junto con la glucólisis, lo que les proporciona un conjunto energético más rico y flexible de lo que se apreciaba antes.
Muchos tipos celulares, muchas elecciones de combustible
Un tumor no es una masa uniforme. Es un pequeño ecosistema que contiene células cancerosas, células de soporte, vasos sanguíneos y células inmunitarias, cada una con necesidades energéticas distintas. Algunas células cancerosas viven cerca de los vasos sanguíneos y disfrutan de abundante oxígeno y nutrientes; otras están enterradas en regiones con pobre suministro. Como resultado, células dentro del mismo tumor pueden favorecer la glucólisis, depender principalmente de OXPHOS o usar ambas vías a la vez. Esta variedad metabólica—llamada heterogeneidad—surge de diferencias en el flujo sanguíneo, niveles de nutrientes, tipo celular y señales del entorno circundante. Además, los tumores frecuentemente muestran simbiosis metabólica: las células glucolíticas exportan lactato como un subproducto similar a un desecho, que las células vecinas dependientes de OXPHOS importan y oxidarán como combustible valioso. Un intercambio de lactato similar ocurre entre células cancerosas y células de soporte como fibroblastos, células vasculares y células inmunosupresoras, lo que en conjunto ayuda al tumor a prosperar y resistir la terapia.
En constante cambio: cómo la energía tumoral se desplaza con el tiempo
El metabolismo tumoral no solo es diverso en un momento dado; también es altamente dinámico. A medida que los tumores crecen, se enfrentan a condiciones cambiantes como hipoxia, acumulación de ácido, falta de nutrientes y variaciones en la rigidez tisular. Bajo condiciones duras y con poco oxígeno, muchas células cancerosas se desplazan hacia la glucólisis. Frente a acumulación de ácido o escasez de azúcar, pueden volver a un mayor uso de OXPHOS. La misma flexibilidad aparece durante hitos biológicos clave. Las células que se dividen rápidamente se apoyan en la glucólisis para generar los bloques de construcción necesarios para nuevo ADN, lípidos y membranas. Las células en reposo o las que circulan en la sangre dependen con más frecuencia de OXPHOS. Durante la invasión y la metástasis, las células cancerosas ajustan repetidamente su elección de combustible: algunos pasos favorecen la glucólisis, otros favorecen OXPHOS, y las células metastásicas que colonizan nuevos órganos ajustan su metabolismo para concordar con el “suelo” del tejido de destino.
Genes, enzimas y “centrales” detrás del cambio
En la maquinaria celular, genes y enzimas dirigen estas decisiones energéticas. Oncogenes y supresores tumorales pueden empujar a las células hacia la glucólisis o hacia OXPHOS, o permitirles aumentar ambas vías. Mutaciones o alteraciones en enzimas clave del TCA, como las que manejan citrato, succinato o isocitrato, pueden inclinar el equilibrio, a veces promoviendo señales que favorecen el cáncer como el crecimiento vascular y la invasión. Enzimas situadas en encrucijadas críticas—como la piruvato quinasa M2, que ayuda a decidir si el carbono derivado del azúcar se destina a energía o a material de construcción—vinculan la glucólisis con la función mitocondrial. Al mismo tiempo, diferencias en el número, la estructura y el rendimiento de las mitocondrias a lo largo de las regiones tumorales amplían aún más el espectro de estados energéticos posibles.
Repensar el tratamiento mediante un objetivo energético en movimiento
Puesto que las células tumorales pueden alternar entre glucólisis y OXPHOS, simplemente bloquear una vía a menudo no es suficiente; el cáncer puede redirigir su uso de combustible y sobrevivir. Los autores sostienen que el metabolismo energético en el cáncer es solo brevemente estable y es, fundamentalmente, cambiante de forma continua. Proponen ver los tumores a través de un “espectro del metabolismo energético” que debe medirse a lo largo del tiempo, no solo una vez. En la práctica, esto podría significar seguir las preferencias de combustible de un tumor en diferentes etapas de la enfermedad y combinar inhibidores de la glucólisis y de OXPHOS de forma personalizada. Tales estrategias dinámicas guiadas por el metabolismo podrían cerrar mejor el suministro energético del tumor, limitar su capacidad de adaptación y mejorar el control a largo plazo de la enfermedad.
Cita: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Palabras clave: metabolismo del cáncer, glucólisis, fosforilación oxidativa, microambiente tumoral, plasticidad metabólica