Clear Sky Science · es
La transición endotelial a mesenquimal mediada por APOA2 y la reprogramación del metabolismo lipídico tumoral confieren resistencia a fármacos antiangiogénicos a través de TGF-β
Por qué este descubrimiento importa para los pacientes
Los médicos usan cada vez más fármacos que asfixian los tumores hepáticos cortándoles el suministro sanguíneo, pero muchos pacientes ven cómo sus cánceres dejan de responder tras un beneficio inicial. Este estudio aborda una pregunta urgente: ¿por qué algunos cánceres de hígado se hacen resistentes a estos tratamientos que bloquean los vasos sanguíneos y cómo podríamos superarlos? Los investigadores descubren una alianza oculta entre una proteína sanguínea que transporta grasas y una potente señal de crecimiento que permite a los tumores reorganizar tanto sus vasos sanguíneos como su uso de energía, señalando una vía alternativa para tratar un cáncer de difícil curación.
Un tumor que aprende a vivir sin su línea vital habitual
El carcinoma hepatocelular, la forma más común de cáncer de hígado, depende en gran medida de vasos sanguíneos nuevos para crecer. Los fármacos estándar para la enfermedad avanzada están diseñados para bloquear una vía clave de crecimiento vascular centrada en VEGF y su receptor VEGFR2. Sin embargo, en muchos pacientes, los tumores siguen prosperando pese a estos medicamentos. Al comparar muestras tumorales de pacientes que sí o no respondieron al fármaco antiangiogénico apatinib, los autores encontraron que un gen, APOA2, destacaba. Los tumores de pacientes resistentes presentaban niveles marcadamente más altos de APOA2, una proteína conocida sobre todo por su papel en el transporte de grasas en la sangre. Esto planteó la posibilidad de que APOA2 pudiera ayudar a los tumores a eludir los fármacos dirigidos a los vasos.
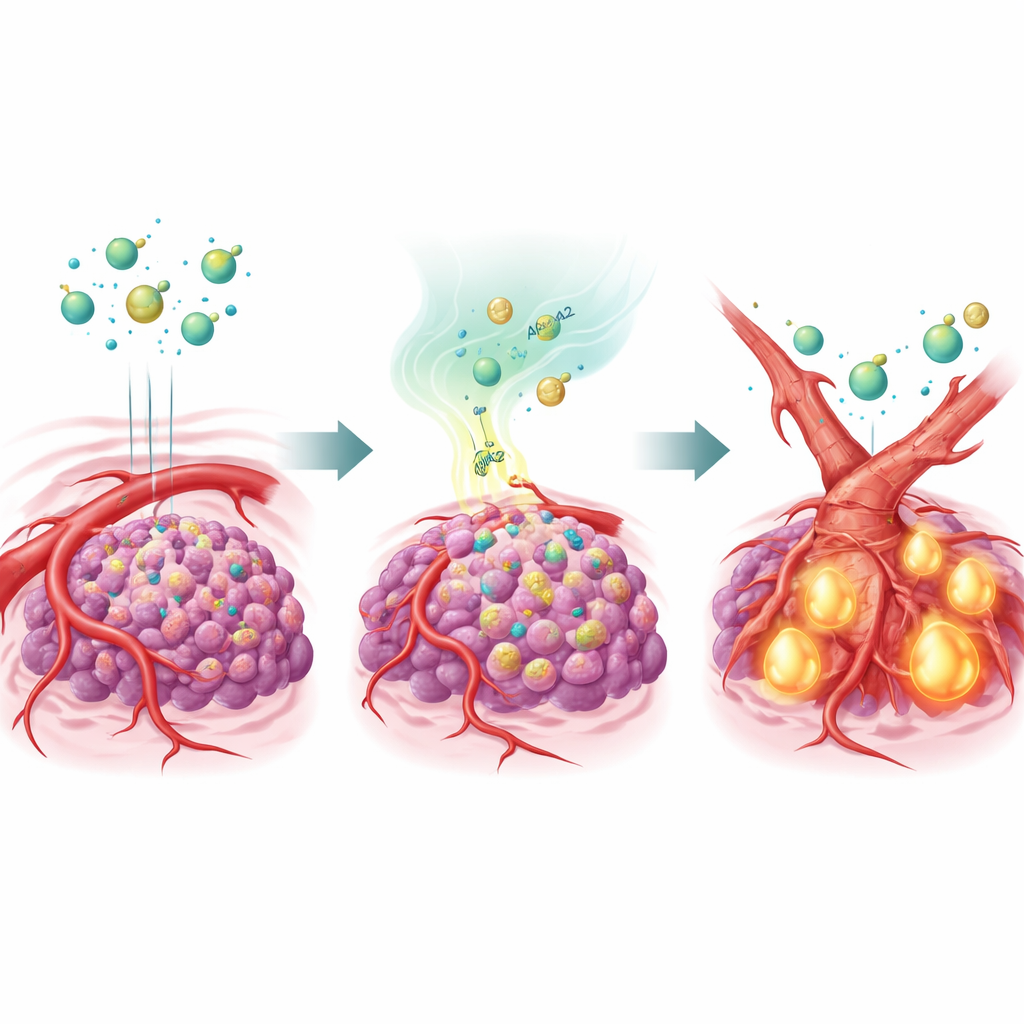
Una proteína transportadora de grasas que remodela los vasos
Para probar esta idea, el equipo modificó células de cáncer de hígado para que sobreprodujeran APOA2 e implantó esas células en ratones. Cuando se trataron con varios fármacos antiangiogénicos, estos tumores ricos en APOA2 ignoraron en gran medida la terapia: sus vasos persistieron y los cánceres siguieron creciendo. El análisis detallado mostró que una señal maestra llamada TGF-β estaba fuertemente activada en estos tumores, y sus niveles eran elevados tanto en el microambiente tumoral como en la sangre de los animales. TGF-β actuó sobre las células que recubren los vasos sanguíneos, impulsándolas a cambiar de identidad mediante un proceso denominado transición endotelial a mesenquimal. Al desplazarse hacia un estado más parecido a una cicatriz, mesenquimal, estas células perdieron gran parte de su VEGFR2, el mismo elemento que los fármacos antiangiogénicos pretenden bloquear. En efecto, los vasos se remodelaron en una forma que los fármacos ya no podían alcanzar.
Un desvío metabólico que mantiene alimentadas a las células cancerosas
La historia no terminó en la pared vascular. La misma señal TGF-β impulsada por APOA2 también reprogramó cómo se nutren las células tumorales. En lugar de confiar principalmente en la degradación de azúcares, las células con altos niveles de APOA2 empezaron a captar más ácidos grasos libres del entorno y a oxidarlos en sus mitocondrias mediante la beta-oxidación de ácidos grasos. Experimentos que midieron el uso de nutrientes y el consumo de oxígeno mostraron que estas células se volvieron más dependientes de las grasas como fuente de energía y produjeron más combustible celular (ATP). Este cambio permitió que las células tumorales continuaran dividiéndose rápidamente y evitaran la muerte celular, incluso cuando el suministro sanguíneo estaba comprometido por el tratamiento antiangiogénico.
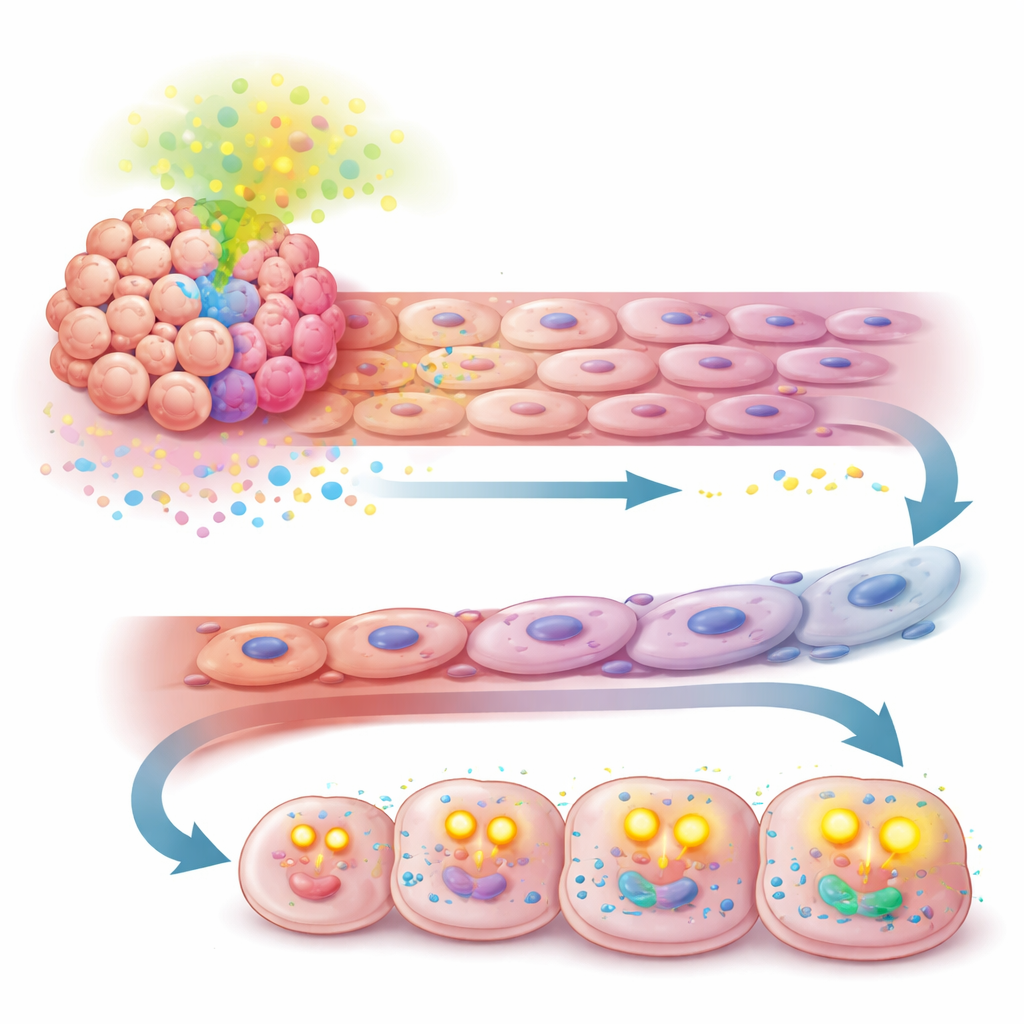
Convertir una debilidad en un nuevo objetivo terapéutico
De forma crucial, cuando los investigadores bloquearon TGF-β, las ventajas conferidas por APOA2 se desmoronaron. Inhibir esta señal en modelos murinos redujo los cambios anormales en los vasos, restauró la sensibilidad a la terapia y ralentizó el crecimiento tumoral. Aún más prometedor, un anticuerpo dual que bloquea simultáneamente TGF-β y el punto de control inmunitario PD-1 funcionó mejor que cualquiera de los enfoques por separado en tumores con altos niveles de APOA2. Estos resultados sugieren que, en un subconjunto de cánceres hepáticos marcados por APOA2 elevado, la enfermedad ha cambiado silenciosamente su dependencia de la vía VEGF habitual hacia una ruta centrada en TGF-β que sostiene tanto los vasos como el metabolismo tumoral.
Qué significa esto para la atención futura del cáncer de hígado
Para un lector no especializado, el mensaje clave es que algunos tumores hepáticos escapan a los fármacos actuales dirigidos a los vasos sanguíneos al reconfigurar tanto su “plomería” como su “suministro energético”. Una proteína asociada a las grasas, APOA2, aumenta la señal TGF-β, que a su vez camufla los vasos para que los fármacos existentes no los reconozcan y enseña a las células cancerosas a vivir de las grasas en lugar de la glucosa. El estudio sugiere que el análisis de APOA2 en los tumores podría identificar a pacientes poco propensos a beneficiarse de los antiangiogénicos estándar, pero que podrían responder a fármacos que bloqueen TGF-β, especialmente en combinación con inmunoterapia moderna. En resumen, al exponer cómo se adaptan los tumores, este trabajo apunta a una estrategia más personalizada que ataque tanto los vasos como la fuente de energía de la que dependen estos cánceres resistentes.
Cita: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Palabras clave: carcinoma hepatocelular, resistencia a antiangiogénicos, APOA2, señalización TGF-beta, metabolismo lipídico del cáncer