Clear Sky Science · es
Irisina inhibe la diferenciación adipogénica de las células madre mesenquimales de la médula ósea a través del eje de señalización SIRT1/RANBP2/FTO y protege contra la osteoporosis
Por qué una hormona muscular importa para los huesos frágiles
La osteoporosis suele presentarse como un problema simple de “huesos débiles”, pero en el interior del esqueleto se libra una silenciosa lucha. Las mismas células madre de la médula ósea pueden convertirse tanto en células formadoras de hueso como en adipocitos. Con la edad, especialmente tras la menopausia, este equilibrio se inclina hacia la formación de grasa, dejando los huesos más finos y frágiles. Este estudio explora cómo una hormona liberada por los músculos durante el ejercicio, llamada irisina, puede reorientar esas células madre hacia la formación de hueso en lugar de grasa, apuntando a un futuro en el que una hormona del entrenamiento podría ayudar a proteger contra la osteoporosis.
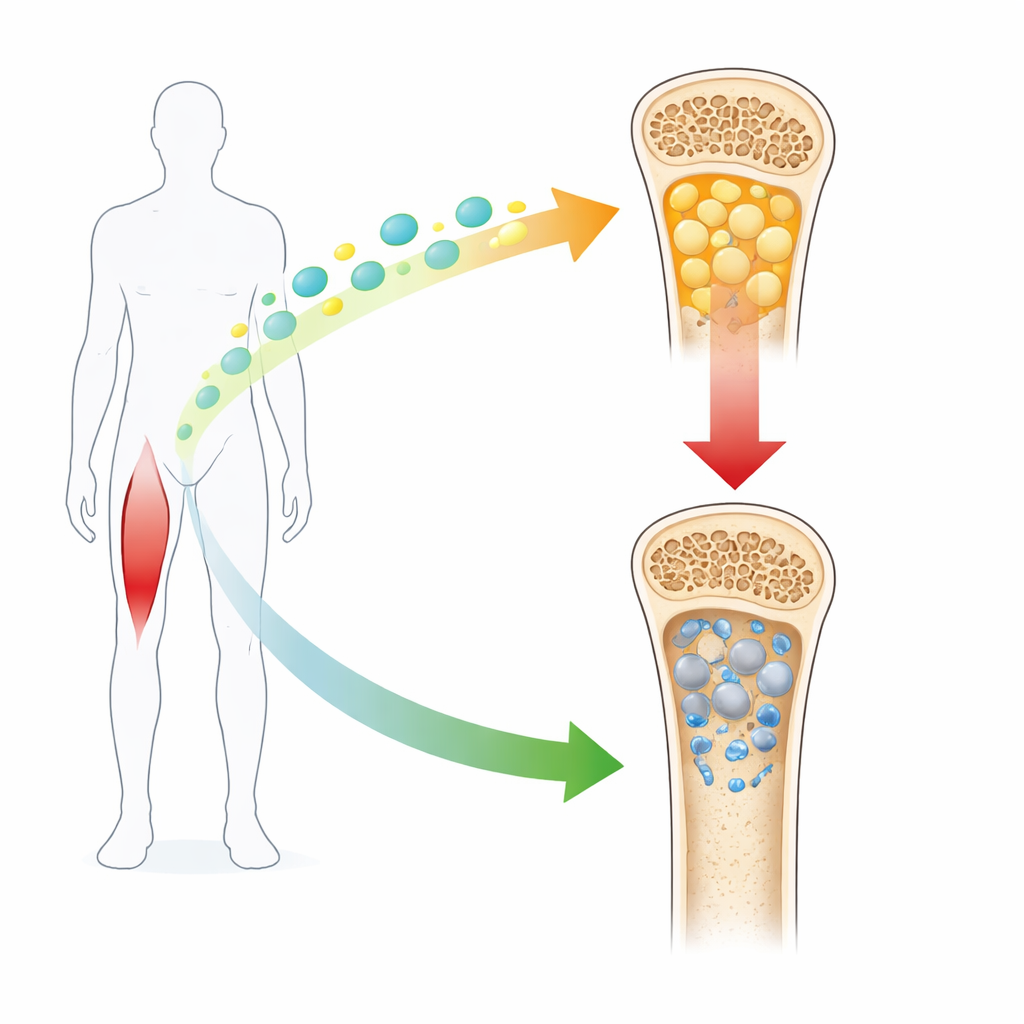
Cuando el hueso se convierte en grasa
La médula ósea no es sólo una cavidad vacía, sino un taller activo de células madre que pueden elegir distintos destinos. En adultos sanos, suficientes de estas células se diferencian en formadores de hueso para mantener el esqueleto fuerte. En la osteoporosis, sobre todo en mujeres posmenopáusicas, más de estas células se transforman en adipocitos. Esta “obesidad de la médula ósea” va de la mano con huesos frágiles y fracturas. Los investigadores comenzaron confirmando que este cambio hacia la grasa se acompaña de niveles más bajos de irisina, tanto en ratones con pérdida de estrógenos como en pacientes humanos con osteoporosis, vinculando la caída de esta hormona con un empeoramiento de la salud ósea.
Una señal ligada al ejercicio con un doble papel
La irisina se libera por los músculos durante la actividad física y se ha estudiado por sus efectos sobre el metabolismo y el gasto energético. Aquí, el equipo preguntó si la irisina también ayuda a decidir si las células madre de la médula ósea se convierten en grasa o en hueso. En cultivos celulares, añadieron irisina a células madre de médula ósea de ratón y observaron lo que ocurría. La irisina potenció la capacidad de las células para diferenciarse en osteoblastos, aumentando los depósitos minerales y la actividad de genes óseos clave. Al mismo tiempo, suprimió de forma marcada su transformación en adipocitos, reduciendo las gotas de grasa y disminuyendo la expresión de genes y proteínas que impulsan la adipogénesis. En ratones vivos a los que se les extirparon los ovarios para simular la pérdida ósea posmenopáusica, inyecciones semanales de irisina preservaron la masa y la microestructura óseas y redujeron la acumulación de grasa dentro de la cavidad medular.
Dentro de la maquinaria de decisión de la célula
Para entender cómo ejercía este control la irisina, los investigadores examinaron cambios en la actividad génica cuando las células madre se exponían a irisina durante la formación de grasa. Un protagonista destacado fue SIRT1, una proteína conocida por regular el envejecimiento, el metabolismo y las respuestas al estrés. El equipo mostró que disminuir SIRT1 hacía que las células tuvieran más probabilidad de convertirse en adipocitos, mientras que potenciar SIRT1 tenía el efecto contrario. De forma importante, cuando SIRT1 se redujo, la irisina ya no pudo bloquear eficazmente la formación de grasa, ni en células ni en ratones, revelando que SIRT1 es un relevo clave en la señal protectora ósea de la irisina.
Una cadena molecular que desactiva una proteína “pro‑grasa”
Al profundizar, el estudio se centró en otra proteína, FTO, que se ha relacionado con la obesidad y el almacenamiento de grasa. Niveles altos de FTO favorecen el desarrollo de adipocitos, en parte al estabilizar un regulador maestro de la grasa llamado PPARγ. Los investigadores hallaron que SIRT1 no alteraba la producción de FTO a nivel génico, sino que afectaba a la estabilidad de la proteína FTO. La SIRT1 activada por irisina aumentó la actividad de una tercera proteína, RANBP2, que marca a FTO de forma que lo dirige a su degradación. Cuando RANBP2 se redujo, SIRT1 ya no pudo disminuir los niveles de la proteína FTO y la formación de grasa reapareció. A través de esta cadena —irisina a SIRT1, SIRT1 a RANBP2, y RANBP2 a la degradación de FTO— las células se desviaron de convertirse en adipocitos y volvieron hacia roles formadores de hueso.
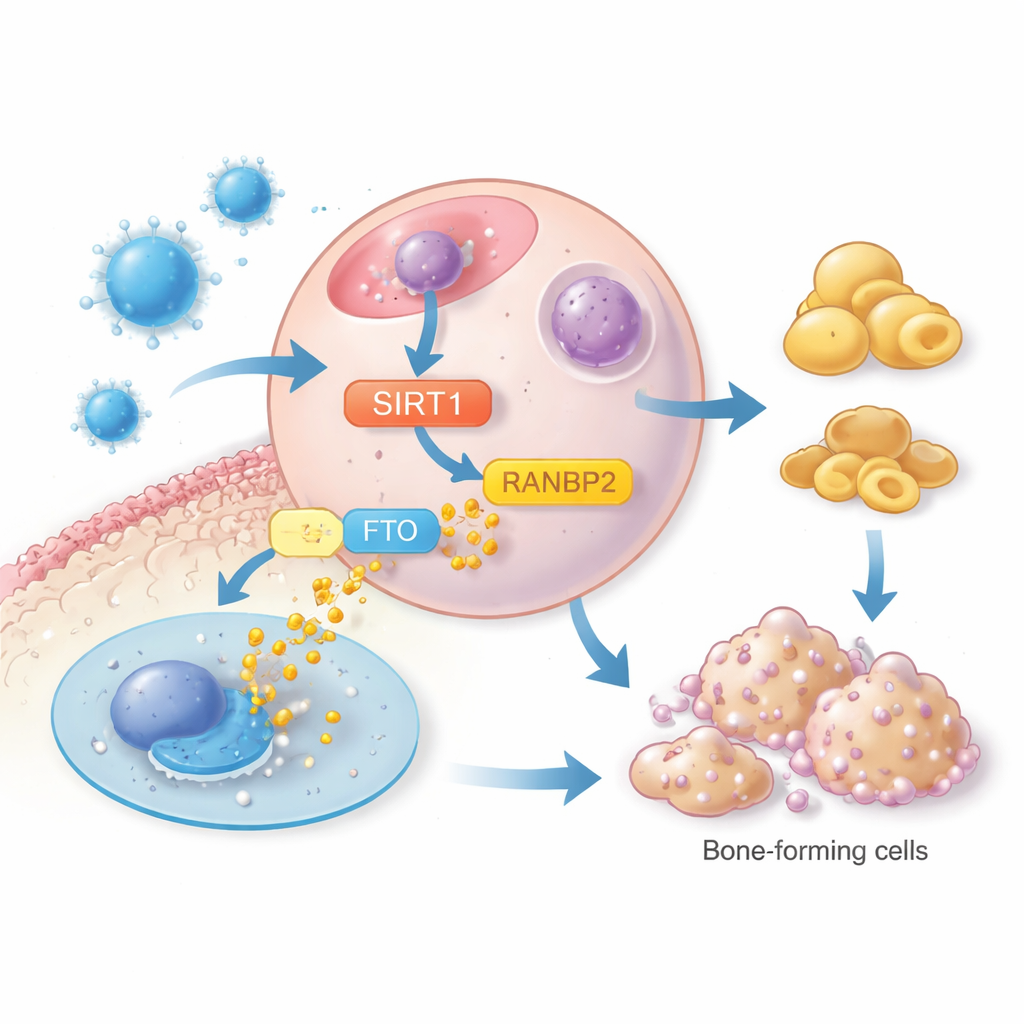
Qué podría significar esto para el cuidado óseo futuro
Al trazar esta vía paso a paso, el estudio revela a la irisina como algo más que una simple hormona del ejercicio. Actúa como un agente molecular en la médula ósea, orientando a las células madre a no convertirse en grasa y a favorecer la formación de hueso, a través de un eje de señalización SIRT1–RANBP2–FTO. Para el público general, esto significa que mantener o imitar la señal natural de irisina del organismo podría algún día ser una estrategia para prevenir o tratar la osteoporosis, complementando medidas de estilo de vida como el ejercicio. Aunque hacen falta más estudios en humanos a mayor escala, los hallazgos señalan un nuevo y prometedor conjunto de objetivos moleculares para mantener los huesos más fuertes por más tiempo.
Cita: Chen, J., Liu, J., Fu, Q. et al. Irisin inhibits adipogenic differentiation of bone marrow mesenchymal stem cells through the SIRT1/RANBP2/FTO signaling axis and protects against osteoporosis. Cell Death Discov. 12, 114 (2026). https://doi.org/10.1038/s41420-026-02976-5
Palabras clave: osteoporosis, irisinina, células madre de la médula ósea, equilibrio hueso-grasa, señalización SIRT1