Clear Sky Science · es
KCTD1 estabiliza c-Myc para aumentar PD-L1 y suprimir la inmunidad antitumoral en el carcinoma hepatocelular
Por qué importa esto para la atención del cáncer en el futuro
Muchas personas con cáncer de hígado no se benefician de las inmunoterapias más prometedoras de hoy, diseñadas para liberar a las propias células T del organismo contra los tumores. Este estudio explora por qué una forma importante de cáncer de hígado, el carcinoma hepatocelular, puede seguir escondiéndose del ataque inmunitario incluso durante el tratamiento, e identifica un nuevo interruptor molecular, llamado KCTD1, que podría hacer que los fármacos de inmunoterapia existentes funcionen mejor.
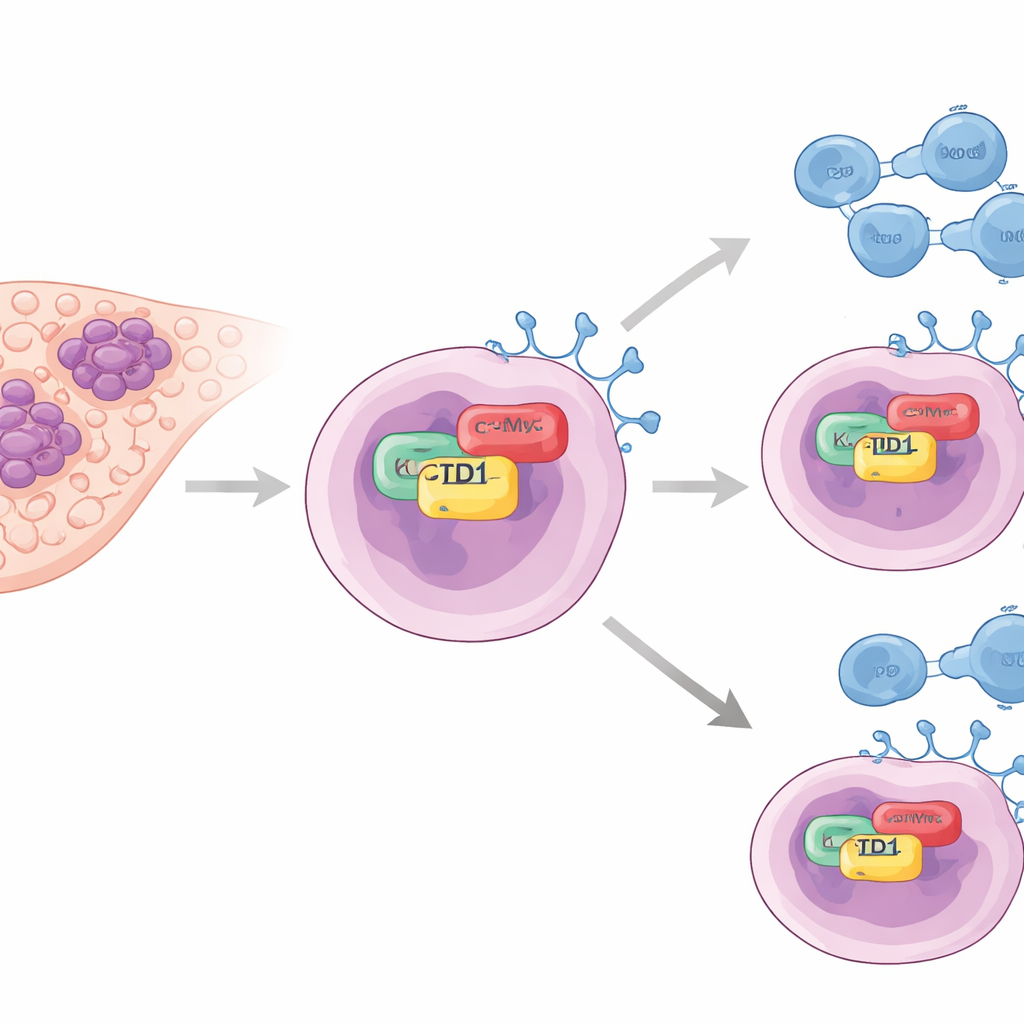
Un ayudante oculto de los “interruptores” tumorales
Los autores se centraron en una proteína llamada KCTD1, previamente relacionada con el crecimiento tumoral hepático pero poco estudiada en la evasión inmune. En muestras tumorales de pacientes, encontraron que los niveles de KCTD1 eran notablemente más altos en el tejido hepático canceroso que en el hígado normal. De forma importante, los tumores ricos en KCTD1 también presentaban altos niveles de PD-L1, una proteína de superficie en las células cancerosas que se une a PD-1 en las células T y, efectivamente, le indica al sistema inmune que se retire. Los pacientes cuyos tumores tenían menos KCTD1 tendieron a vivir más tiempo, lo que sugiere que esta proteína está conectada tanto con la gravedad de la enfermedad como con la fuerza del escudo inmunitario tumoral.
Conectando los puntos moleculares dentro de las células cancerosas
Para entender cómo KCTD1 incrementa PD-L1, el equipo recurrió a líneas celulares de cáncer de hígado cultivadas en el laboratorio. Cuando redujeron KCTD1, los niveles de proteína PD-L1 cayeron y la PD-L1 restante se degradó más rápidamente, lo que indica que KCTD1 ayuda a estabilizar PD-L1 en lugar de limitarse a activar su gen. Mediante experimentos bioquímicos de pull-down y microscopía fluorescente, mostraron que KCTD1 se une físicamente a otro impulsor clave del cáncer, la oncoproteína c-Myc, dentro del núcleo celular. Esta interacción ocurre a través de regiones de contacto específicas en ambas proteínas y conduce a una c-Myc más estable, lo que a su vez aumenta la producción de PD-L1. Cuando la c-Myc se redujo por sí sola, PD-L1 disminuyó incluso si KCTD1 era abundante, situando a c-Myc como el eslabón crucial en la cadena KCTD1–c-Myc–PD-L1.
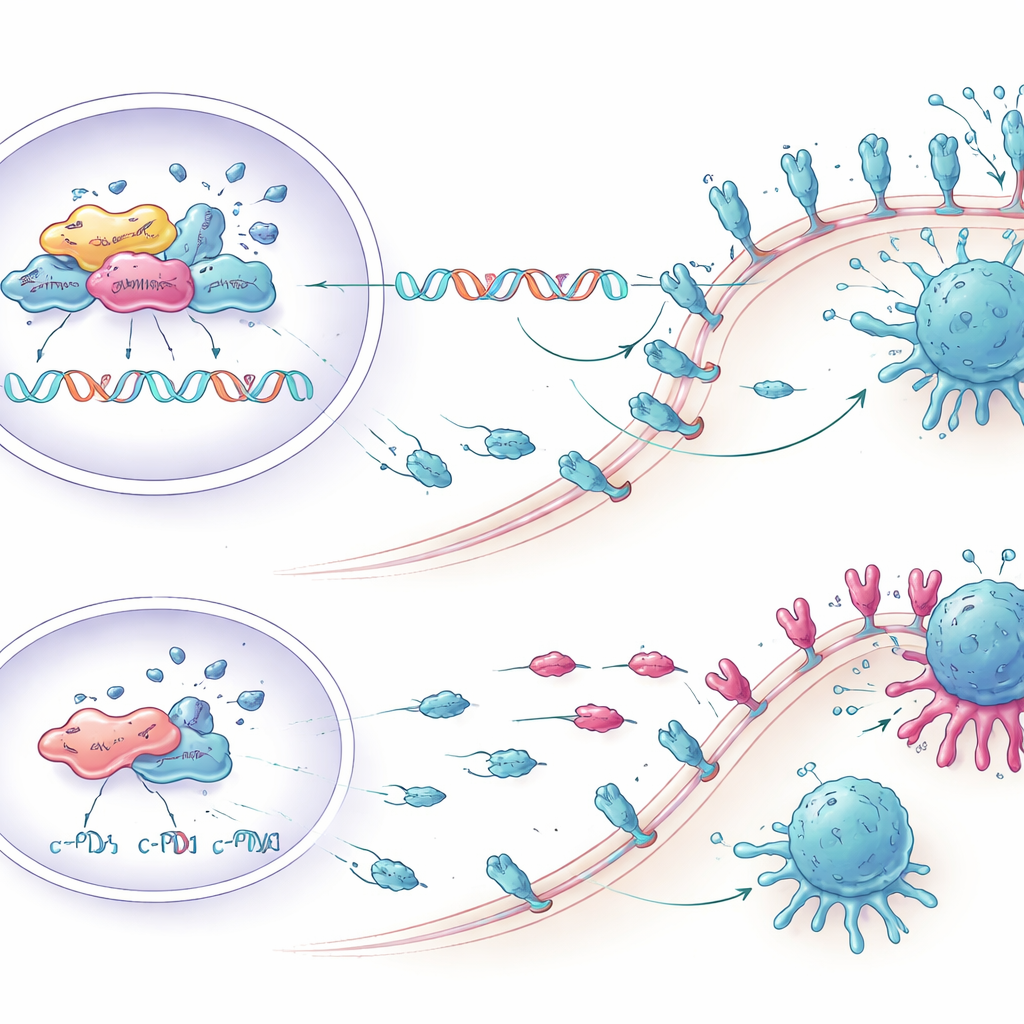
Reavivar las células T en el laboratorio
Los investigadores se preguntaron entonces si reducir KCTD1 podría realmente fortalecer el ataque inmunitario. Co-cultivaron células humanas de cáncer de hígado con células inmunitarias tomadas de donantes de sangre. Las células tumorales diseñadas para tener menos KCTD1, y por tanto menos PD-L1, desencadenaron respuestas más fuertes de las células T CD8 —los principales asesinos del sistema inmune contra las células cancerosas. Más de estas células T produjeron moléculas inflamatorias como TNF-α e interferón gamma, mostraron marcadores más altos de proliferación y activación, y presentaron menos signos de agotamiento. Como resultado, más células tumorales sufrieron muerte celular programada cuando se suprimió KCTD1, demostrando que los cambios moleculares se tradujeron en ganancias reales en la eliminación tumoral por parte del sistema inmune.
Poner a prueba el mecanismo en ratones
Para ver si el mismo patrón se mantenía en organismos vivos, el equipo implantó células de cáncer hepático de ratón carentes de KCTD1 directamente en los hígados de ratones. Los tumores con KCTD1 reducido formaron menos y más pequeños nódulos, mostraron una división celular más lenta y presentaron más células cancerosas en proceso de muerte. Estos tumores también expresaron menos c-Myc y PD-L1. La eliminación de las células T CD8 en los ratones borró gran parte de este beneficio, lo que indica que la desaceleración tumoral dependía en gran medida de la actividad de las células T. Finalmente, cuando los investigadores combinaron la reducción de KCTD1 con un anticuerpo anti–PD-1 —un fármaco de bloqueo de puntos de control inmune ya existente—, los ratones tuvieron la menor carga tumoral y los niveles más altos de infiltración tumoral de células T CD4 y CD8.
Qué podría significar esto para los pacientes
En conjunto, el trabajo revela a KCTD1 como un coordinador central que estabiliza c-Myc, aumenta PD-L1 en las células de cáncer de hígado y mitiga el ataque de las células T CD8. Interrumpir esta vía hace que los tumores sean tanto más vulnerables al sistema inmune como más sensibles a los fármacos que bloquean PD-1 en ratones. Para los pacientes, esto sugiere que en el futuro los fármacos dirigidos a KCTD1 o a su superficie de contacto con c-Myc podrían combinarse con las inmunoterapias actuales para ayudar a más personas con cáncer de hígado a beneficiarse de un control inmunitario duradero de su enfermedad.
Cita: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Palabras clave: carcinoma hepatocelular, inmunoterapia tumoral, vía PD-1 PD-L1, señalización c-Myc, inmunidad T antitumoral