Clear Sky Science · es
Multi-ómica revela heterogeneidad y poblaciones funcionales de células progenitoras de oligodendrocitos inducidas por células madre neurales humanas
Por qué importa proteger el aislamiento cerebral
El cableado de nuestro cerebro depende de un recubrimiento graso llamado mielina, que envuelve las fibras nerviosas como el aislamiento de los cables eléctricos. Cuando la mielina se daña, como ocurre en la esclerosis múltiple y otros trastornos, las señales se enlentecen o fallan, provocando problemas en el movimiento, la visión y el pensamiento. Este estudio explora un grupo especial de células humanas capaces de reconstruir la mielina y plantea una pregunta práctica: ¿qué células son más adecuadas para futuras terapias celulares destinadas a reparar este aislamiento crucial?
De células neuronales iniciales a formadoras de mielina
Los investigadores partieron de células madre neurales humanas—células iniciales versátiles obtenidas de tejido cerebral fetal que ya están comprometidas a convertirse en células del sistema nervioso. En el laboratorio, indujeron a estas células madre a transformarse en células progenitoras de oligodendrocitos, o hOPC, que son los precursores directos de las células formadoras de mielina. Bajo el microscopio, las células pasaron de formas redondeadas y simples a morfologías más complejas con múltiples ramas, y activaron proteínas características que señalan los pasos hacia células maduras formadoras de mielina. Esto proporcionó una fuente fiable y relativamente segura de precursores humanos para análisis detallados.
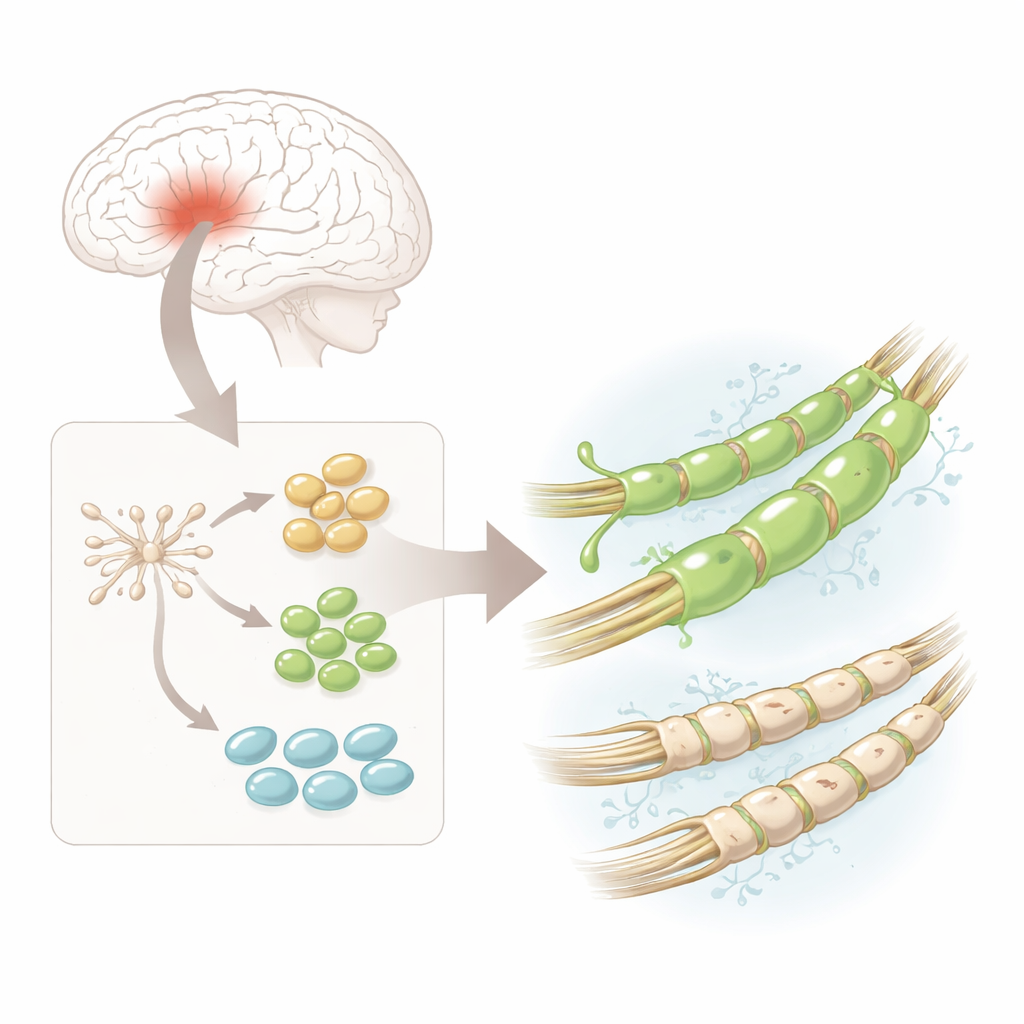
Un tipo celular, muchas variedades ocultas
Empleando la secuenciación de ARN unicelular—un enfoque que registra qué genes están activos en miles de células individuales—el equipo descubrió que las hOPC no eran todas iguales. En su lugar, se agruparon en tres etapas principales: «pre-progenitores» tempranos, progenitores más comprometidos y células que se aproximan a la identidad completa de oligodendrocitos. En todas estas etapas destacó un gen: PDGFRA, que codifica un receptor en la superficie celular. Un método de imagen altamente sensible llamado RNA-Scope confirmó que el transcrito y la proteína de PDGFRA eran más abundantes que otros marcadores clave en cada etapa, lo que sugiere que este receptor podría definir células particularmente capaces de formar mielina.
Separando las células de reparación más potentes
Para probar esta idea, los científicos separaron las hOPC en dos grupos según si presentaban el receptor PDGFR-α en su superficie. Compararon células positivas para PDGFR-α, células negativas y células no separadas en una serie de pruebas funcionales. Tras ser trasplantadas en ratones «shiverer», que no pueden formar mielina normal, las células PDGFR-α–positivas produjeron una mielina más densa y compacta alrededor de las fibras nerviosas que los otros grupos. Estas células también migraron más lejos y se multiplicaron más rápido en ensayos de laboratorio. En otras palabras, la población PDGFR-α–positiva fue la más vigorosa para desplazarse hasta donde se la necesitaba, expandirse en número y reconstruir el aislamiento.
Señales internas que impulsan el crecimiento y la reparación
Profundizando más, el equipo comparó la actividad génica entre células PDGFR-α–positivas y negativas. Encontraron que las positivas activaban redes de genes implicadas en el crecimiento de células gliales y la formación de mielina, así como varias vías de señalización clave dentro de la célula. Destacaron en particular dos rutas: PI3K–AKT–mTOR, asociada desde hace tiempo al crecimiento celular y la producción de mielina, y la señalización TGF-β, que influye en cómo las células jóvenes del cerebro eligen su destino. Los datos sugirieron que la activación de PDGFR-α se integra con PI3K–AKT–mTOR, que a su vez potencia las señales relacionadas con TGF-β, empujando conjuntamente a las células hacia convertirse en eficientes formadoras de mielina.
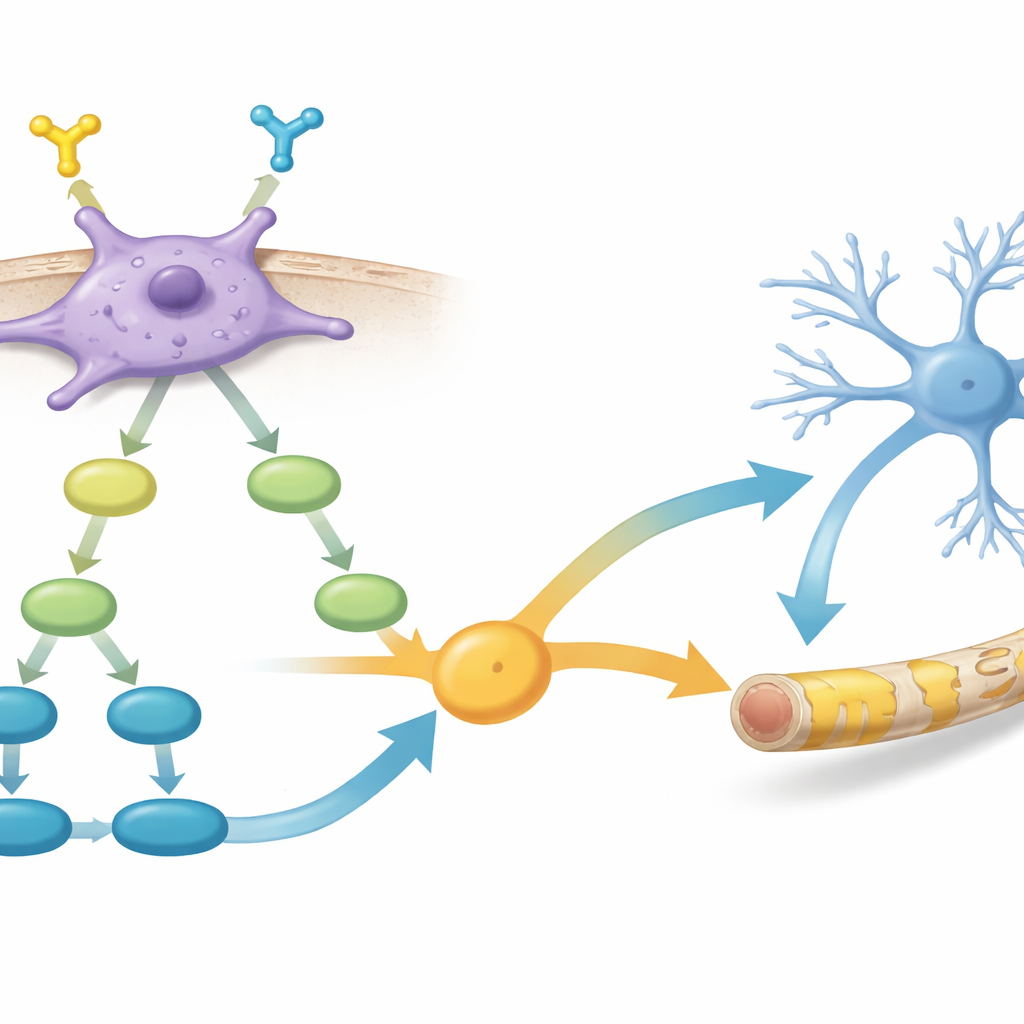
Potenciar la reparación de la mielina con un ayudante químico
Los investigadores preguntaron después si podían mejorar aún más estas células prometedoras. Trataron las hOPC PDGFR-α–positivas con una pequeña molécula que activa la vía TGF-β y examinaron tanto la actividad génica como el comportamiento celular. Tras el tratamiento, estas células mostraron niveles más altos de múltiples genes relacionados con la mielina y produjeron vainas de mielina más gruesas y completas cuando se trasplantaron en ratones shiverer, en comparación con las células PDGFR-α–positivas no tratadas. Esto respalda la idea de que afinar cuidadosamente la señalización interna en progenitores ya bien seleccionados puede mejorar todavía más su rendimiento como herramientas vivas de reparación de la mielina.
Qué significa esto para tratamientos futuros
Para públicos no especializados, el mensaje central es que no todos los precursores formadores de mielina son iguales. Combinando potentes herramientas de lectura génica e imagen, este estudio identifica un subgrupo destacado—las hOPC PDGFR-α–positivas—que migran mejor, se dividen más y reconstruyen la mielina de manera más efectiva que sus pares. También pone de relieve vías de señalización internas que pueden ser moduladas químicamente para potenciar aún más estas células. En conjunto, estas ideas trazan una hoja de ruta para diseñar terapias celulares más seguras y eficaces que restauren el aislamiento del cerebro en enfermedades donde se pierde la mielina.
Cita: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Palabras clave: reparación de la mielina, células progenitoras de oligodendrocitos, células madre neurales, terapia celular, secuenciación de ARN unicelular