Clear Sky Science · es
La bioenergética mitocondrial y el cruce con el SASP determinan la eficacia senolítica en la senescencia inducida por terapia
Por qué es tan difícil eliminar las células “zombi” del cáncer
Muchos fármacos modernos contra el cáncer no matan a todas las células tumorales de inmediato. En lugar de ello, algunas células entran en un estado parecido a un limbo llamado senescencia: dejan de dividirse pero permanecen vivas, algo así como células “zombi”. Estas células senescentes inducidas por la terapia pueden ser útiles al principio, pero si persisten pueden alimentar recaídas, resistencia y efectos secundarios. Por eso los científicos prueban fármacos senolíticos diseñados para eliminar selectivamente células senescentes. Este artículo plantea una pregunta aparentemente simple: ¿por qué algunas células senescentes del cáncer mueren cuando se exponen a senolíticos, mientras que otras sobreviven obstinadamente?
Centralitas que recuerdan su pasado
En el corazón del estudio están las mitocondrias, las pequeñas centralitas energéticas dentro de las células. Los autores examinaron si la forma en que las mitocondrias queman distintos combustibles—como azúcares, grasas y aminoácidos—afecta la sensibilidad de las células cancerosas senescentes a senolíticos que apuntan a una proteína de supervivencia llamada BCL‑xL. Usando un ensayo de alto rendimiento (MitoPlate S‑1), “huellan” funcionalmente la actividad mitocondrial en varias líneas de cáncer antes y después de que se indujera la senescencia con distintos tratamientos (fármacos dañinos para el ADN, bloqueadores mitóticos, estrés oxidativo o inhibidores del ciclo celular). Encontraron que la senescencia inducida por terapia no produjo un estado mitocondrial único y uniforme. En cambio, cada fármaco dejó una “impresión bioenergética” distinta, cambiando cuán amplia e intensa era la capacidad de las mitocondrias para explotar diversas fuentes de energía. Crucialmente, esta flexibilidad se superpuso a una línea base preexistente: la configuración mitocondrial original de las células parentales fijaba un límite superior—el “techo”—sobre la intensidad máxima de la respuesta senolítica posterior.
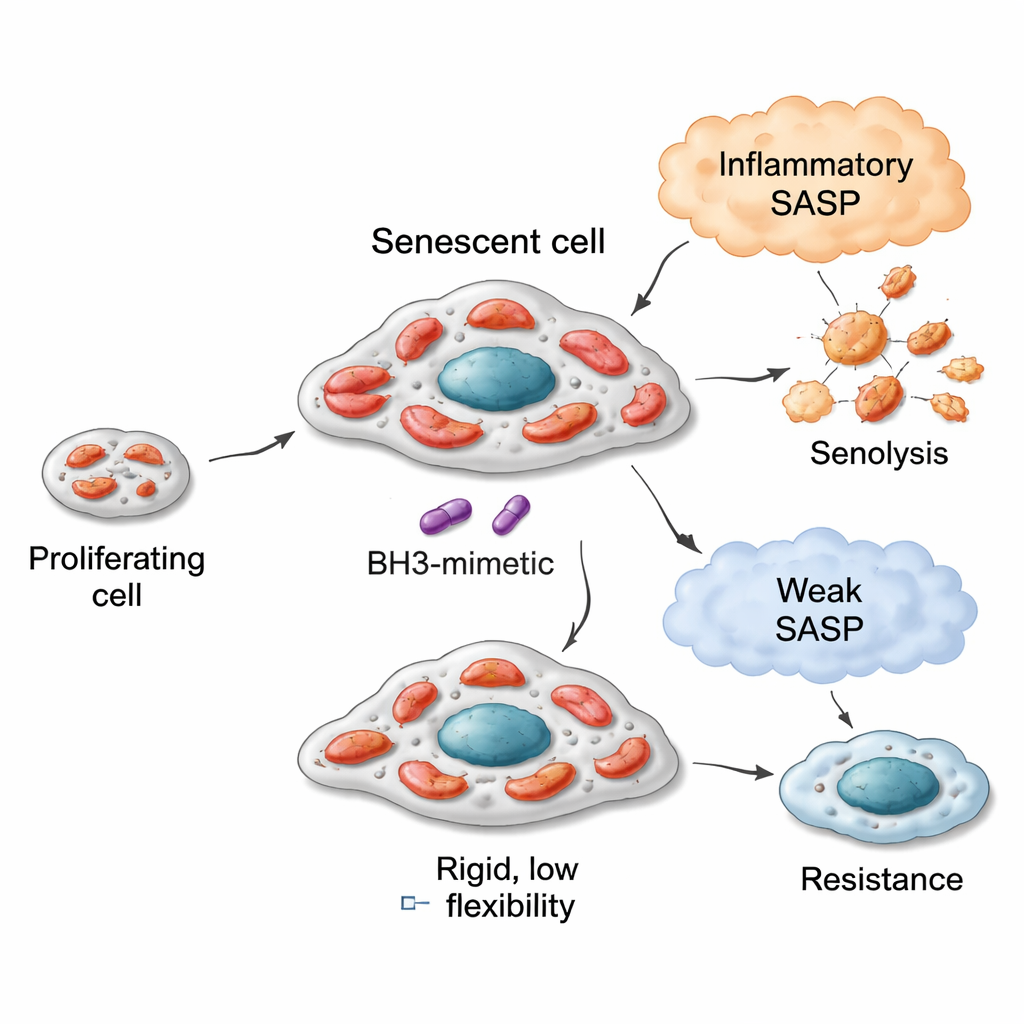
Motores flexibles, distintos combustibles y sensibilidad senolítica
En modelos de cáncer de pulmón, mama y colon, las células senescentes con mitocondrias más flexibles—capaces de oxidar una gama más amplia de combustibles—tendían a ser más vulnerables a senolíticos dirigidos a BCL‑xL como navitoclax (ABT‑263) y A1331852. Por ejemplo, las células de cáncer de pulmón inducidas a senescencia por el fármaco bleomicina desarrollaron mitocondrias que usaban vigorosamente muchos sustratos, especialmente los vinculados a la degradación de ácidos grasos y ciertas vías de aminoácidos. Estas células fueron altamente sensibles a los senolíticos. En contraste, las células llevadas a senescencia por un inhibidor de CDK4/6 (palbociclib) exhibieron un repertorio metabólico más estrecho y respondieron pobremente a los mismos agentes senolíticos. No obstante, esta relación tenía límites: las células de cáncer de mama también podían volverse metabólicamente flexibles tras la senescencia, pero debido a que sus mitocondrias iniciales estaban menos “preparadas” para la apoptosis, su respuesta senolítica máxima fue modesta. Las células de cáncer de colon con maquinaria apoptótica defectuosa permanecieron resistentes independientemente de cómo cambiara su metabolismo. Una única medida—qué tan bien las células oxidaban el combustible succinato en estado basal—sirvió como un indicador simple de esta capacidad mitocondrial heredada.
Cuando el metabolismo dialoga con la inflamación
Las células senescentes son famosas por el SASP, un cóctel de factores secretos inflamatorios y de crecimiento que pueden influir en los tejidos circundantes. El equipo investigó cómo el metabolismo mitocondrial se conecta con este comportamiento secretor usando células diseñadas con un reportero para miR‑146a, un microARN activado por el regulador maestro inflamatorio NF‑κB. Encontraron que, si bien los perfiles generales del SASP estaban mayormente dictados por el tipo celular, solo ciertos estados senescentes activaban este eje NF‑κB/miR‑146a. Esos eran los mismos estados que respondían bien a los senolíticos contra BCL‑xL. Importante: estas células senescentes «SASP inflamatorio‑positivo» también mostraron mayor uso de la oxidación de ácidos grasos y un aumento transcripcional en genes que transportan grasas de cadena larga hacia las mitocondrias. Bloquear la entrada de ácidos grasos con el fármaco etomoxir atenuó la activación de miR‑146a sin revertir completamente la senescencia, lo que sugiere que la elección del combustible mitocondrial ayuda a permitir un SASP inflamatorio que favorece la senolisis.
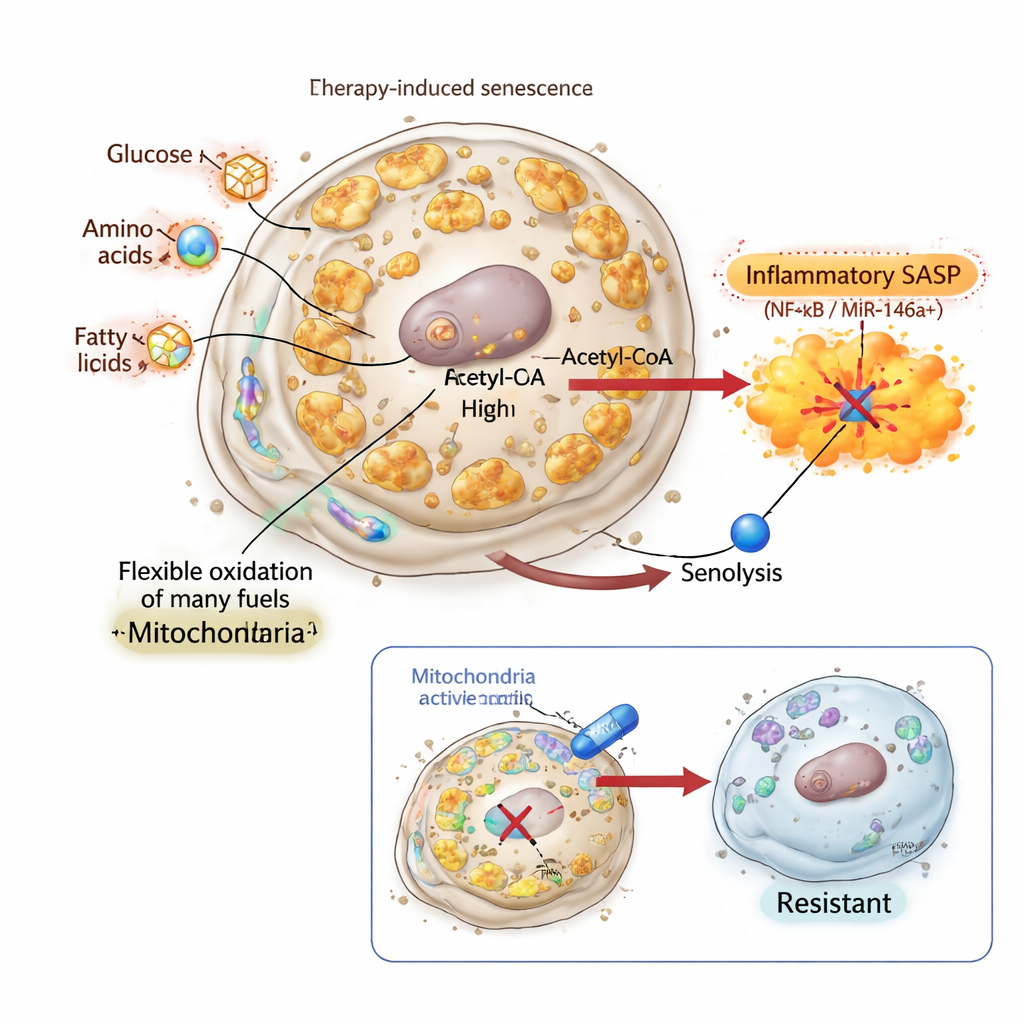
Silenciar la señal y crear células senescentes inmatables
Para probar si el SASP inflamatorio es realmente necesario para la muerte senolítica, los investigadores recurrieron a la inflachromena, un compuesto que se une a las proteínas de la cromatina HMGB1 y HMGB2 y bloquea su papel en la activación de genes del SASP. En células de cáncer de pulmón y mama, la inflachromena indujo un fenotipo senescente de manual: las células se volvieron grandes, dejaron de dividirse y acumularon marcadores de senescencia. Su masa mitocondrial y la actividad bioenergética aumentaron sustancialmente, y el uso de combustibles se remodeló claramente. Sin embargo, su SASP quedó debilitado y el reportero de miR‑146a permaneció en gran medida silencioso. De forma llamativa, estas células senescentes sin SASP fueron completamente resistentes a senolíticos dirigidos a BCL‑xL, a pesar de tener mitocondrias reprogramadas y bioenergéticamente activas y una expresión reducida del clásico gen antiapoptótico BCL2. Esto demostró que los cambios mitocondriales por sí solos no bastan; sin una salida inflamatoria impulsada por la mitocondria, el «segundo golpe» senolítico fracasa.
Qué significa esto para futuros tratamientos contra el cáncer
Para el lector general, la conclusión del estudio es que eliminar las células «zombi» inducidas por la terapia está gobernado por un circuito por capas. Primero, la salud y el cableado original de las mitocondrias de una célula tumoral determinan hasta dónde pueden llegar los fármacos senolíticos. Segundo, el tratamiento particular que provoca la senescencia puede empujar el metabolismo mitocondrial hacia más o menos flexibilidad, acercando o alejando a las células del umbral de la apoptosis. Tercero—y lo más decisivo—los senolíticos solo funcionan bien si la reprogramación metabólica activa con éxito un programa SASP inflamatorio que se comunique con el núcleo. Sin ese diálogo inflamatorio, las células senescentes pueden convertirse en un estado final resistente a los fármacos. En la práctica, esto sugiere que las terapias futuras podrían optimizarse mediante pruebas funcionales tanto de la flexibilidad mitocondrial como de la inflamación del SASP en los tumores, y luego seleccionar combinaciones de fármacos inductores de senescencia y senolíticos que aseguren que las células «zombi» no solo queden congeladas, sino preparadas para ser eliminadas.
Cita: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Palabras clave: senescencia celular, mitocondrias, senolíticos, metabolismo del cáncer, SASP inflamatorio