Clear Sky Science · es
La reducción de SREBP1 desencadena ferroptosis al suprimir el eje Nrf2-XCT/GPX4 en el cáncer de ovario
Volver la fábrica de grasas del cáncer en su contra
El cáncer de ovario se detecta a menudo en etapas avanzadas y puede ser muy difícil de tratar. Este estudio explora una vulnerabilidad sorprendente en estos tumores: su dependencia de la síntesis de grasas y lípidos. Los investigadores muestran que apagar un interruptor clave de la “fábrica de grasas” en las células cancerosas puede tanto frenar su crecimiento como activar un tipo particular de muerte celular, además de facilitar que el sistema inmunitario ataque el tumor.
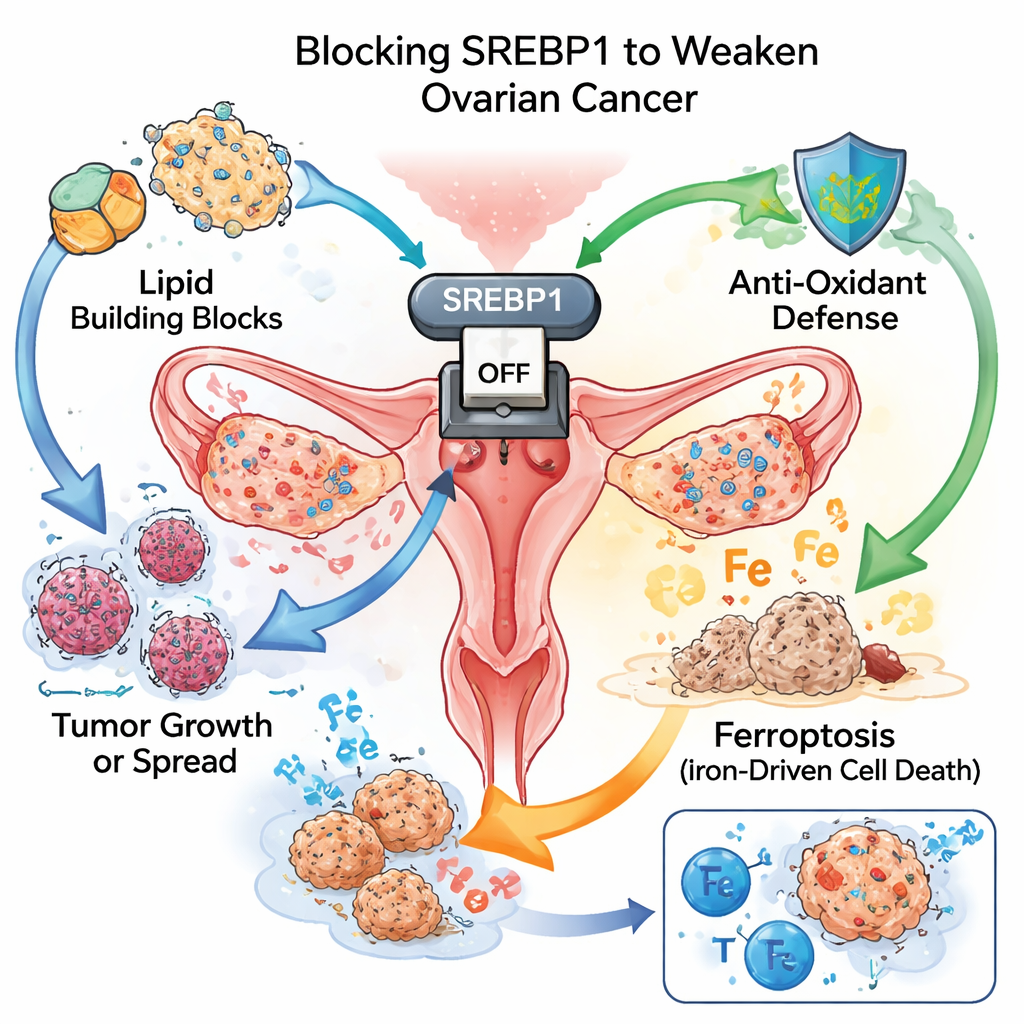
Un interruptor maestro para el combustible tumoral
Como malas hierbas de rápido crecimiento, las células tumorales necesitan grandes cantidades de bloques de construcción y energía. Una forma de satisfacer esta demanda es reprogramar cómo sintetizan y utilizan las grasas. El equipo se centró en SREBP1, una proteína que actúa como interruptor maestro de la producción de lípidos. En muestras de tejido de más de un centenar de pacientes, los tumores ováricos presentaban niveles de SREBP1 mucho más altos que el tejido normal circundante. Las mujeres cuyos tumores mostraban una tinción más intensa de SREBP1 tendieron a tener una enfermedad más agresiva y una supervivencia más corta, lo que señala a esta proteína tanto como impulsora de la progresión como marcador de mal pronóstico.
Frenar el crecimiento y la diseminación cortando el suministro de lípidos
En líneas celulares de cáncer de ovario cultivadas en el laboratorio, reducir SREBP1 disminuyó drásticamente la capacidad de las células para multiplicarse y formar colonias. Las células se quedaron bloqueadas en fases específicas del ciclo celular, lo que impidió su división eficiente. Los investigadores también observaron menos señales de movimiento e invasión: pruebas de herida y Transwell mostraron que las células con menos SREBP1 migraban menos, y marcadores clave de un proceso de cambio de forma llamado EMT volvieron hacia un estado más “normal”. Al mismo tiempo, las mediciones de triglicéridos y colesterol cayeron, y las tinciones mostraron menos gotas lipídicas dentro de las células, lo que confirma que su maquinaria interna de síntesis de grasas había sido reducida.
Desencadenando una muerte celular alimentada por hierro
El efecto más llamativo de bloquear SREBP1 fue la activación de la ferroptosis, una forma de muerte celular reconocida recientemente que está impulsada por el hierro y la oxidación (peroxidación) de las membranas celulares. Solo un inhibidor de la ferroptosis, y no inhibidores de otras vías de muerte, pudo rescatar a las células con SREBP1 silenciado, lo que apunta a la ferroptosis como la causa principal de su desaparición. Pruebas químicas mostraron más productos de daño derivado de lípidos oxidados, menos glutatión antioxidante y mayores niveles de moléculas lipídicas reactivas. Dos proteínas que normalmente protegen a las células de la ferroptosis, llamadas xCT y GPX4, se redujeron de forma marcada cuando se disminuyó SREBP1, eliminando un amortiguador protector crucial frente a este proceso destructivo.
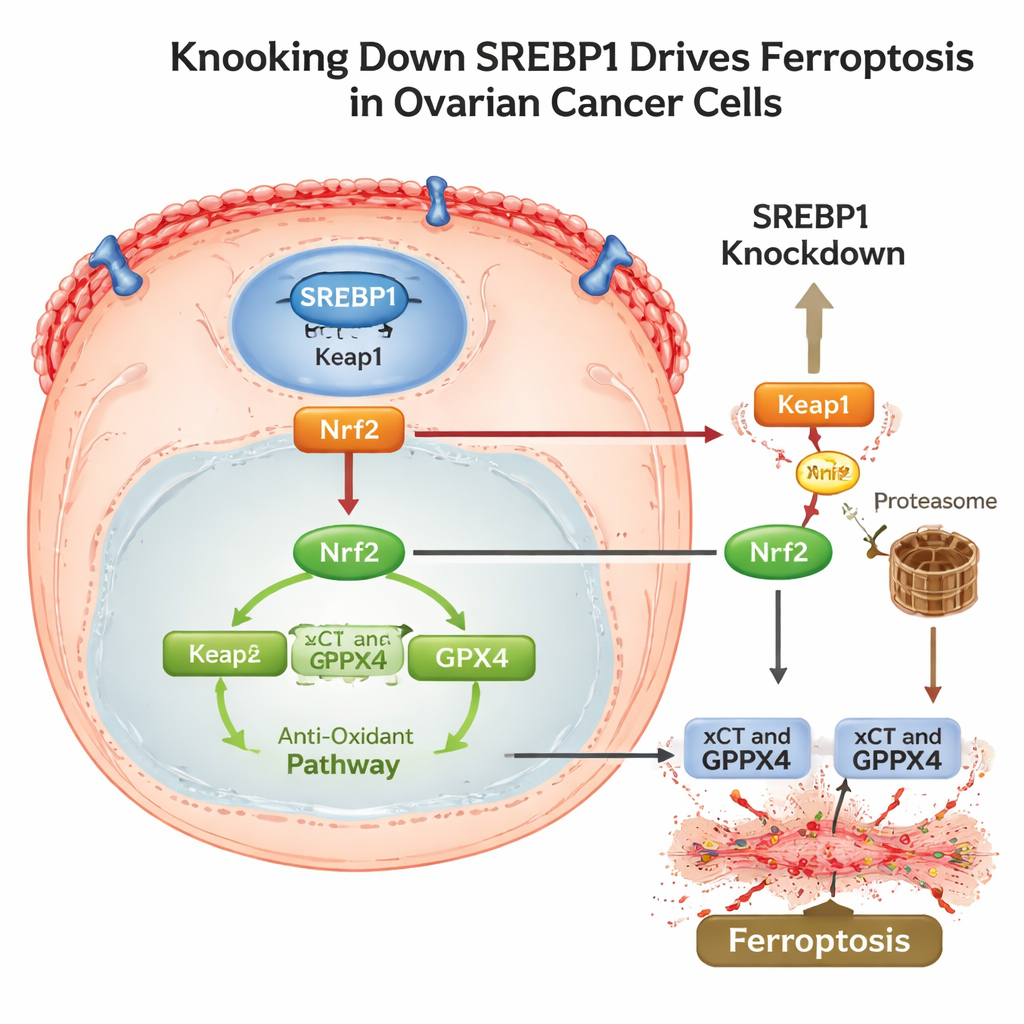
Desarmando el escudo antioxidante y las artimañas de evasión
Para entender cómo SREBP1 se conecta con este programa de muerte, los científicos trazaron una vía a través de otra proteína principal de respuesta al estrés, Nrf2. En condiciones normales, Nrf2 ayuda a las células a sobrevivir activando genes antioxidantes, incluidos xCT y GPX4. El estudio encontró que la reducción de SREBP1 aumentó los niveles de Keap1, una proteína que marca a Nrf2 para su eliminación, lo que condujo a una mayor degradación de Nrf2 y a menos presencia de esta proteína en el núcleo. A medida que Nrf2 disminuyó, sus defensas descendentes se debilitaron y siguió la ferroptosis. De forma importante, los tumores ricos en SREBP1 también mostraron niveles más altos de PD-L1, una proteína de superficie que ayuda a las células cancerosas a ocultarse de los linfocitos T atacantes. Cuando SREBP1 se silenció en tumores de ratón, los cánceres crecieron más despacio, mostraron más señales de daño lipídico, menos Nrf2 y GPX4, y menor PD-L1, junto con una mayor actividad inmunitaria.
Por qué esto importa para futuros tratamientos
En términos sencillos, los tumores ováricos parecen usar SREBP1 como una herramienta de doble filo para sobrevivir: alimentan su crecimiento al aumentar la producción de lípidos y, al mismo tiempo, se arman con un escudo antioxidante y un disfraz inmunológico. Este trabajo muestra que apagar SREBP1 puede privar al tumor de lípidos, quitarle su protección contra el daño impulsado por el hierro y reducir su capacidad para evadir el ataque inmune. Eso convierte a SREBP1 en un objetivo atractivo para nuevos fármacos y sugiere que combinar inhibidores de SREBP1 con tratamientos que induzcan ferroptosis o liberen al sistema inmunitario podría ofrecer a las pacientes un control de su enfermedad más eficaz y duradero.
Cita: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Palabras clave: cáncer de ovario, metabolismo de lípidos, ferroptosis, SREBP1, inmunidad tumoral