Clear Sky Science · es
PDHA1 aumenta la resistencia a la ferroptosis en el cáncer de próstata resistente a la anoikis mediante la regulación al alza de AIFM2
Por qué algunas células de cáncer de próstata se niegan a morir
Cuando las células cancerosas se desprenden de un tumor y entran en el torrente sanguíneo, la mayoría deberían morir antes de llegar a un nuevo órgano. Sin embargo, una minoría peligrosa sobrevive, viaja y siembra metástasis que a menudo resultan letales. Este estudio plantea una pregunta clave: ¿qué permite a ciertas células de cáncer de próstata resistir una forma de muerte celular que normalmente las alcanza al perder el contacto con su tejido de origen? Al desvelar un circuito de supervivencia oculto dentro de estas células, la investigación apunta a nuevas maneras de bloquear la metástasis en su origen.
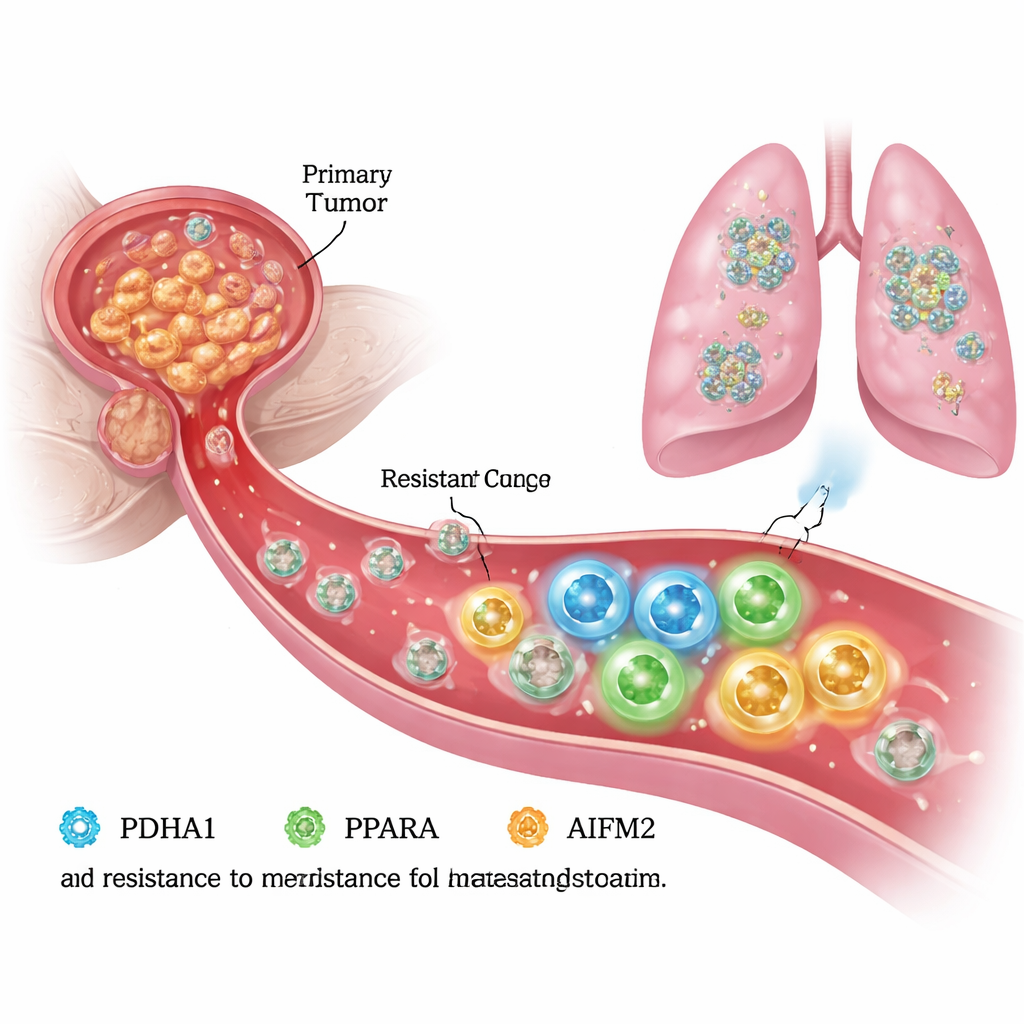
Escapando a la muerte en el torrente sanguíneo
Para propagarse, las células de cáncer de próstata deben soportar la vida sin el apoyo del tejido circundante, conocido como matriz extracelular. En estas condiciones “desprendidas”, las células sanas sufren una muerte programada llamada anoikis, y muchas células cancerosas también son vulnerables a un proceso relacionado, dependiente del hierro, llamado ferroptosis. Los autores generaron en el laboratorio células de cáncer de próstata resistentes a la anoikis y las compararon con sus células “parentales” originales. Encontraron que las células resistentes no solo migraban e invadían con más agresividad, sino que también sobrevivían mejor bajo condiciones de desprendimiento, lo que sugiere que habían reconfigurado su maquinaria interna para evitar la ferroptosis y seguir creciendo.
Un cambio metabólico con una segunda función
Profundizando, el equipo se centró en una enzima metabólica llamada PDHA1, conocida principalmente por ayudar a las células a convertir el piruvato derivado de la glucosa en acetil-CoA en las mitocondrias, alimentando la producción de energía. En las células resistentes a la anoikis, los niveles y la actividad de PDHA1 eran notablemente más altos, y las muestras de pacientes mostraron más PDHA1 en tumores primarios de hombres cuyo cáncer de próstata se había diseminado a ganglios linfáticos o sitios distantes. Cuando los investigadores redujeron PDHA1, las células resistentes perdieron gran parte de su capacidad de moverse, invadir y sobrevivir. Sorprendentemente, una porción sustancial de PDHA1 en estas células ya no estaba confinada a las mitocondrias; se había reubicado en el núcleo, donde el ADN se empaqueta con histonas que pueden modificarse químicamente para activar o silenciar genes.
Reescribir la actividad génica para bloquear la ferroptosis
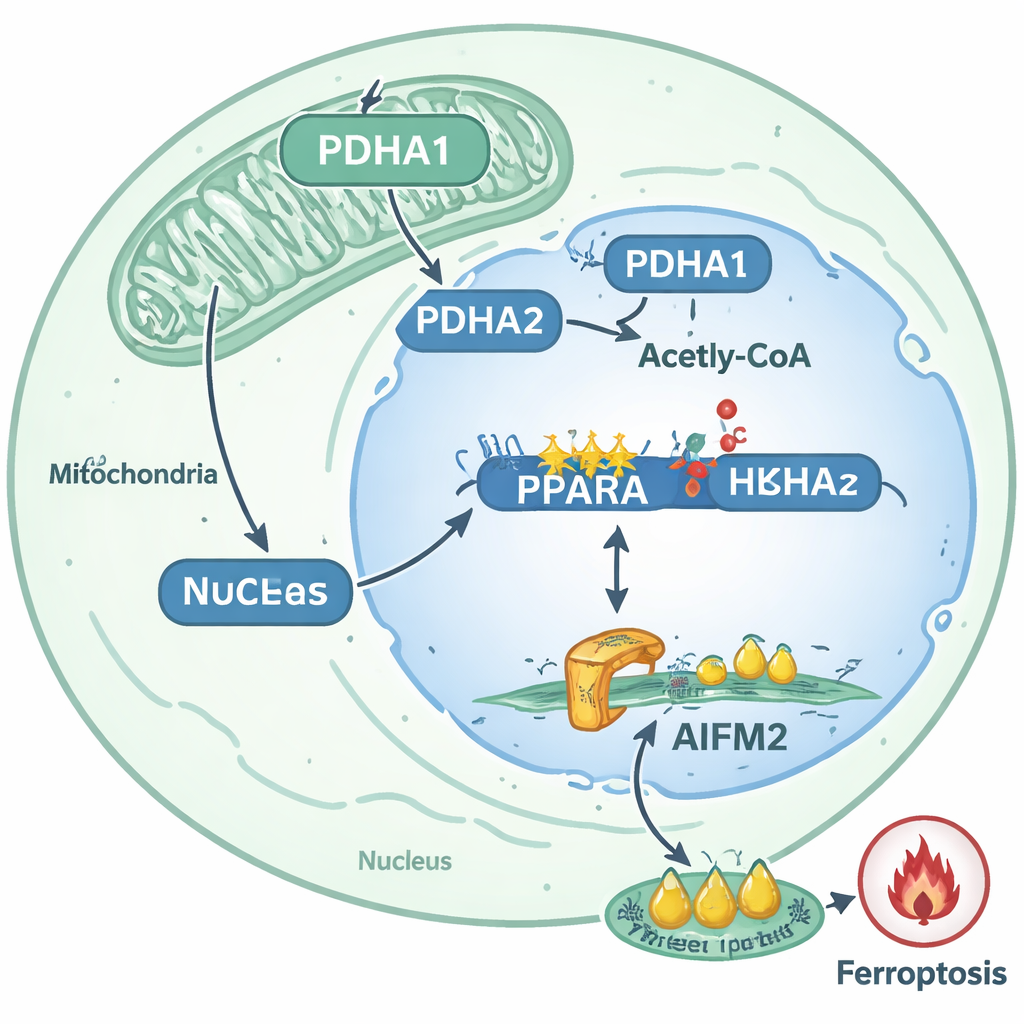
Dentro del núcleo, PDHA1 parecía impulsar la producción local de acetil-CoA, un bloque de construcción clave para la acetilación de histonas. Los autores mostraron que PDHA1 nuclear aumentaba una marca específica, la acetilación de H3K9, en la región de control de un gen llamado PPARA. Este cambio actuó como aflojar los “carretes” de la cromatina, haciendo más fácil activar PPARA. PPARA, a su vez, funcionó como un interruptor maestro que incrementó la producción de otra proteína, AIFM2, al unirse a su promotor y elevar su transcripción. Así, en lugar de ajustar directamente el gen AIFM2, PDHA1 actuó a través de PPARA, estableciendo una vía de varios pasos desde el metabolismo alterado hasta la regulación génica alterada.
Construir un escudo contra el daño inducido por el hierro
AIFM2 se conoce como un freno interno de la ferroptosis: ayuda a proteger los lípidos de las membranas celulares de la oxidación destructiva. En las células resistentes de cáncer de próstata, la regulación al alza de PDHA1 aumentó los niveles de AIFM2, mientras que la reducción de PDHA1 los disminuyó. Pruebas funcionales mostraron que reducir PDHA1 intensificó los rasgos característicos de la ferroptosis: más especies reactivas de oxígeno, más daño lipídico, menor potencial de membrana mitocondrial y la contracción característica de las mitocondrias—especialmente cuando las células se exponían al fármaco que induce ferroptosis, erastina. La sobreexpresión de AIFM2 revirtió estos efectos, rescatando la supervivencia celular en cultivos y restaurando la metástasis pulmonar en ratones, incluso cuando PDHA1 estaba suprimida. Esto confirmó que AIFM2 es un efector descendente crítico de la resistencia a la ferroptosis mediada por PDHA1.
Del circuito molecular a ideas terapéuticas
Al trazar estos sucesos, el estudio describe una vía clara por la que las células de cáncer de próstata desprendidas se vuelven más difíciles de matar: PDHA1 se traslada al núcleo, aumenta la acetilación de histonas en el gen PPARA, potencia la actividad de PPARA y, por tanto, eleva los niveles de AIFM2 para bloquear la ferroptosis. Esta vía está fuertemente vinculada al comportamiento metastásico en tumores de pacientes y en modelos animales. Para el público general, la conclusión es que ciertas células cancerosas reconvierten una enzima metabólica habitual en una herramienta epigenética que reconfigura la actividad génica y construye un escudo bioquímico contra una potente forma de muerte celular. Los autores sugieren que fármacos dirigidos a PDHA1, PPARA o AIFM2—o terapias que desencadenen deliberadamente la ferroptosis—podrían, en el futuro, combinarse para despojar a las células metastásicas de próstata de esta ventaja de supervivencia y hacerlas mucho más vulnerables durante su viaje más crítico: el salto de un órgano a otro.
Cita: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Palabras clave: metástasis del cáncer de próstata, ferroptosis, resistencia a la anoikis, PDHA1, AIFM2