Clear Sky Science · es
La polimerasa de ADN kappa estabilizada por Ptbp2 interacciona con MRE11 y promueve la inestabilidad genómica en la leucemia
Cómo las células leucémicas mantienen el ADN roto y aún así sobreviven
Nuestro ADN está constantemente bajo ataque, pero las células sanas suelen ser muy eficaces para detectar y reparar el daño. En la leucemia, sin embargo, algunas células aprenden a convivir con ADN roto e inestable e incluso convierten esa inestabilidad en una ventaja para sobrevivir. Este estudio desvela una “alianza” molecular entre una proteína del empalme (Ptbp2), una enzima especial que copia el ADN (la polimerasa de ADN kappa, o Polk) y un factor sensor de daños (MRE11) que ayuda a las células leucémicas a reparar lo justo para mantenerse con vida, mientras acumulan el caos genético que impulsa la progresión del cáncer.
Un ayudante oculto en las células leucémicas
Los investigadores se centraron en la leucemia mieloide crónica (LMC), un cáncer de la sangre generalmente impulsado por la fusión génica BCR::ABL1. Aunque los fármacos modernos que bloquean BCR::ABL1 funcionan bien en fases tempranas, muchos pacientes en la fase agresiva de “crisis blástica” responden mal. Trabajos previos mostraron que Ptbp2, una proteína que se une al ARN e influye en el procesamiento de los mensajes, se ve aumentada por BCR::ABL1 y actúa como oncogén en la LMC. Aquí, el equipo descubrió que Ptbp2 se une a la región final (3′ UTR) del ARN mensajero de Polk y lo protege de la degradación. Como resultado, las células leucémicas producen más proteína Polk cuando los niveles de Ptbp2 son altos.
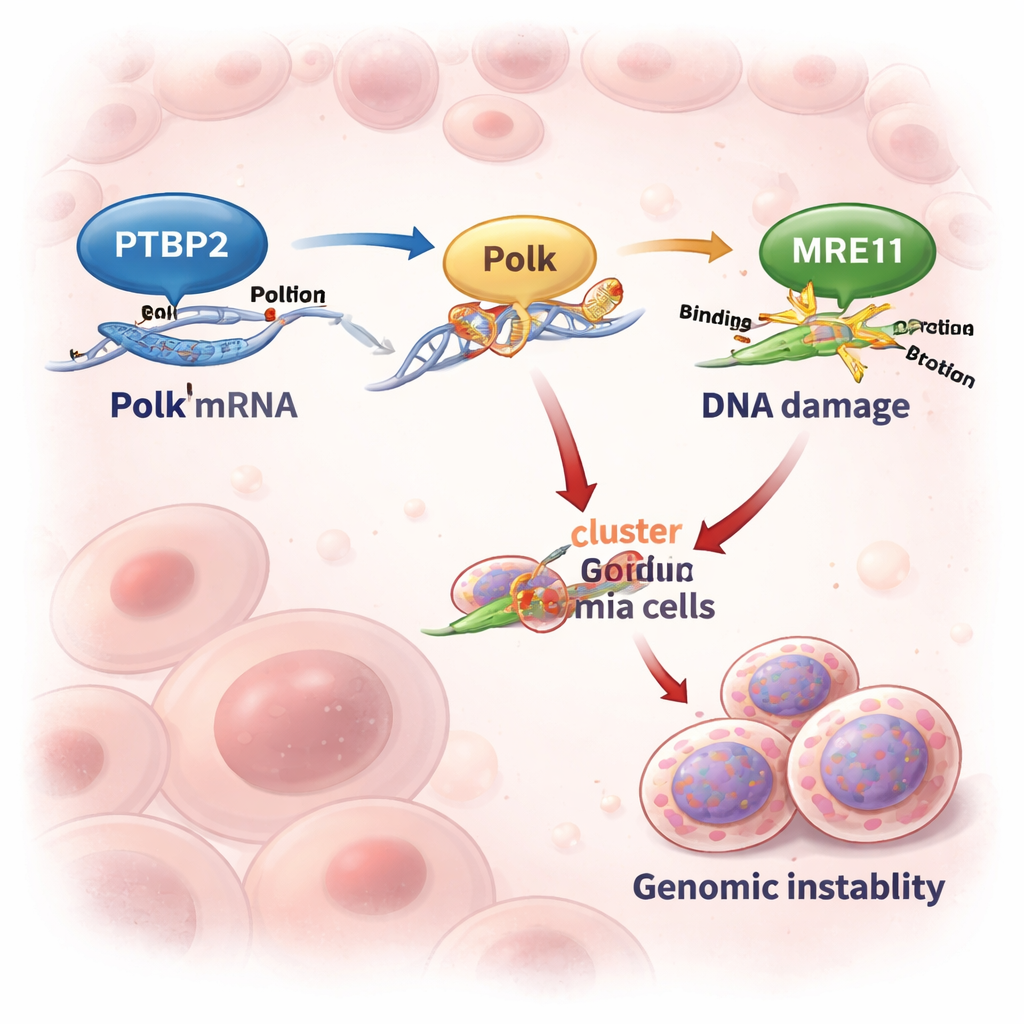
Activando una máquina de copia del ADN propensa a errores
Polk es una polimerasa de ADN “de reserva” que puede copiar sobre ADN dañado cuando la maquinaria de replicación habitual se detiene. Esta capacidad puede rescatar a células estresadas, pero tiene un costo, porque Polk es propensa al error y puede introducir mutaciones. En líneas celulares y muestras de pacientes con LMC avanzada, los niveles de Ptbp2 y Polk subían y bajaban de manera correlacionada. Cuando los científicos eliminaron Ptbp2 en células leucémicas, los niveles de Polk cayeron drásticamente y el ARN de Polk decayó casi el doble de rápido. Reintroducir Polk en las células deficientes en Ptbp2 restauró su comportamiento, demostrando que el papel principal de Ptbp2 aquí es mantener a Polk abundante y activa.
Reparando el daño—pero no a la perfección
Para evaluar cómo este dúo afecta la reparación del ADN, los investigadores trataron las células con hidroxiurea, un fármaco que detiene la replicación del ADN y que se usa con frecuencia en pacientes con LMC. Las células sin Ptbp2 sufrieron mucho más daño en el ADN, visible como largas “colas de cometa” y focos intensos de γH2AX—marcadores de roturas cromosómicas. Estas células dañadas eran más propensas a morir. En cambio, las células con altos niveles de Ptbp2 y Polk toleraron mejor el fármaco, repararon el daño con más eficiencia y sobrevivieron, aunque su reparación fue descuidada. La sobreexpresión de Polk en células con eliminación de Ptbp2 rescató esta sensibilidad, confirmando que la asociación Ptbp2–Polk ayuda a las células leucémicas a superar el estrés de replicación y evitar la apoptosis.
Una red de daño del ADN que favorece la inestabilidad
La historia no termina con Polk. El equipo mostró que Polk interacciona físicamente con MRE11, un miembro clave del complejo MRN que detecta roturas en el ADN y activa la vía de respuesta al daño ATM–CHK2. Cuando se eliminó Ptbp2, Polk disminuyó, los niveles y la actividad de MRE11 cayeron y la señalización ATM–CHK2 se debilitó. Reponer Polk restauró a MRE11 y su activación. Experimentos detallados con fibras de ADN revelaron que Ptbp2 y Polk ayudan a proteger las horquillas de replicación detenidas de ser degradadas, en gran medida a través de MRE11. Bloquear MRE11 con un fármaco socavó esta protección de las horquillas y aumentó el daño en el ADN. Paradójicamente, las células con señalización activa Ptbp2–Polk–MRE11 acumularon más anomalías cromosómicas, como intercambios entre cromátidas hermanas, roturas, huecos, husos multipolares y células gigantes multinucleadas—señales clásicas de inestabilidad genómica que pueden alimentar un cáncer más agresivo.
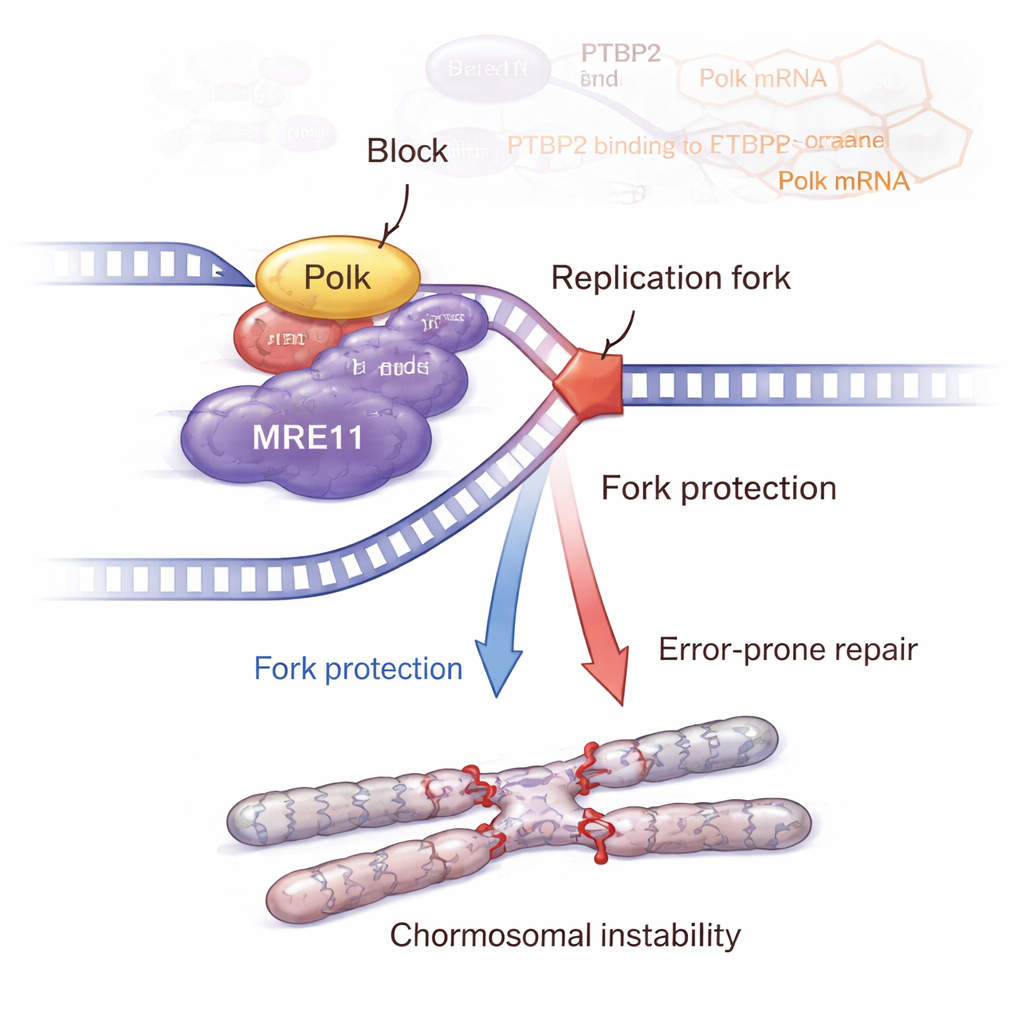
De los ratones a posibles nuevos tratamientos
En modelos murinos, las células leucémicas con Ptbp2 intacto produjeron tumores más grandes y más anormales que las células sin Ptbp2. Los tejidos de estos ratones mostraron niveles más altos de Ptbp2, Polk, el marcador de proliferación Ki-67 y estructuras de división celular distorsionadas. En un modelo murino separado similar a la LMC impulsado por BCR::ABL1, añadir Ptbp2 adicional aumentó Polk y el número de células en división atípicas y conglomerados leucémicos invasivos en bazo e hígado, lo que apunta a una progresión más rápida de la enfermedad. En conjunto, estos hallazgos sugieren que el eje Ptbp2–Polk–MRE11–ATM–CHK2 permite a las células leucémicas sobrevivir a un estrés intenso del ADN mientras van acumulando mutaciones perjudiciales de forma sostenida.
Por qué esto importa para los pacientes
Para un público general, el mensaje clave es que algunas células leucémicas evaden el control caminando con cuidado por una cuerda floja: reparan su ADN lo suficiente para seguir vivas, pero no tan bien como para evitar las mutaciones. Ptbp2 estabiliza a Polk, que a su vez se asocia con MRE11 para proteger el ADN estresado y mantener en marcha las señales de daño—sin embargo, esa reparación es imperfecta y promueve el caos genético. Dado que la LMC avanzada y otros cánceres parecen depender de este frágil equilibrio, dirigir terapias contra Ptbp2 o su control sobre Polk podría inclinar la balanza para que las células abandonen la supervivencia y tiendan hacia la autodestrucción, ofreciendo una estrategia terapéutica prometedora, especialmente en la difícil etapa de crisis blástica.
Cita: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Palabras clave: leucemia mieloide crónica, inestabilidad genómica, reparación del ADN, polimerasa de ADN kappa, PTBP2