Clear Sky Science · es
Mitofagia en el cáncer de páncreas: ideas mecanísticas e implicaciones para nuevas estrategias terapéuticas
Por qué importan las centrales energéticas de nuestras células en el cáncer de páncreas
El adenocarcinoma ductal pancreático es uno de los cánceres más letales, en parte porque los tumores aprenden rápidamente a resistir casi todos los tratamientos disponibles. Este artículo de revisión explora un protagonista sorprendente en esa historia de resistencia: la mitofagia, el sistema integrado de la célula para identificar y reciclar mitocondrias deterioradas, las pequeñas “centrales eléctricas” que generan energía. Comprender cómo el cáncer de páncreas secuestra este proceso de limpieza podría abrir nuevas vías hacia terapias más eficaces y duraderas.
Equipos de limpieza celular y los trucos de supervivencia del cáncer
Las mitocondrias hacen mucho más que generar energía; ayudan a controlar el metabolismo, la muerte celular y el manejo de moléculas dañinas llamadas especies reactivas de oxígeno. Cuando las mitocondrias están dañadas o son excesivas, las células utilizan la mitofagia para marcarlas y eliminarlas. Esto puede ocurrir por dos vías principales. Una, conocida como la vía PINK1/Parkin, depende de un sensor de daño (PINK1) y una enzima etiquetadora (Parkin) para señalar las mitocondrias defectuosas para su destrucción. La otra utiliza proteínas receptoras como BNIP3, NIX y FUNDC1 situadas en la superficie mitocondrial para conectarlas directamente con las bolsas de eliminación celular, llamadas autofagosomas, sin el mismo paso de marcado. Estas vías suelen trabajar juntas, ofreciendo a las células maneras flexibles de adaptar su reserva mitocondrial al estrés, como la baja disponibilidad de oxígeno o la exposición a fármacos. 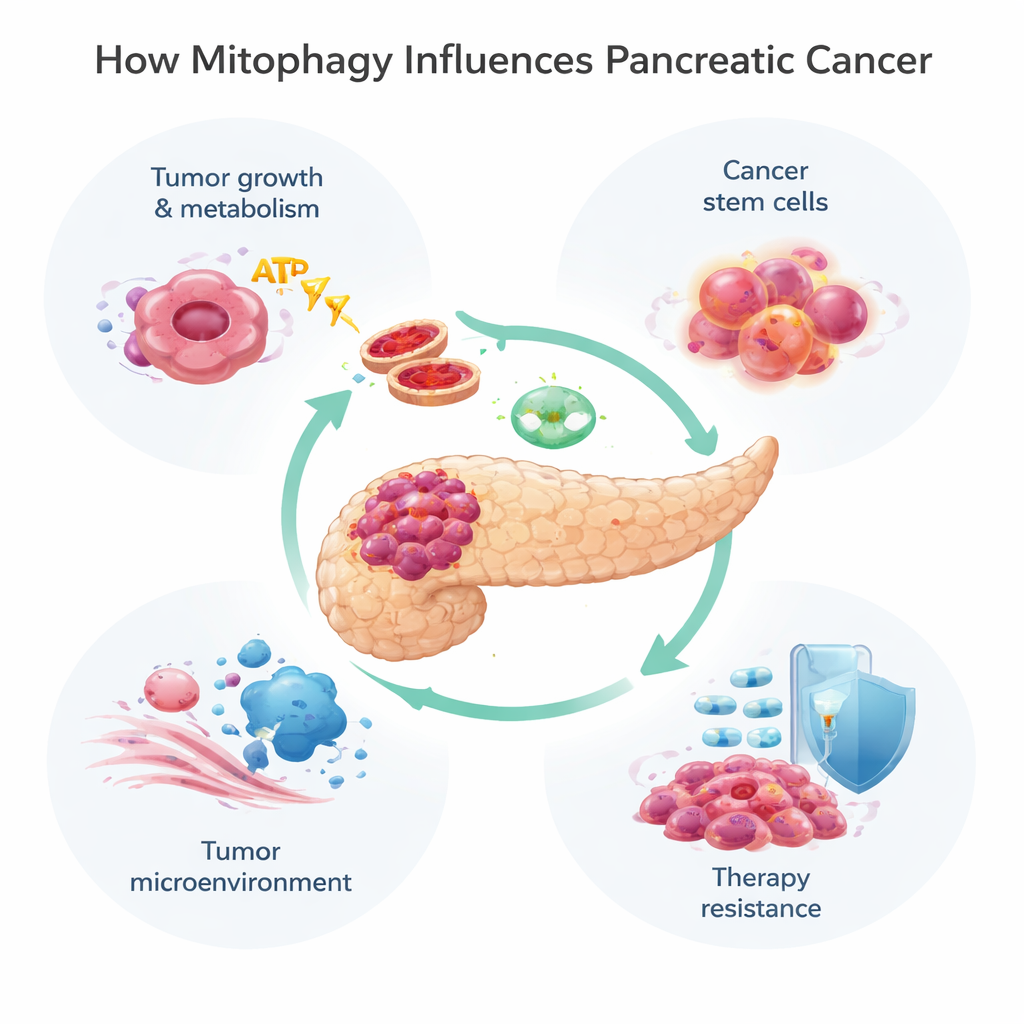
Cómo los tumores pancreáticos remodelan su uso de energía
Los tumores pancreáticos viven en un entorno hostil: tienen un suministro deficiente de sangre y oxígeno y están rodeados por un tejido denso tipo cicatriz. Para sobrevivir, las células cancerosas reprograman sus sistemas energéticos, a menudo desplazándose de la respiración mitocondrial dependiente de oxígeno a un proceso más primitivo de quema de azúcar conocido como glucólisis. La mitofagia ayuda a afinar este cambio. En etapas tempranas del desarrollo tumoral, la pérdida de PINK1 o Parkin acelera la formación del cáncer al permitir la acumulación de hierro, el exceso de especies reactivas de oxígeno y el impulso hacia la glucólisis. Al mismo tiempo, otra proteína de mitofagia, NIX, puede ayudar a eliminar mitocondrias todavía funcionales, empujando a las células aún más hacia un metabolismo glucolítico y un crecimiento más rápido. En contraste, BNIP3 muestra un patrón más complejo: aparece temprano, más tarde se silencia en muchos tumores avanzados y, cuando se restaura, puede ralentizar el crecimiento de las células cancerosas, lo que sugiere que algunas rutas de mitofagia restringen el cáncer mientras que otras lo impulsan.
Células madre cancerosas y el vecindario tumoral
No todas las células cancerosas son iguales. Un subconjunto pequeño, a menudo llamado células madre cancerosas, puede autorrenovarse, generar nuevos tumores y resistir particularmente bien la quimioterapia. En el cáncer de páncreas, estas células dependen de la mitofagia para mantener su flexibilidad metabólica. Una proteína modificadora llamada ISG15 apoya este proceso y ayuda a conservar sus rasgos similares a células madre, vinculando la mitofagia directamente con la recaída y el fracaso del tratamiento. Más allá de las propias células cancerosas, la mitofagia también moldea el microambiente tumoral —la mezcla de células de soporte, células inmunitarias y tejido conectivo alrededor del tumor. Por ejemplo, los fibroblastos asociados al cáncer pueden verse empujados a un “efecto Warburg inverso”, en el que aumentan su propia mitofagia y glucólisis y luego alimentan al tumor con subproductos ricos en energía. La mitofagia también influye en cómo las células inmunitarias reconocen y atacan el cáncer, al alterar la presentación de señales inmunitarias como el MHC‑I y los frenos como PD‑L1 que usan los tumores para ocultarse.
Por qué bloquear o potenciar la limpieza puede cambiar la respuesta a los fármacos
Muchos tratamientos estándar y experimentales para el cáncer de páncreas, incluido el fármaco quimioterápico gemcitabina y un nuevo fármaco dirigido contra la mutación KRAS‑G12D, dañan las mitocondrias. Las células tumorales a menudo responden activando la mitofagia, eliminando el daño y escapando a la muerte. Los estudios muestran que la mitofagia impulsada por PINK1 puede atenuar los efectos letales de la quimioterapia y de algunos compuestos naturales, ayudando a las células cancerosas a sobrevivir. Por otro lado, en determinadas condiciones, forzar la mitofagia en exceso —especialmente a través de BNIP3 y NIX— puede despojar a las células de demasiadas mitocondrias funcionales, precipitando una crisis energética y promoviendo la muerte celular. Esta naturaleza dual significa que la mitofagia puede proteger a los tumores frente al tratamiento o, si se manipula de forma adecuada, volverlos más vulnerables. 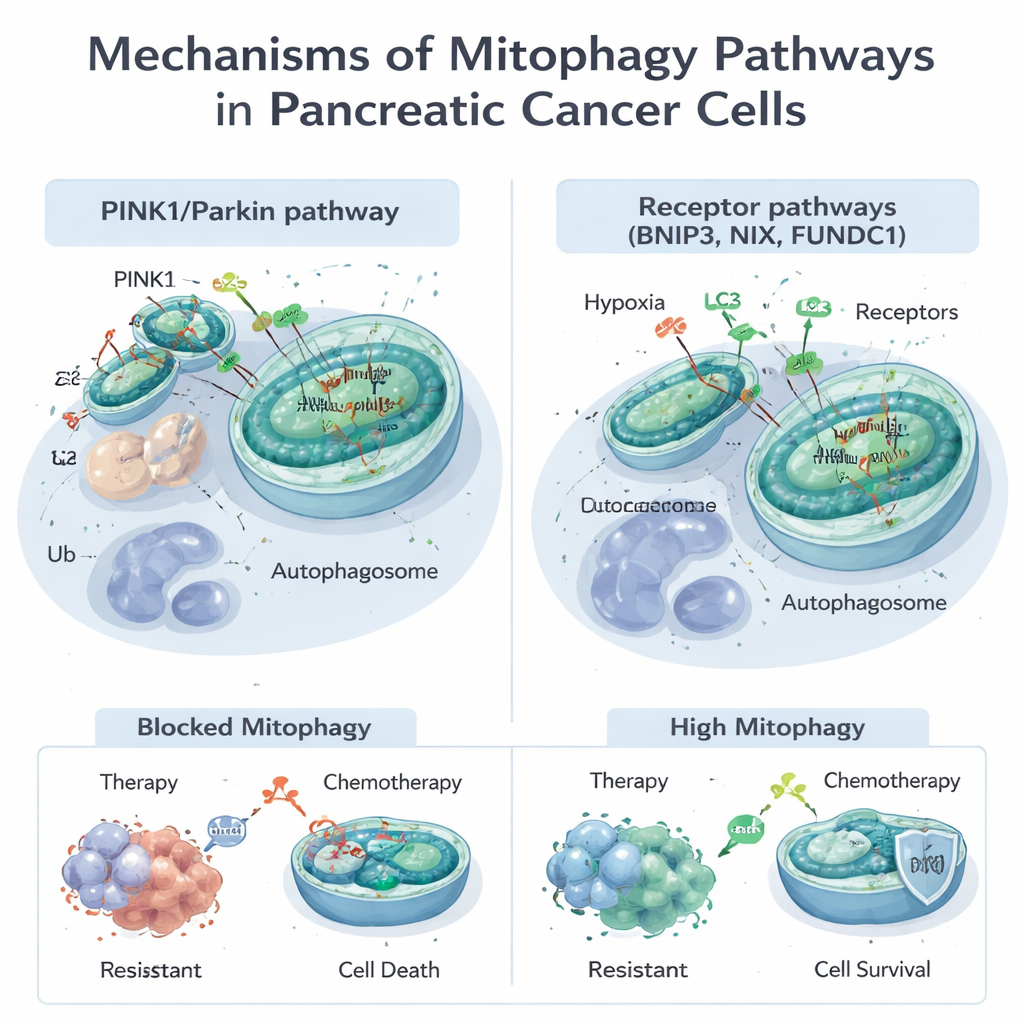
Nuevas ideas terapéuticas y la necesidad de una selección inteligente de pacientes
Dado que la mitofagia se sitúa en la encrucijada del metabolismo, las respuestas al estrés y la muerte celular, es un objetivo atractivo para terapias combinadas. Las estrategias farmacológicas actuales actúan mayoritariamente de forma indirecta: algunos compuestos interfieren con la fisión y fusión mitocondrial; otros, como la cloroquina y la hidroxicloroquina, bloquean las etapas finales del proceso de reciclaje al deshabilitar la fusión de los sacos de desecho con los compartimentos ácidos de degradación. Varios ensayos clínicos están probando estos fármacos junto con la quimioterapia estándar en cáncer de páncreas. Sin embargo, los resultados hasta ahora son heterogéneos: algunos pacientes se benefician y otros no. Parte del problema es que los tumores difieren ampliamente en sus perfiles basales de mitofagia y metabolismo: unos dependen en gran medida de la respiración mitocondrial y otros de la glucólisis. Los autores sostienen que el éxito futuro dependerá de mejores biomarcadores y firmas génicas para agrupar a los pacientes según su actividad de mitofagia y uso energético, y del desarrollo de fármacos más precisos que ajusten selectivamente vías específicas de mitofagia en lugar de activar o bloquear la autofagia de forma tosca. Para el lector general, la idea clave es que aprender a leer y a ajustar con cuidado este sistema de limpieza mitocondrial podría ayudar a convertir el cáncer de páncreas de un enemigo obstinado en una enfermedad más manejable.
Cita: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Palabras clave: cáncer de páncreas, mitofagia, mitocondrias, resistencia a la quimioterapia, metabolismo tumoral