Clear Sky Science · es
Las células madre mesenquimales primadas atenúan la fibrosis por esquistosomiasis al potenciar el cambio de subtipos de macrófagos y la eférofagocitosis mediante el eje Itgb2-Rac1
Reduciendo las cicatrices hepáticas de un parásito común
La esquistosomiasis, una enfermedad parasitaria que afecta a más de 200 millones de personas en todo el mundo, a menudo deja tras de sí cicatrices persistentes en el hígado incluso después de eliminar los gusanos. Estas cicatrices, conocidas como fibrosis, pueden progresar hacia cirrosis e insuficiencia hepática potencialmente mortal. Este estudio explora un nuevo tratamiento celular que enseña a las propias células inmunitarias del organismo a limpiar el daño con mayor eficacia, ofreciendo un enfoque novedoso para revertir la cicatrización hepática inducida por parásitos.
Por qué las cicatrices hepáticas son difíciles de curar
Cuando los gusanos Schistosoma depositan huevos en el hígado, el sistema inmunitario forma cúmulos compactos de células—granulomas—a su alrededor. Con el tiempo, esta respuesta protectora deposita tejido cicatricial en exceso, endureciendo gradualmente el hígado. Un papel clave en este proceso lo desempeñan los macrófagos, el equipo de limpieza del organismo. Un subtipo, llamado macrófagos “inflamatorios”, alimenta el daño al liberar señales químicas agresivas; otro subtipo, más “resolutivo”, ayuda a descomponer la cicatriz y a calmar la inflamación. La pregunta central de este trabajo es si podemos inducir de forma segura a los macrófagos a pasar del estado dañino al reparador.
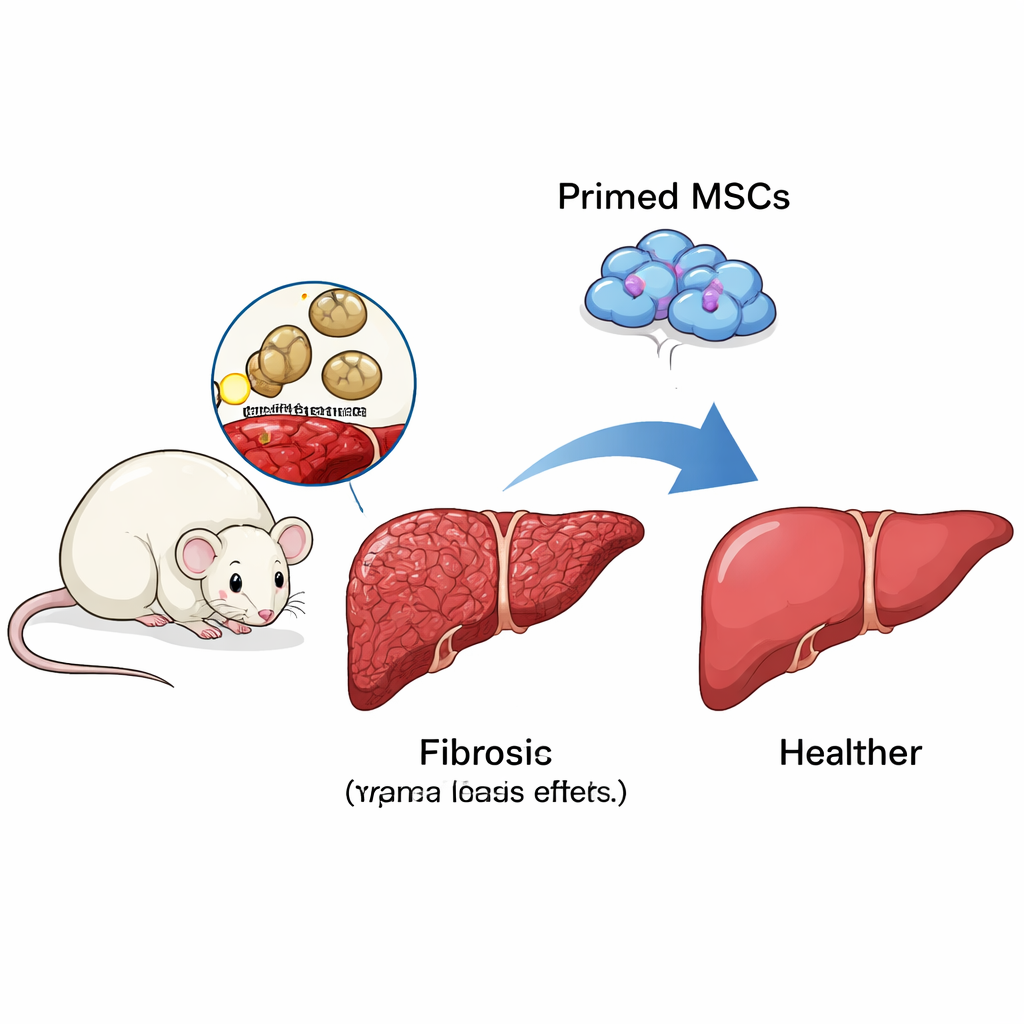
Entrenando células madre para guiar al sistema inmune
Las células madre mesenquimales (CMM)—células versátiles presentes en la médula ósea y otros tejidos—han despertado interés como posible tratamiento para la fibrosis hepática. Por sí solas, sin embargo, no siempre funcionan bien. Los investigadores hallaron que “primar” las CMM en el laboratorio con dos señales inmunitarias, IFN-γ y LPS, mejoró de forma notable su eficacia en ratones infectados con Schistosoma japonicum. Comparados con animales no tratados o con aquellos que recibieron CMM no primadas, los ratones que obtuvieron CMM primadas tenían hígados de mejor aspecto a simple vista, ganaron más peso y mostraron granulomas mucho más pequeños y menor acumulación de colágeno al microscopio. Los marcadores de células activadas formadoras de cicatriz también disminuyeron, indicando una reducción real de la fibrosis y no solo cambios cosméticos.
Reprogramando al equipo de limpieza del organismo
Indagando más a fondo, el equipo midió cómo las CMM primadas afectaban el comportamiento de los macrófagos. En los hígados tratados había menos macrófagos inflamatorios y más del subtipo pro-resolutor, mejor capacitado para desmantelar la fibrosis. Al mismo tiempo, los niveles de moléculas proinflamatorias clásicas cayeron, mientras que los factores útiles para la reparación se mantuvieron en un rango equilibrado en lugar de dispararse. Cuando los investigadores bloquearon la llegada de nuevos macrófagos inflamatorios al hígado, tanto el número de células resolutorias como los beneficios sobre la fibrosis disminuyeron. Esto sugiere que las CMM primadas no se limitan a añadir células nuevas, sino que convierten a los macrófagos inflamatorios entrantes en una forma más pacífica y orientada a la reparación.
Ayudando a los macrófagos a comer para curar
El estudio se centró luego en un proceso denominado eférofagocitosis: la “ingestión” ordenada de células moribundas, especialmente neutrófilos agotados, otro tipo de célula inmunitaria. En ratones infectados tratados con CMM primadas, los macrófagos hepáticos eran con mucha más frecuencia encontrados con neutrófilos ingeridos en su interior, señal de una limpieza activa. En cultivos, los macrófagos expuestos a CMM primadas mejoraron su capacidad para engullir neutrófilos apoptóticos marcados y, en paralelo, modificaron su actividad génica hacia un perfil pro-resolutor. Los investigadores identificaron una diana molecular clave para este cambio: un receptor llamado Itgb2 en los macrófagos, que comunica con un interruptor interno, Rac1, que controla el esqueleto celular y el movimiento de engullir. Las CMM primadas aumentaron tanto la actividad de Itgb2 como de Rac1; bloquear cualquiera de los dos redujo drásticamente la eférofagocitosis y revirtió el cambio hacia macrófagos de tipo reparador.
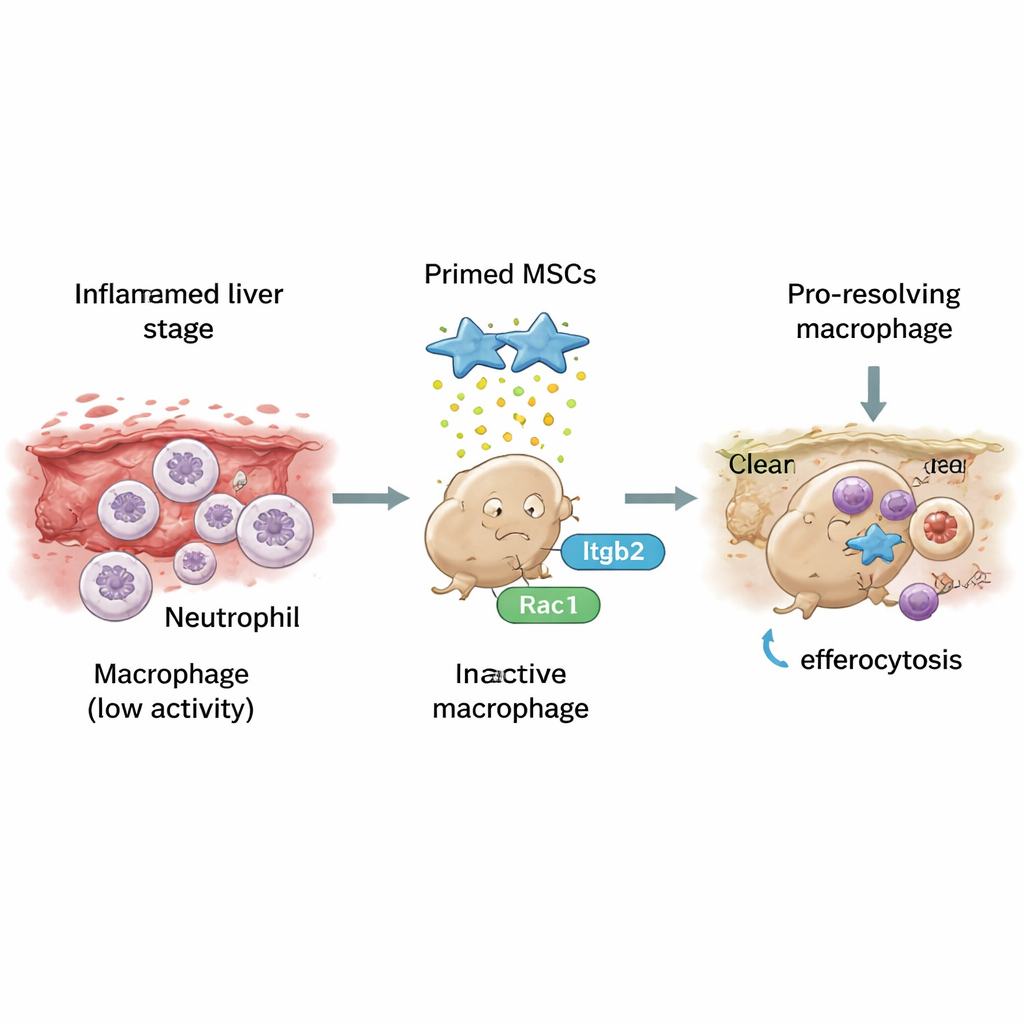
Qué podría significar esto para tratamientos futuros
En términos sencillos, el trabajo muestra que células madre especialmente primadas pueden actuar como “entrenadoras” de las células inmunitarias tras la esquistosomiasis, animándolas a dejar de avivar la inflamación y, en su lugar, eliminar escombros y tejido cicatricial con mayor eficacia. Al activar la vía Itgb2–Rac1, estas CMM primadas ayudan a que los macrófagos dispongan con fluidez de las células moribundas y adopten luego una personalidad resolutiva contra la fibrosis. Aunque queda mucho por hacer antes de poder probar este enfoque en personas, el estudio proporciona una hoja de ruta mecanicista clara para diseñar terapias basadas en CMM que no solo supriman el daño, sino que además ayuden activamente al hígado a reconstruirse tras la infección parasitaria.
Cita: Lei, J., Ren, Y., Chen, Z. et al. Primed mesenchymal stem cells attenuate schistosomiasis fibrosis by enhancing macrophage subset switching and efferocytosis via Itgb2-Rac1 axis. Cell Death Discov. 12, 97 (2026). https://doi.org/10.1038/s41420-026-02947-w
Palabras clave: esquistosomiasis, fibrosis hepática, células madre mesenquimales, macrófagos, eférofagocitosis