Clear Sky Science · es
La osteopontina derivada del cáncer colorrectal reconecta a los macrófagos hacia un estado M2 pro‑metastásico a través del eje PI3K/AKT/CSF1‑CSF1R
Por qué esto importa para las personas con cáncer de colon
La mayoría de las muertes por cáncer colorrectal (de colon y recto) no se deben al tumor primario, sino a su diseminación a otros órganos. Este estudio investiga cómo las células cancerosas «se comunican» con las células inmunitarias cercanas para facilitar la propagación tumoral. Al descubrir una señal clave que las células cancerosas envían para reprogramar a las células inmunitarias y convertirlas en colaboradoras en lugar de combatientes, el trabajo apunta a nuevas estrategias terapéuticas que podrían ralentizar o detener la metástasis en el cáncer colorrectal avanzado.
Una proteína pegajosa con un lado oscuro
Los investigadores se centraron en una proteína llamada osteopontina, u OPN, que la producen tanto las células cancerosas como ciertas células inmunitarias dentro de los tumores. La OPN lleva tiempo asociada a peores desenlaces en muchos cánceres, pero no estaba claro cómo promovía la diseminación en el cáncer colorrectal. Mediante el análisis de grandes bases de datos de pacientes y muestras tumorales, el equipo encontró que los niveles de OPN eran mucho más altos en tejido de cáncer colorrectal que en tejido de colon normal, especialmente en pacientes con enfermedad avanzada y metástasis a distancia. Los pacientes cuyos tumores mostraban más OPN tendían a tener una supervivencia peor, lo que sugiere que la OPN está estrechamente ligada a formas agresivas y difíciles de tratar del cáncer.
No son solo las propias células cancerosas
Sorprendentemente, cuando los científicos forzaron a las células de cáncer colorrectal en el laboratorio a producir más o menos OPN, las células no se volvieron por sí mismas más invasivas ni más móviles. Su proliferación, migración y capacidad para invadir a través de membranas artificiales cambiaron muy poco. Esto cuestionó la idea común de que la OPN actúa principalmente potenciando de forma directa la agresividad intrínseca de las células tumorales. En lugar de eso, el equipo examinó el vecindario del tumor—el llamado microambiente tumoral—y en particular a un grupo de células inmunitarias llamadas macrófagos, que pueden atacar a los tumores (estado «M1») o apoyarlos (estado «M2»).
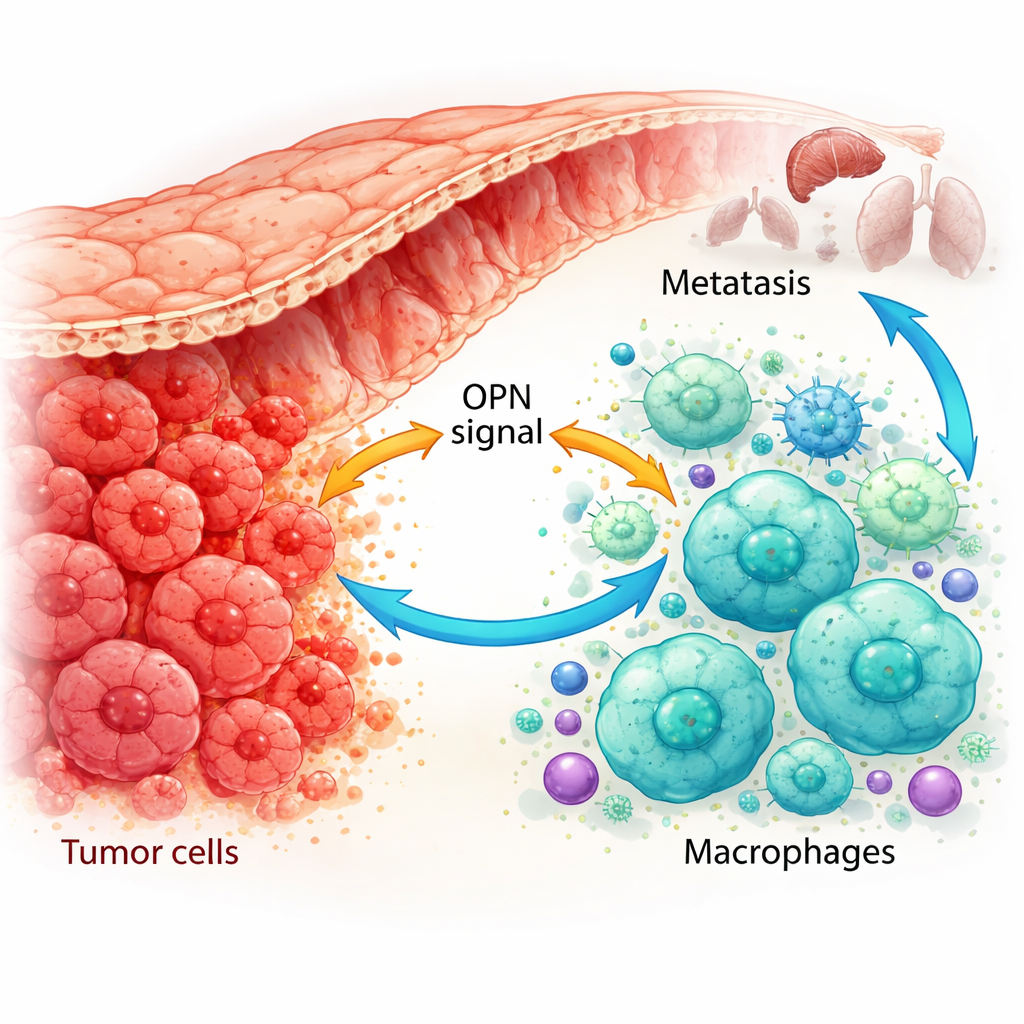
Cómo las células inmunitarias se reconvierten en cómplices del tumor
Utilizando mapas genéticos de célula única y tinciones avanzadas de tejidos de pacientes, los investigadores mostraron que la OPN no solo la producen las células cancerosas, sino también macrófagos asociados al tumor. En tumores que ya se habían diseminado, tanto las células cancerosas como un subtipo específico de macrófagos mostraban altos niveles de OPN. Estos macrófagos tendían a presentar un estado similar a M2, que apoya al tumor, y eran más abundantes cuando los niveles tumorales de OPN eran altos. En modelos murinos, los tumores diseñados para producir más OPN atrajeron más de estos macrófagos M2 y crecieron más rápido, mientras que los tumores con OPN reducida mostraron menos macrófagos M2 y crecieron más despacio. Esto sugiere que la OPN es un reclutador y reprogramador potente de macrófagos en el entorno tumoral.
La cadena de señal oculta: de la OPN a la metástasis
Para desentrañar la cadena molecular de eventos, el equipo cultivó macrófagos humanos junto con células de cáncer colorrectal que producían distintas cantidades de OPN. Encontraron que las células cancerosas con altos niveles de OPN empujaban a los macrófagos hacia el estado M2 y fomentaban un movimiento bidireccional: los macrófagos migraban hacia el tumor y las células tumorales se volvían más invasivas en respuesta a señales procedentes de esos macrófagos. Al profundizar, los científicos descubrieron que la OPN activa en los macrófagos una vía de señalización llamada PI3K/AKT. Esta activación, a su vez, hace que los macrófagos liberen grandes cantidades de otra molécula, CSF1, y aumenten el receptor para esa molécula, CSF1R, en su superficie. CSF1 actúa entonces en un circuito que refuerza aún más el estado M2 pro‑metastásico y mantiene el reclutamiento de macrófagos hacia el tumor.
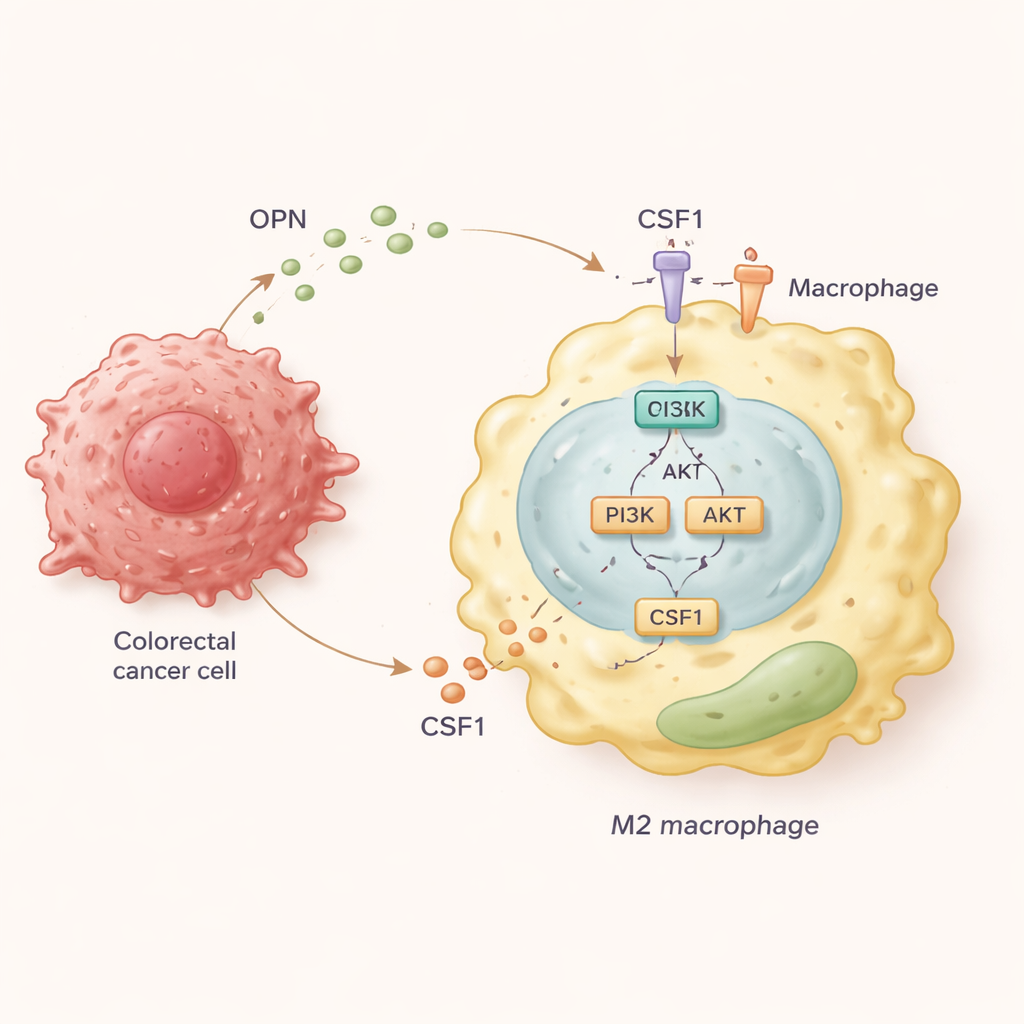
Bloquear el circuito para frenar la diseminación
En modelos murinos de cáncer colorrectal con diseminación intrabdominal, los investigadores probaron un fármaco que bloquea CSF1R llamado PLX3397. Los ratones con tumores ricos en OPN desarrollaron numerosos nódulos metastásicos, pero el tratamiento con el inhibidor de CSF1R redujo de forma significativa tanto el número de metástasis como la presencia de macrófagos de tipo M2 en los tumores. Las células tumorales mostraron menor proliferación y más signos de muerte celular programada. Es importante señalar que el fármaco eliminó principalmente a los macrófagos promotores del tumor sin afectar en gran medida al tipo más inflamatorio, lo que sugiere una forma relativamente selectiva de debilitar el sistema de apoyo tumoral.
Qué significa esto para tratamientos futuros
Para un público general, el mensaje principal es que algunos cánceres colorrectales logran diseminarse no solo porque las células tumorales sean agresivas, sino porque secuestran a las células inmunitarias cercanas y las convierten en cómplices. En este estudio, la OPN derivada de las células cancerosas actúa como un interruptor maestro que reprograma a los macrófagos a través de la cadena de señalización PI3K/AKT y CSF1/CSF1R, creando un terreno fértil para la metástasis. Al interrumpir esta cadena—particularmente en el paso de CSF1R—los investigadores pudieron reducir la diseminación tumoral en ratones. Esto sugiere que medir los niveles de OPN podría ayudar a identificar a los pacientes que podrían beneficiarse de fármacos dirigidos a los macrófagos, y que combinar estos fármacos con tratamientos existentes o inmunoterapias podría ofrecer nuevas esperanzas para personas con cáncer colorrectal avanzado.
Cita: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Palabras clave: cáncer colorrectal, osteopontina, macrófagos asociados a tumores, metástasis, inhibición de CSF1R