Clear Sky Science · es
Rottlerin desencadena la degradación dual de SLC7A11 y GPX4 para inducir ferroptosis y sensibilizar quimioterapéuticamente el carcinoma hepatocelular
Por qué este compuesto natural importa para el cáncer de hígado
El carcinoma hepatocelular, la forma más frecuente de cáncer primario de hígado, suele diagnosticarse en fases avanzadas y sigue siendo difícil de tratar. Este estudio explora si una molécula de origen vegetal llamada rottlerin, conocida desde hace tiempo por sus efectos anticáncer amplios, puede aprovecharse para desencadenar una forma más reciente de muerte celular denominada ferroptosis en células de cáncer hepático. Al comprender cómo actúa rottlerin a nivel molecular, los investigadores esperan abrir nuevas vías para tratamientos más efectivos y con menor probabilidad de generar resistencia.
Una nueva forma de matar células cancerosas
Los fármacos anticancerígenos tradicionales suelen empujar a las células tumorales hacia programas de muerte bien conocidos, como la apoptosis. La ferroptosis es distinto: es un proceso dependiente del hierro impulsado por la acumulación de lípidos tóxicos en las membranas celulares. Las células de cáncer de hígado son especialmente vulnerables a este tipo de daño porque dependen en gran medida de sistemas antioxidantes para controlar estos tóxicos de base lipídica. El equipo preguntó si rottlerin podría sabotear esas defensas y así forzar a las células hepáticas cancerosas a entrar en ferroptosis.
Cómo rottlerin ralentiza el crecimiento tumoral
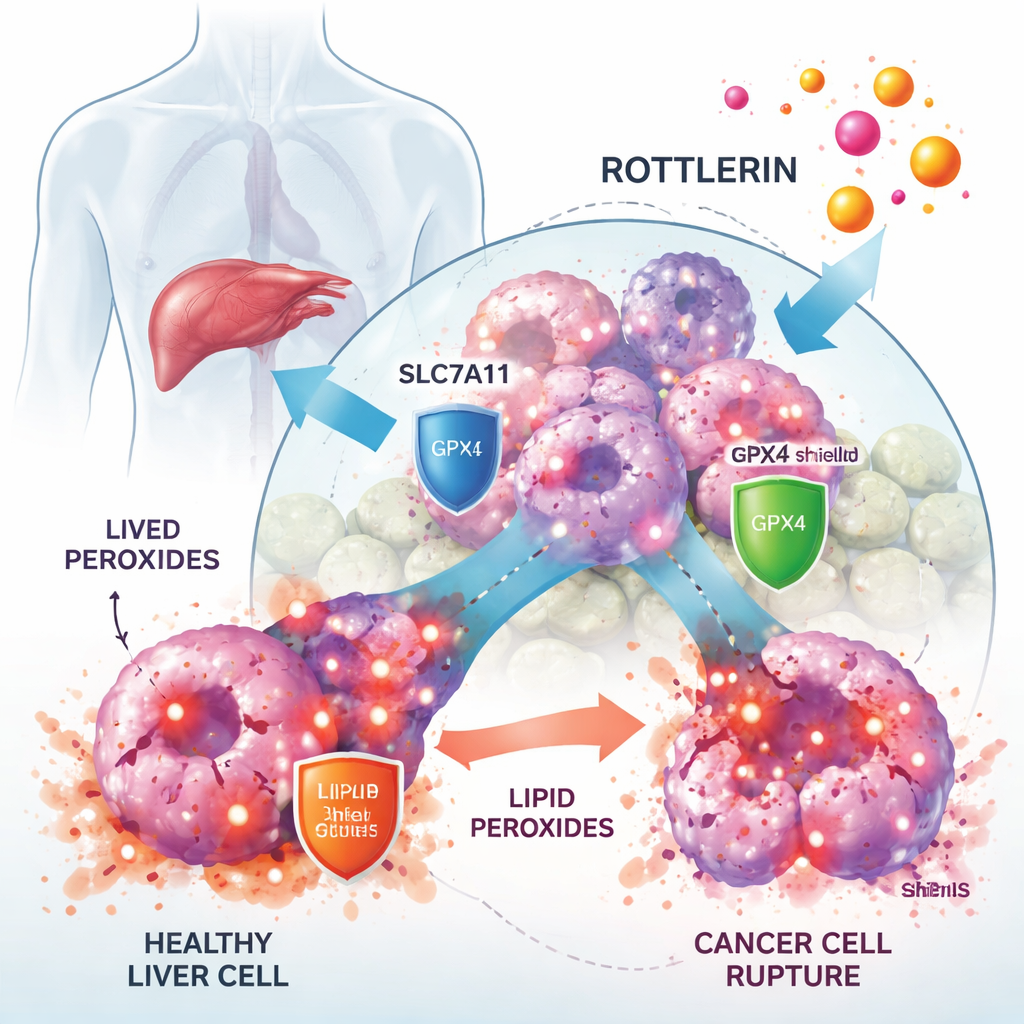
Trabajando con líneas celulares humanas de cáncer hepático, los investigadores mostraron que rottlerin reducía drásticamente el crecimiento de las células cancerosas a concentraciones micromolares bajas, mientras que las células normales relacionadas con el hígado resultaron menos afectadas. Cuando añadieron un bloqueador específico de la ferroptosis llamado Ferrostatin‑1, gran parte de la muerte celular inducida por rottlerin se rescató, lo que sugiere con fuerza que la ferroptosis era el principal modo de muerte. La microscopía y las pruebas bioquímicas respaldaron esto: las células tratadas con rottlerin acumularon altos niveles de peróxidos lipídicos, mostraron mitocondrias alteradas y presentaron cantidades reducidas de la molécula antioxidante glutatión, todas señales características de la ferroptosis.
Desarmando los escudos antioxidantes de las células
Las células de cáncer hepático sobreviven apoyándose en un eje defensivo crítico formado por el transportador SLC7A11 y la enzima GPX4. SLC7A11 importa cistina, un bloque de construcción para el glutatión, mientras que GPX4 usa glutatión para neutralizar peróxidos lipídicos antes de que dañen las membranas. El estudio encontró que rottlerin provocaba una disminución de los niveles de proteína de SLC7A11 y GPX4 con el tiempo. Esto no se debió a que las células dejaran de sintetizarlas, sino a que las proteínas estaban siendo marcadas con pequeñas etiquetas de “destrúyeme” (ubiquitina) y enviadas a la maquinaria de destrucción proteica de la célula, el proteasoma. Bloquear el proteasoma revirtió esta pérdida, y aumentar artificialmente SLC7A11 o GPX4 en las células las protegió de forma parcial frente a rottlerin. En conjunto, estos hallazgos muestran que rottlerin actúa como un degradador dual de dos defensas centrales contra la ferroptosis.
Potenciando fármacos existentes contra el cáncer de hígado
Muchos pacientes con cáncer de hígado avanzado reciben sorafenib, un fármaco de primera línea que por sí mismo puede inducir ferroptosis, pero la resistencia suele limitar su beneficio. Los autores probaron si dosis bajas de rottlerin, de otro modo poco activas, podían hacer que las células tumorales fueran más sensibles a fármacos inductores de ferroptosis como sorafenib y RSL3. En cultivo celular, combinar rottlerin a baja dosis con cualquiera de esos fármacos aumentó notablemente la muerte de las células cancerosas y desplazó las curvas dosis‑respuesta, indicando una mayor potencia. Es importante que este efecto sensibilizador persistió incluso cuando la proteína diana clásica de rottlerin, PKCδ, se redujo genéticamente, lo que muestra que la acción clave no se realiza a través de esta quinasas sino mediante la degradación de SLC7A11 y GPX4. En modelos murinos con tumores hepáticos humanos, el tratamiento combinado de rottlerin y sorafenib ralentizó el crecimiento tumoral más que sorafenib solo y redujo aún más los niveles de SLC7A11 y GPX4 en los tumores.
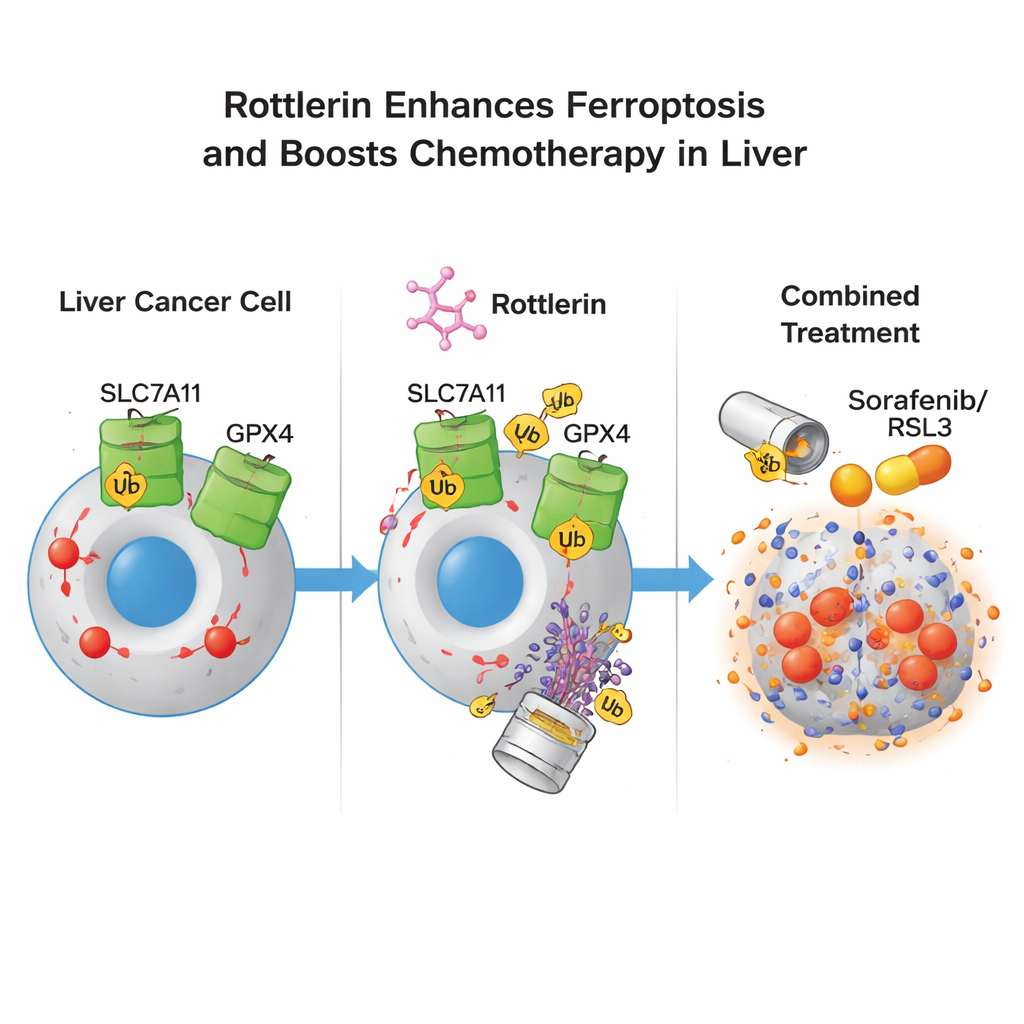
Qué podría significar esto para tratamientos futuros
Para el público general, el mensaje es que rottlerin actúa como una “llave maestra de dos cerrojos” sobre las células de cáncer de hígado: elimina simultáneamente dos cerraduras cruciales —SLC7A11 y GPX4— que normalmente protegen a las células frente a una oleada letal de oxidación lipídica. Una vez que esas cerraduras desaparecen, las células cancerosas son mucho más propensas a sufrir ferroptosis, especialmente cuando se combinan con fármacos existentes que las empujan en esa dirección. Aunque se necesita más trabajo antes de que rottlerin o compuestos relacionados puedan usarse en pacientes, esta estrategia de degradador dual ofrece una vía prometedora para burlar las defensas adaptativas que con frecuencia hacen que los tumores hepáticos sean tan difíciles de tratar.
Cita: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Palabras clave: cáncer de hígado, ferroptosis, rottlerin, SLC7A11, GPX4