Clear Sky Science · es
Apuntar a vulnerabilidades metabólicas: el agonista de REV-ERB SR9009 potencia la eficacia de sorafenib en el cáncer de hígado
Por qué es importante privar de energía a las células cancerosas
El cáncer de hígado es uno de los más letales a nivel mundial, y muchos pacientes con enfermedad avanzada siguen dependiendo de un fármaco antiguo llamado sorafenib. Aunque el sorafenib puede frenar el crecimiento tumoral, las células cancerosas a menudo se adaptan y desarrollan resistencia, lo que limita la supervivencia de los pacientes. Este estudio explora una nueva manera de mejorar el efecto del sorafenib atacando la forma en que las células de cáncer de hígado se alimentan, ofreciendo una visión de tratamientos futuros que podrían golpear más fuerte los tumores sin añadir efectos secundarios graves.
Cómo se quedan cortos los tratamientos actuales para el cáncer de hígado
El sorafenib ha sido durante mucho tiempo un tratamiento básico para pacientes cuyos tumores hepáticos no pueden extirparse quirúrgicamente. Las inmunoterapias más recientes ahora ayudan a algunas personas a vivir más tiempo, pero muchos pacientes no reúnen los requisitos para esos tratamientos o no responden a ellos. Para esos pacientes, el sorafenib sigue siendo importante, sin embargo la resistencia suele aparecer en cuestión de meses. Los investigadores se plantearon una pregunta simple pero potente: ¿qué cambios ocurren dentro de las células de cáncer de hígado que les permiten evadir los efectos del sorafenib, y pueden esos cambios convertirse en nuevos puntos débiles terapéuticos?
Las células cancerosas aumentan sus centrales energéticas
Para encontrar respuestas, el equipo comparó células de cáncer de hígado que aún respondían al sorafenib con células que habían aprendido a sobrevivir al fármaco. Mediante secuenciación masiva de ARN, descubrieron que las células resistentes incrementaron considerablemente la actividad de genes implicados en la fosforilación oxidativa mitocondrial: la vía principal mediante la cual las células generan energía en sus pequeñas “centrales”, las mitocondrias. Otros genes de protección frente al estrés, incluidos los relacionados con el manejo de una molécula llamada hemo, también se vieron reforzados. En conjunto, estos cambios sugieren que las células cancerosas resistentes hacen frente al sorafenib reconfigurando su producción de energía y sus defensas frente al estrés, en lugar de simplemente ignorar los blancos originales del fármaco.
Un segundo fármaco que corta la energía
Los investigadores recurrieron entonces al SR9009, un compuesto experimental diseñado originalmente para actuar sobre proteínas circadianas llamadas REV-ERB que ayudan a controlar el metabolismo. Se sabe que SR9009 interfiere con la actividad mitocondrial y es más perjudicial para las células tumorales que para las normales. Tanto en células de cáncer de hígado de ratón como humanas, la combinación de SR9009 con sorafenib redujo drásticamente la supervivencia celular en comparación con cada fármaco por separado. Los dos fármacos juntos redujeron la producción de energía mitocondrial casi hasta cero, forzando a las células a depender de vías alternativas de consumo de azúcar que no pudieron compensar completamente. Los ensayos de laboratorio mostraron caídas pronunciadas en el ATP celular —la moneda universal de la energía— y menos colonias de células cancerosas sobrevivientes. Importante: los fibroblastos normales y las células hepáticas no cancerosas se vieron mucho menos afectadas, lo que sugiere que la estrategia podría atacar de forma selectiva el tejido tumoral.
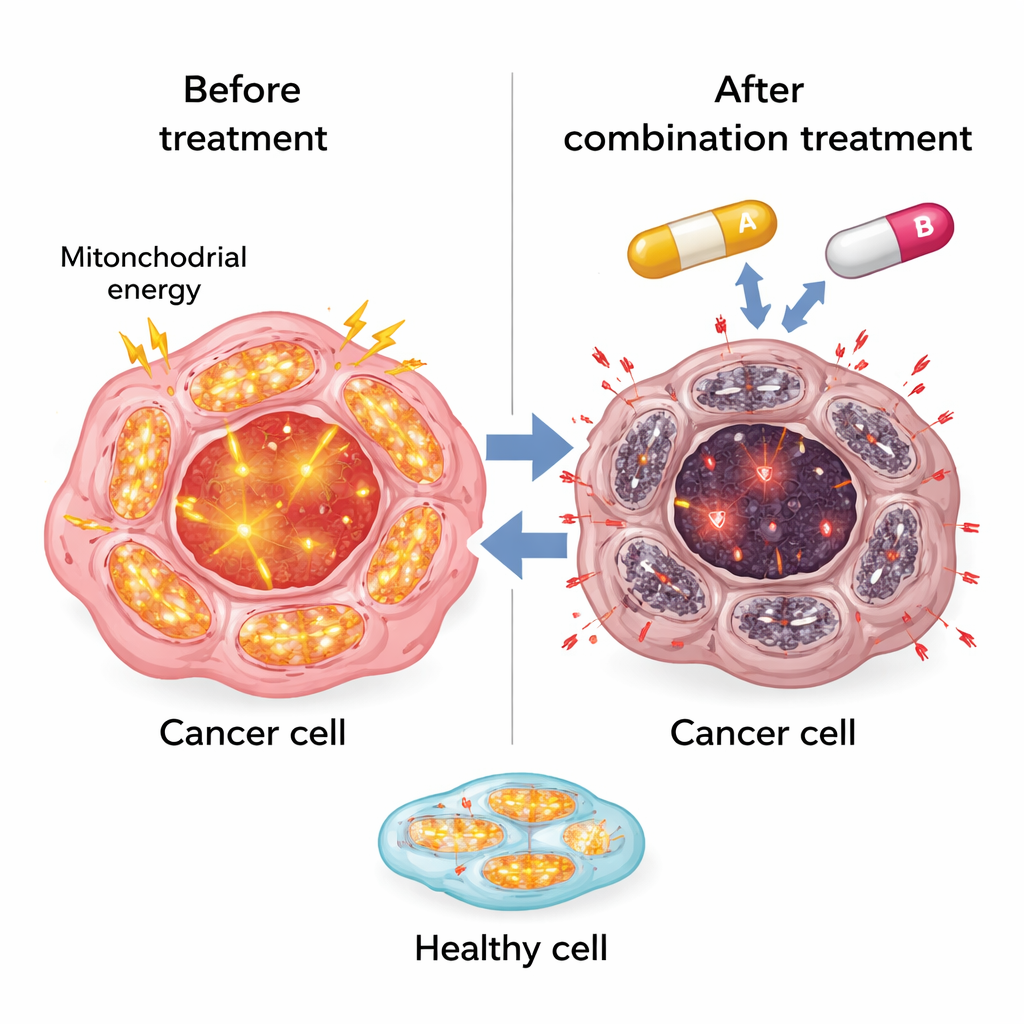
Alteración del equilibrio del hemo y activación de estrés tóxico
El estudio también descubrió una segunda vulnerabilidad: cómo las células resistentes gestionan el hemo, una pequeña molécula que contiene hierro y que es esencial para muchas enzimas, incluidas las mitocondriales. Las células resistentes de cáncer de hígado aumentaron los niveles de HO-1, una enzima que descompone el hemo libre, y elevaron la ferritina, que almacena de forma segura el hierro liberado. Esto parecía protegerlas del daño relacionado con el hemo. SR9009 cambió ese equilibrio. En las células resistentes, SR9009 aumentó los niveles de hemo libre y reforzó marcadores de estrés oxidativo como especies reactivas de oxígeno y daño lipídico, especialmente cuando se combinó con sorafenib. Al mismo tiempo, las proteínas mitocondriales disminuyeron, lo que refuerza la idea de que saturar las centrales energéticas y las defensas frente al estrés empuja a las células cancerosas más allá de un punto de no retorno.
Control tumoral más fuerte en modelos animales
Para ver si estos efectos se traducían más allá de placas de cultivo, el equipo probó la pareja de fármacos en ratones. En animales con tumores hepáticos ordinarios y resistentes al sorafenib, solo la combinación de sorafenib más SR9009 redujo el tamaño de los tumores resistentes. En un modelo independiente en el que los cánceres de hígado surgieron de forma espontánea tras la exposición a un agente cancerígeno, añadir SR9009 a una dosis reducida de sorafenib provocó la reducción tumoral en más del 90% de los nódulos, mientras que los tumores en ratones tratados solo con sorafenib continuaron en su mayoría creciendo. De manera notable, la combinación no aumentó la toxicidad global: los ratones mantuvieron un peso corporal estable, los recuentos sanguíneos permanecieron normales y los marcadores de lesión hepática fueron menores cuando se incluyó SR9009, lo que sugiere un efecto protector sobre el tejido hepático sano.
Qué podría significar esto para los pacientes
Para un lector general, el mensaje clave es que este trabajo describe una forma ingeniosa de hacer que un fármaco existente contra el cáncer de hígado sea más eficaz explotando cómo se adaptan los tumores. Las células resistentes al sorafenib sobreviven en parte al potenciar sus centrales energéticas y sus sistemas de control del estrés. SR9009 derriba esos apoyos, dejando a las células cancerosas privadas de energía y sobrecargadas de subproductos tóxicos, mientras respeta a las células normales. Aunque SR9009 en sí aún no es un medicamento aprobado y estos hallazgos provienen de modelos preclínicos, el estudio proporciona una hoja de ruta: combinar fármacos estándar con agentes que apunten al metabolismo específico del tumor podría vencer la resistencia y permitir dosis más bajas y seguras. A largo plazo, tales estrategias combinadas podrían brindar a los pacientes con cáncer de hígado avanzado más tiempo y mejor calidad de vida.
Cita: Sabbioni, S., Guerriero, P., Shankaraiah, R.C. et al. Targeting metabolic vulnerabilities: REV-ERB agonist SR9009 potentiates sorafenib efficacy in liver cancer. Cell Death Discov. 12, 86 (2026). https://doi.org/10.1038/s41420-026-02940-3
Palabras clave: cáncer de hígado, resistencia a fármacos, metabolismo del cáncer, terapia combinada, mitocondrias