Clear Sky Science · es
Vesículas extracelulares derivadas de CMM aumentan la proliferación y la metástasis del osteosarcoma a través de la vía circRNA-0010220/β-catenina
Por qué importa esta historia sobre el cáncer óseo
El osteosarcoma es el cáncer óseo más frecuente en niños y adultos jóvenes y con frecuencia se disemina a los pulmones. Incluso con quimioterapia y cirugía modernas, muchos pacientes siguen enfrentando recaídas y metástasis potencialmente letales. Este estudio explora las “conversaciones” ocultas entre las células tumorales óseas y las células madre de la médula ósea cercanas, revelando un mensajero molecular diminuto que ayuda a los tumores a crecer y diseminarse —y que podría convertirse en un nuevo objetivo terapéutico.
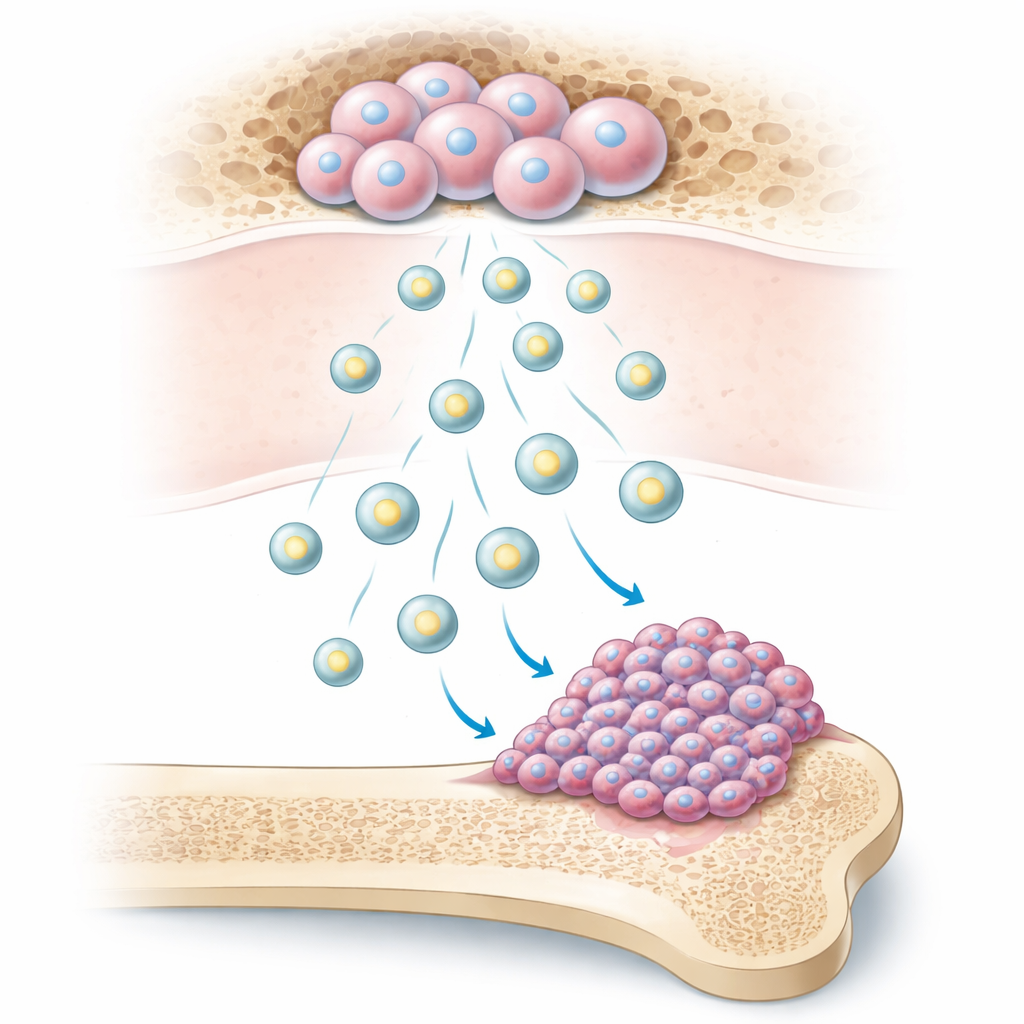
Paquetes minúsculos con gran influencia
Nuestros huesos contienen células madre mesenquimales de la médula ósea, células versátiles que ayudan a mantener y reparar el tejido óseo. Estas células liberan burbujas minúsculas envueltas en membrana llamadas vesículas extracelulares. Los investigadores muestran que las células de osteosarcoma absorben con facilidad estas vesículas. Cuando eso ocurre, las células cancerosas comienzan a dividirse más rápido, forman más colonias, se desplazan con mayor rapidez sobre superficies e invaden barreras en ensayos de laboratorio. En ratones, los tumores expuestos a estas vesículas crecieron más y produjeron más metástasis pulmonares, lo que indica que estos paquetes microscópicos aumentan poderosamente la agresividad del cáncer.
Un mensaje circular que fortalece el cáncer
El equipo examinó luego qué mensajes genéticos dentro de las vesículas alteraban más a las células de osteosarcoma. Se centraron en los ARN circulares, una clase recientemente descubierta de moléculas de ARN que forman lazos cerrados y son inusualmente estables. La secuenciación reveló un candidato destacado, denominado circRNA‑0010220, que aumentó marcadamente en las células de osteosarcoma tratadas con vesículas de células madre y en muestras tumorales de pacientes. Cuando los científicos redujeron los niveles de circRNA‑0010220 en las células madre, sus vesículas perdieron gran parte de la capacidad para estimular el crecimiento, la migración y la invasión de las células cancerosas, tanto en cultivos celulares como en modelos murinos. Esto situó a circRNA‑0010220 como un impulsor clave de los efectos perjudiciales.
Se apaga un freno epigenético
Profundizando, los investigadores trazaron cómo este ARN circular reprograma el comportamiento de las células tumorales. Dentro de las células de osteosarcoma, circRNA‑0010220 viaja al núcleo, el centro de control celular. Allí se une a una proteína llamada EZH2, una enzima que añade marcas químicas a las histonas —las proteínas semejantes a un carrete alrededor de las cuales se enrolla el ADN. Actuando conjuntamente, circRNA‑0010220 y EZH2 aumentan una marca específica denominada H3K27me3 en la región reguladora del gen CTNNBIP1. Esta modificación compacta fuertemente la cromatina en esa región, silenciando efectivamente el gen. Como CTNNBIP1 actúa normalmente como un freno sobre una potente vía promotora del crecimiento, su silenciamiento elimina una salvaguardia importante contra el comportamiento cancerígeno descontrolado.
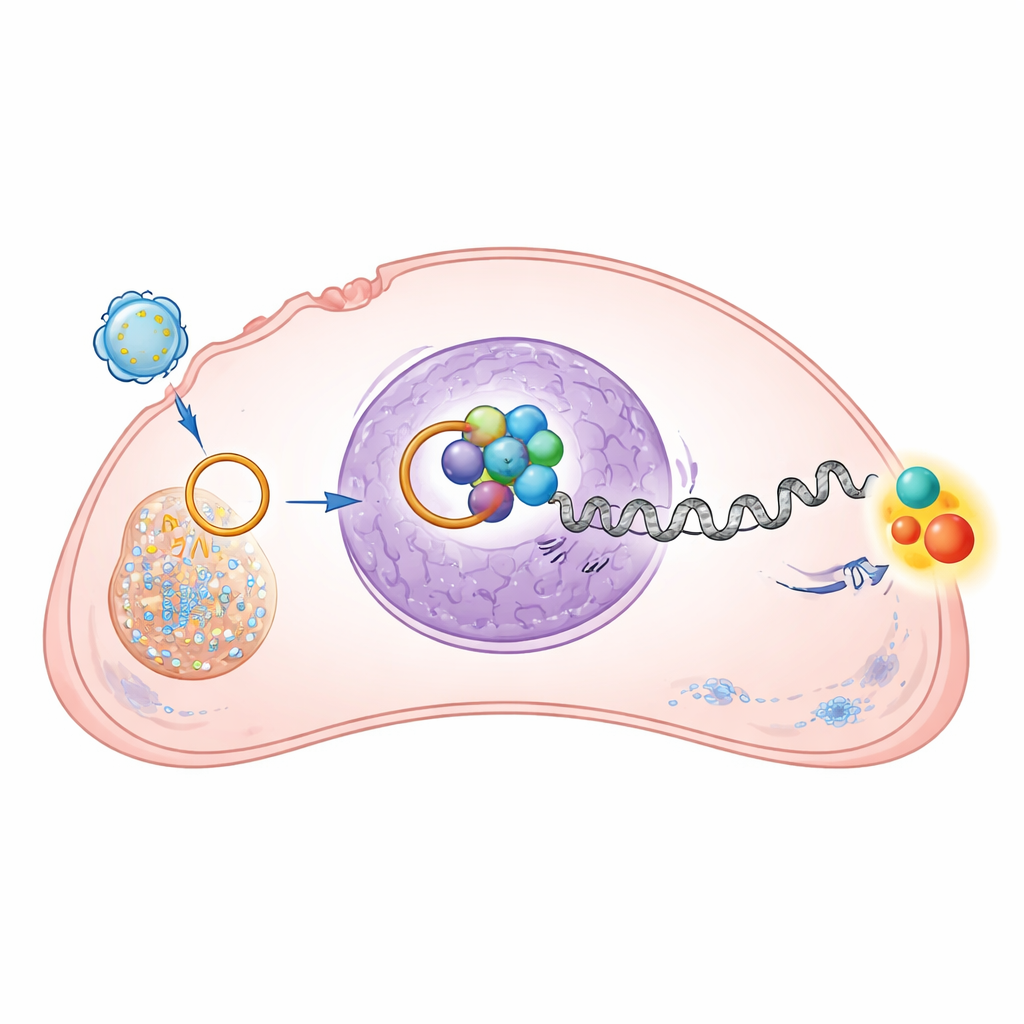
Activación de una vía de crecimiento potente
CTNNBIP1 restringe la vía Wnt/β‑catenina, un sistema de señalización bien conocido que, cuando está sobreactivado, fomenta la división, la migración y la supervivencia celular. Al apagar CTNNBIP1, circRNA‑0010220 aumenta indirectamente los niveles y la actividad nuclear de β‑catenina en las células de osteosarcoma. El estudio mostró que los genes controlados por esta vía —vinculados al progreso del ciclo celular, a rasgos semejantes a células madre y a la invasión— se activaron más cuando estaba presente circRNA‑0010220 transportado por vesículas. Cuando los investigadores emplearon un fármaco que bloquea específicamente a β‑catenina, los efectos pro‑crecimiento y pro‑migración de circRNA‑0010220 se revirtieron en gran medida. Esto confirma que el ARN circular opera a través de esta vía de crecimiento para impulsar la progresión tumoral.
Qué significa esto para tratamientos futuros
En conjunto, el trabajo describe una cadena completa de eventos: las células madre de la médula ósea envían vesículas cargadas con circRNA‑0010220 a las células de osteosarcoma; el ARN circular se asocia con EZH2 en el núcleo para silenciar químicamente a CTNNBIP1; esto libera el freno sobre la vía Wnt/β‑catenina, alimentando en último término un crecimiento y una diseminación tumoral más rápidos. Para los pacientes, esto sugiere varios enfoques nuevos para la terapia. Interrumpir la transferencia de vesículas, bloquear circRNA‑0010220, interferir en su asociación con EZH2 o atenuar la señalización de β‑catenina podrían ayudar a frenar la progresión del osteosarcoma. Aunque estas ideas deben probarse clínicamente, el estudio expone una conversación previamente oculta en el microambiente tumoral óseo y destaca un conjunto concreto de objetivos moleculares para futuros fármacos.
Cita: Pan, R., Pan, Y., Ruan, W. et al. BMSC-derived extracellular vesicles enhance osteosarcoma proliferation and metastasis via the circRNA-0010220/β-catenin pathway. Cell Death Dis 17, 376 (2026). https://doi.org/10.1038/s41419-026-08655-8
Palabras clave: osteosarcoma, vesículas extracelulares, ARN circular, Wnt beta-catenina, regulación epigenética