Clear Sky Science · es
Pérdida de DIAPH3 acelera la génesis de gliomas en ratones
Por qué importa este estudio cerebral
El glioblastoma es uno de los cánceres cerebrales más letales y, pese a la cirugía, la radioterapia y la quimioterapia, la mayoría de los pacientes sobrevive poco más de un año. Este estudio aborda una pregunta básica pero crucial: ¿qué cambios tempranos dentro de las células cerebrales las empujan a convertirse en tumores tan agresivos, y por qué son estos tumores tan difíciles de eliminar con radiación? Al seguir una sola proteína estructural en células cerebrales de ratón, los investigadores muestran cómo su pérdida desestabiliza los cromosomas, acelera la aparición de tumores y ayuda a las células con rasgos de célula madre tumoral a resistir la radiación que debería destruirlas.
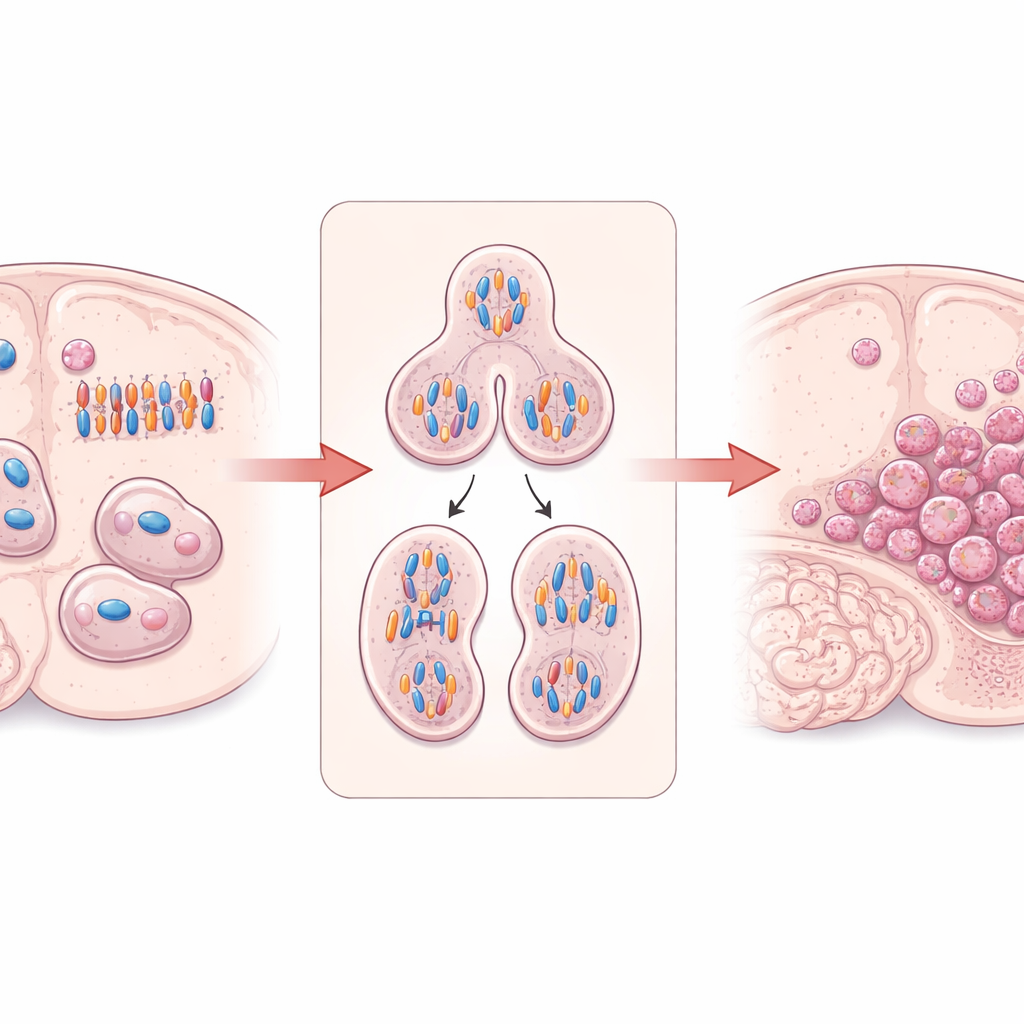
Un “constructor” celular que mantiene la división en orden
El trabajo se centra en DIAPH3, una proteína que ayuda a construir y organizar el andamiaje interno de la célula formado por filamentos de actina y microtúbulos. En las células madre cerebrales en división, DIAPH3 es vital para formar un huso correcto —la estructura que separa los cromosomas duplicados— y para dividir una célula en dos. Investigaciones anteriores demostraron que, cuando falta DIAPH3 en cerebros en desarrollo de ratón, las células en división con frecuencia manejan mal los cromosomas, lo que conduce a números cromosómicos anormales (aneuploidía), detenciones del ciclo celular y muerte celular. De forma intrigante, una pequeña región del cromosoma 13 humano que contiene el gen DIAPH3 se borra con frecuencia en glioblastoma, y niveles más altos de DIAPH3 se han relacionado con mejor supervivencia en algunos pacientes, lo que sugiere que esta proteína puede actuar como supresora tumoral en el cerebro.
Ingeniería de cerebros de ratón para desarrollar tumores
Para probar si la pérdida de DIAPH3 realmente favorece el cáncer cerebral, el equipo creó ratones en los que se podían eliminar selectivamente dos genes en las células madre que forman la corteza: Diaph3 y Trp53, este último codifica al conocido guardián del genoma, p53. Los ratones que carecían solo de Diaph3 en esta región no desarrollaron tumores ni siquiera tras dos años, lo que implica que p53 aún puede eliminar células altamente anormales. En cambio, los ratones que carecían de Trp53 solos, o de ambos Trp53 y Diaph3, acabaron formando gliomas difusos de alto grado que se parecían mucho a la enfermedad humana al observarlos al microscopio. Usando escáneres de MRI ultrarrresolución repetidos, los investigadores mostraron que los animales sin ambos genes desarrollaron tumores detectables antes y que, a mitad de vida, con más frecuencia presentaban gliomas grandes, particularmente en los bulbos olfatorios, que los ratones que solo perdieron Trp53. La tasa de crecimiento tumoral, una vez iniciada, fue similar entre los grupos: lo que cambió fue lo pronto que los tumores aparecían.
Caos cromosómico y reprogramación de la actividad génica
Para indagar por qué la pérdida de DIAPH3 acelera el inicio tumoral, el equipo examinó la actividad génica en los bulbos olfatorios de ratones jóvenes antes de que se viera ningún tumor. En animales que carecían de ambos Diaph3 y Trp53, 126 genes se expresaron a niveles diferentes en comparación con los mutantes solo en Trp53, y casi la mitad de esos genes tenía vínculos previos con el cáncer. Muchos cambios se agruparon en vías que impulsan el crecimiento celular, la migración y la formación de vasos sanguíneos, incluidas las señales VEGF, MAPK, RAS, Rap1 y cAMP, así como redes acopladas a receptores acoplados a proteínas G. Este panorama molecular alterado sugiere que las células se estaban empujando hacia un estado similar al canceroso de forma más temprana. El análisis de número de copias del genoma completo de tumores ya formados reveló que la deficiencia de DIAPH3 no aumentó notablemente los cambios focales pequeños en el ADN, sino que impulsó ganancias y pérdidas a nivel de cromosomas enteros —exactamente la aneuploidía esperada por una segregación cromosómica defectuosa.
Daño genético incorporado y células madre tumorales más resistentes
Las células tumorales aneuploides presentaban más daño interno en el ADN, detectado por niveles elevados del marcador de roturas de ADN γ‑H2AX distribuidos por los núcleos celulares. Sin embargo, estos tumores seguían creciendo, lo que implica que habían adquirido maneras de tolerar dicho estrés. Al comparar la expresión génica en tumores establecidos, los investigadores hallaron cientos de genes alterados por la pérdida de DIAPH3, incluida una llamativa amplificación y sobreproducción del receptor del factor de crecimiento FGFR2 en muchos tumores doblemente mutantes. Se sabe que FGFR2 potencia las máquinas de reparación del ADN en células de glioblastoma, y su activación se ha vinculado a resistencia a la radiación. El equipo aisló células con rasgos de células madre de glioma de tumores de ratón y probó su respuesta a una dosis clínicamente relevante de radiación ionizante. Antes del tratamiento, la frecuencia de células con rasgos de célula madre fue similar en ambos genotipos, pero tras la irradiación, los cultivos procedentes de tumores deficientes en DIAPH3 mantuvieron aproximadamente el doble de células activas con rasgos de célula madre que los procedentes de tumores solo Trp53, demostrando una mayor radioresistencia.
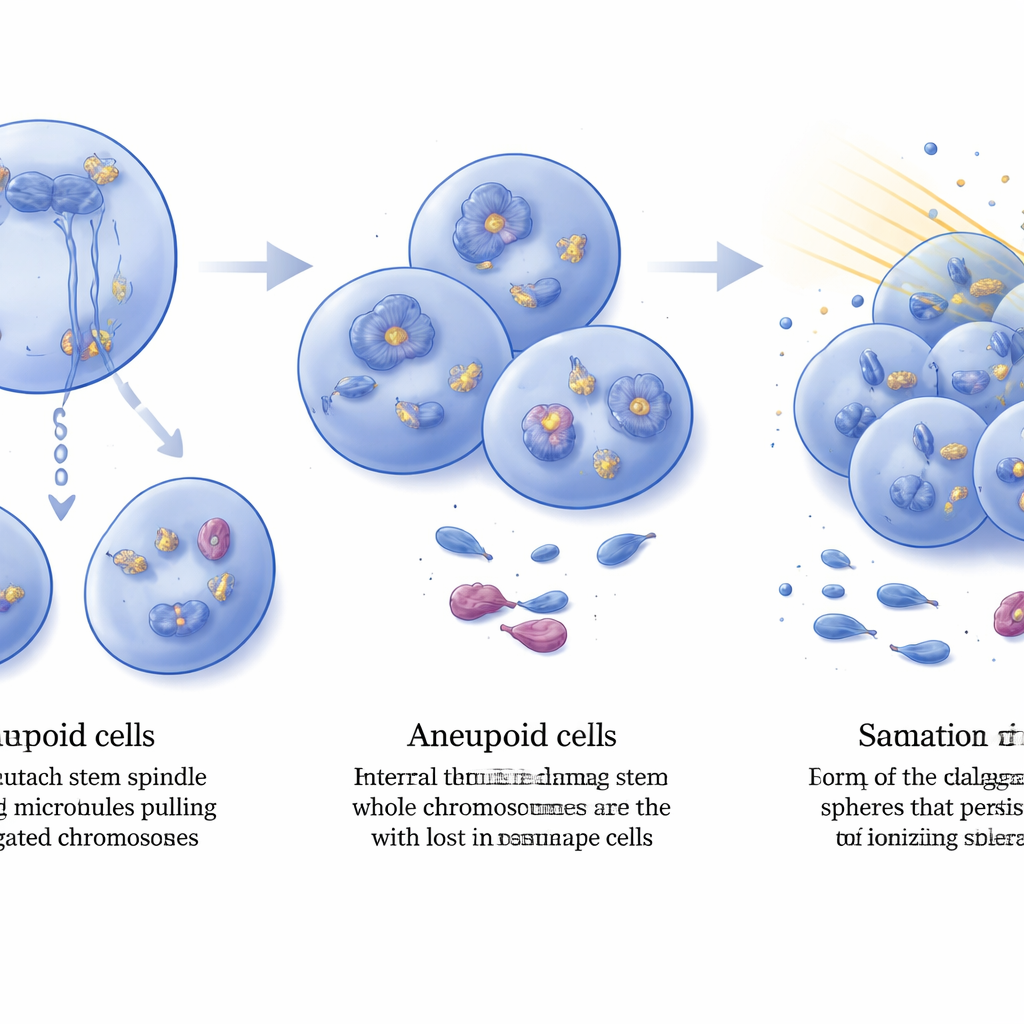
Qué significa esto para el cáncer cerebral
En conjunto, el estudio dibuja a DIAPH3 como un guardián que ayuda a las células madre cerebrales a dividirse con el número correcto de cromosomas. Cuando faltan tanto DIAPH3 como p53, la división celular se vuelve propensa a errores, se pierden o ganan cromosomas enteros y se acumula daño en el ADN. En lugar de morir, algunas células se adaptan amplificando factores vinculados a la reparación, como FGFR2, transformándose en gliomas de alto grado aneuploides cuyas células con rasgos de célula madre son inusualmente resistentes a la radiación. Aunque los modelos murinos no reproducen todas las facetas del glioblastoma humano, estos hallazgos respaldan a DIAPH3 tanto como posible biomarcador de pronóstico como punto nodal en la red de procesos que controlan la iniciación tumoral, la estabilidad del genoma y la respuesta al tratamiento, abriendo nuevas vías para terapias que algún día podrían hacer que este devastador cáncer cerebral sea más vulnerable a los tratamientos existentes.
Cita: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Palabras clave: glioblastoma, inestabilidad cromosómica, células madre de tumores cerebrales, resistencia a la radiación, genes supresores de tumores