Clear Sky Science · es
Las células de glioblastoma que evitan la muerte inducida por quimiorradioterapia exhiben un programa glicolítico bifurcado
Por qué importa este estudio sobre el cáncer cerebral
El glioblastoma es uno de los cánceres cerebrales más letales en adultos y casi siempre vuelve a aparecer tras cirugía, quimioterapia y radiación. Este estudio plantea una pregunta crucial: ¿qué tiene de especial el pequeño grupo de células tumorales que sobrevive al tratamiento y luego reaviva la enfermedad? Al rastrear cómo estas células gestionan el azúcar a lo largo del tiempo, los investigadores descubren una estrategia de supervivencia oculta que puede explicar por qué los tratamientos actuales fallan con tanta frecuencia y sugieren nuevas formas de cortar la vía de sustento del tumor.
Los supervivientes ocultos tras el tratamiento
El tratamiento estándar para el glioblastoma combina un fármaco llamado temozolomida con radiación. Aunque esta combinación mata a la mayoría de las células tumorales, una minoría persistente sobrevive y puede sembrar un nuevo tumor meses después. Para captar a estos supervivientes in fraganti, el equipo empleó células tumorales tomadas directamente de diez pacientes distintos y las expuso a un calendario de tratamiento diseñado para reproducir de cerca lo que reciben las personas en la clínica. Muestrearon células vivas en varios puntos durante y después del tratamiento, y también estudiaron tumores coincidentes cultivados en ratones, lo que les permitió seguir cómo cambian los supervivientes con el tiempo en lugar de limitarse a comparar tumores antes y después de la recaída.
Cómo cambian las células tumorales la forma en que usan el azúcar
El tejido cerebral consume una porción notable del azúcar del cuerpo, y las células de glioblastoma son especialmente voraces. Los investigadores encontraron que, a medida que progresaba el tratamiento, las células supervivientes absorbían aún más glucosa del entorno. Sin embargo, en un giro sorprendente, no quemaban este combustible extra más rápido. En su lugar, estas células redujeron su producción de lactato, el producto de desecho típico de la rápida degradación de azúcares en el cáncer. Las mediciones de proteínas clave mostraron un patrón dividido llamativo: los componentes que introducen la glucosa en la célula y comienzan a descomponerla se incrementaron, mientras que los que manejan los pasos finales y producen lactato disminuyeron. Este programa “bifurcado” significa que la glucosa entra y empieza a procesarse, pero la vía habitual de salida hacia el lactato está en parte cerrada.
Redirigir el combustible hacia materiales de construcción y centrales energéticas
¿A dónde va la glucosa desviada? Usando glucosa especialmente marcada y mediciones avanzadas de metabolitos, el equipo mostró que las células supervivientes canalizan gran parte de este carbono hacia dos destinos principales. Uno es una ruta lateral llamada vía de las pentosas fosfato, que genera las materias primas necesarias para fabricar los bloques constructores del ADN y el ARN. En estas células, muchos componentes de nucleótidos y genes relacionados estaban aumentados, lo que sugiere un fuerte empuje hacia la reconstrucción y la preparación para un crecimiento renovado. El segundo destino son las centrales energéticas de la célula, las mitocondrias. Aumentaron las enzimas del ciclo energético mitocondrial, y trabajos anteriores del mismo grupo mostraron una mayor importación de combustible derivado de la glucosa hacia estas estructuras. En conjunto, esto revela una reprogramación coordinada: menos fermentación desperdiciadora hacia el lactato y más inversión en reparación, materiales de crecimiento y producción de energía flexible.
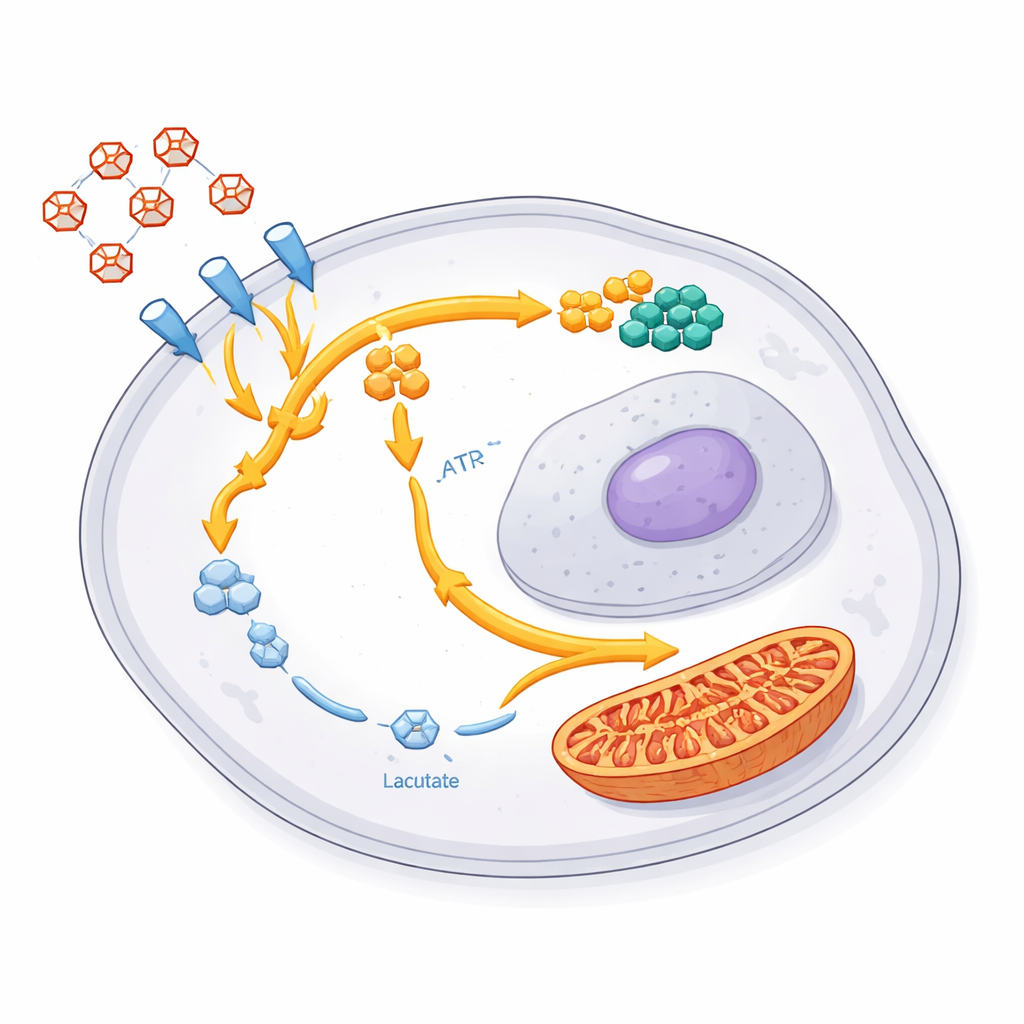
Un manual de supervivencia compartido entre tumores y en animales
Los tumores de glioblastoma difieren mucho entre pacientes, lo que a menudo frustra los tratamientos universales. A pesar de esta diversidad, cada uno de los diez modelos derivados de pacientes mostró el mismo cambio básico tras la quimiorradioterapia: aumento de los pasos tempranos de manejo de la glucosa, disminución de los pasos finales y la producción de lactato, y mayor actividad mitocondrial. Es importante que la misma firma apareció en tumores cerebrales de ratón cultivados a partir de células de pacientes y tratados con versiones adaptadas de la terapia estándar. Los tumores recurrentes en estos animales mantuvieron el programa alterado de uso de azúcar, lo que indica que no se trata de un efecto pasajero sino de un rasgo estable de las células que logran sobrevivir al tratamiento y reconstruir el cáncer.
Qué significa esto para tratamientos futuros
Para un público general, el mensaje central es que las células de glioblastoma que sobreviven no se limitan a “ocultarse” del tratamiento; reconfiguran activamente su manera de usar el azúcar para mantenerse vivas. Absorben más glucosa, evitan convertirla en desecho y la canalizan hacia la fabricación de bloques de ADN y el funcionamiento mitocondrial, lo que les ayuda a reparar daños, mantener un estado flexible similar al de células madre y, eventualmente, reconstituir el tumor. Al revelar este estado metabólico de supervivencia compartido, el estudio apunta a nuevas ideas terapéuticas: atacar los pasos tempranos del procesamiento de la glucosa, la ruta lateral de construcción de ADN o la dependencia mitocondrial de estas células podría hacer que la quimiorradioterapia estándar sea más completa y deje menos escapatorias capaces de reiniciar la enfermedad.
Cita: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Palabras clave: glioblastoma, metabolismo del cáncer, utilización de la glucosa, resistencia a la terapia, vía de las pentosas fosfato