Clear Sky Science · es
El eje DAG/PKC/CREB1/TGF-β1 impulsa la rigidez en elastografía por ondas de corte y la progresión maligna en cáncer de mama triple negativo mediante la reprogramación del metabolismo lipídico
Por qué importa la rigidez tumoral
Los médicos llevan tiempo observando que algunos tumores mamarios se sienten más duros que otros y que esa rigidez suele señalar un cáncer más peligroso. En el cáncer de mama triple negativo, una forma agresiva que carece de dianas farmacológicas habituales, la obesidad parece endurecer los tumores y aumentar su probabilidad de diseminarse. Este estudio explica cómo los cambios en el metabolismo de las grasas en pacientes obesas endurecen los tumores y demuestra que una técnica especializada de ultrasonido, la elastografía por ondas de corte, puede medir esa rigidez desde el exterior como una ventana al comportamiento tumoral.
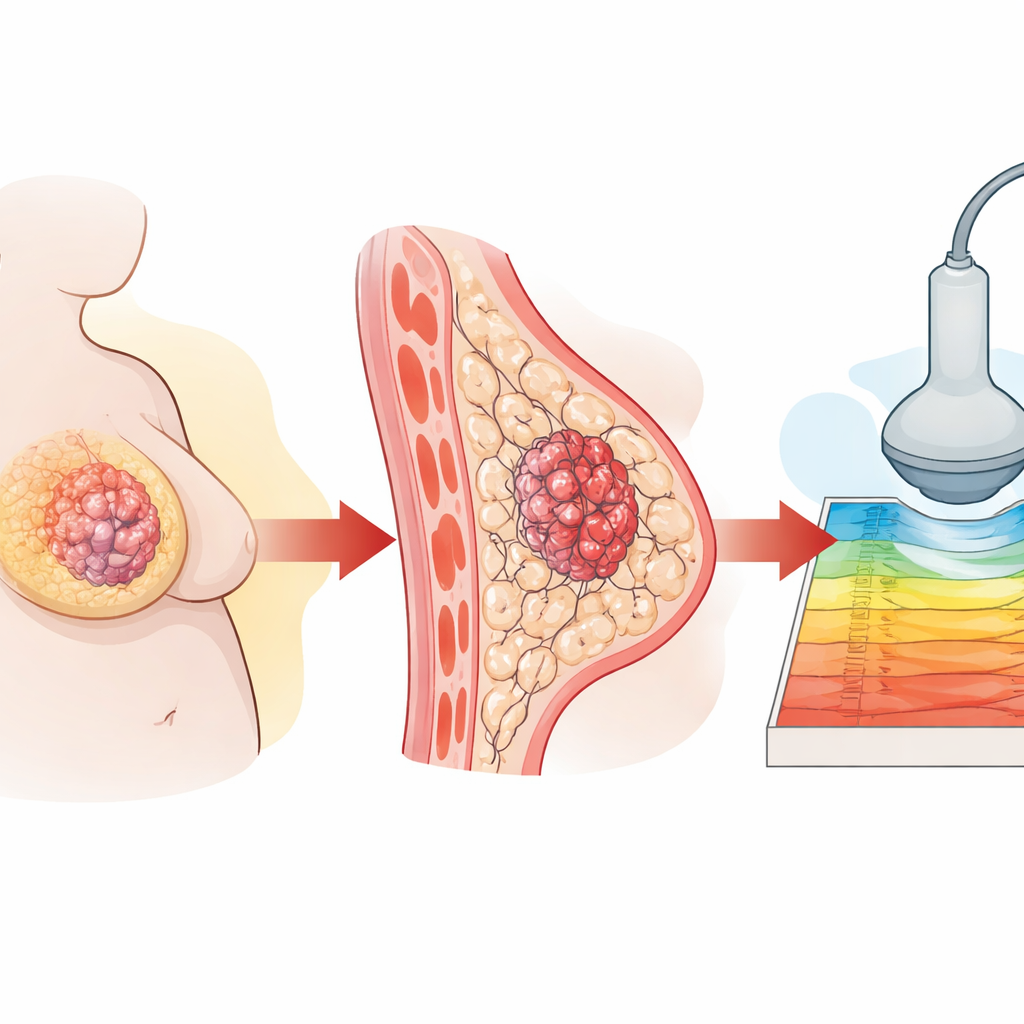
Peso corporal y riesgo tumoral
Los investigadores empezaron siguiendo a 147 mujeres con cáncer de mama triple negativo en un centro oncológico importante de Shanghái. Encontraron que las mujeres con mayor índice de masa corporal (IMC) tenían peores resultados a largo plazo, incluyendo más recidivas y muertes. Al examinar las ecografías, observaron que los tumores en pacientes con mayor peso eran consistentemente más rígidos en la elastografía por ondas de corte, aunque las imágenes ecográficas en escala de grises estándar parecían similares. Las muestras de tejido confirmaron que los tumores de pacientes con mayor peso contenían más colágeno y más células en división activa, ambos signos de un entorno más hostil.
De la dieta a tumores más rígidos
Para investigar causalidad, el equipo recurrió a modelos murinos, alimentando a algunos ratones con una dieta alta en grasas y a otros con una dieta normal antes de implantarles tumores triple negativos. Los ratones con dieta alta en grasas aumentaron más de peso, desarrollaron tumores más grandes y, crucialmente, mostraron un aumento sostenido de la rigidez en la elastografía por ondas de corte con el tiempo. El examen microscópico reveló redes de colágeno más densas, más fibroblastos activados (células de soporte) y niveles más altos de una enzima que entrecruza el colágeno, todo lo cual endurece el tejido. Al mismo tiempo, las células tumorales de los ratones obesos mostraron signos de un metabolismo lipídico acelerado y acumularon más gotas lipídicas en su interior.
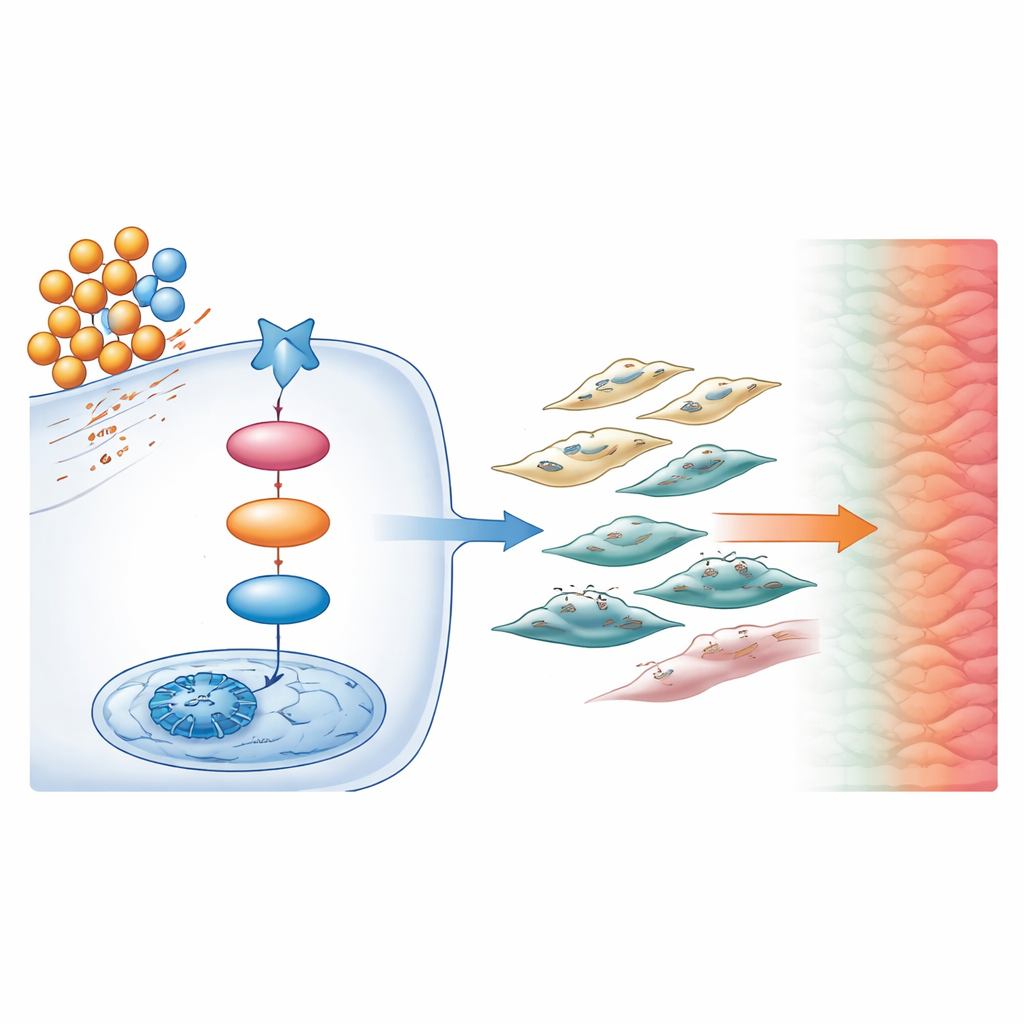
Una reacción química encadenada y oculta
Indagando más a fondo, los científicos utilizaron perfiles lipídicos y análisis de expresión génica para trazar la cadena molecular que impulsa estos cambios. Encontraron que una molécula derivada de grasas llamada diacilglicerol (DAG) estaba elevada en tumores de ratones obesos. El DAG actuó como un interruptor bioquímico, activando una proteína llamada PKC dentro de las células cancerosas. PKC a su vez aumentó la actividad de una proteína reguladora maestra, CREB1, en el núcleo celular. Una vez activada, CREB1 impulsó la producción de TGF-β1, una potente molécula de señalización conocida por promover la cicatrización y la diseminación tumoral. Juntos, esta secuencia DAG → PKC → CREB1 → TGF-β1 formaron una vía central que conecta el exceso de grasa con un tumor más rígido e invasivo.
Una conversación viciosa entre células
TGF-β1 no actuó solo sobre las células cancerosas. También activó a los fibroblastos cercanos, las células estructurales que construyen y remodelan el armazón tisular alrededor de los tumores. Al exponerse a señales procedentes de células cancerosas estimuladas por DAG, los fibroblastos pasaron a un estado altamente activo, depositando colágeno adicional y tensando aún más el entorno tumoral. Estos fibroblastos activados, a su vez, enviaron señales de vuelta a las células cancerosas que incrementaron su metabolismo lipídico, su crecimiento y su capacidad invasiva. En los modelos murinos, esta interacción bidireccional creó un circuito autorreforzante que hizo que los tumores fueran más rígidos en la elastografía por ondas de corte, más fibróticos al microscopio y más propensos a formar metástasis distantes.
Convertir imágenes en pistas para el tratamiento
Combinando datos de pacientes, experimentos en animales y estudios moleculares detallados, los autores muestran que la rigidez medida por elastografía por ondas de corte es más que una curiosidad estructural: refleja la activación de un bucle de señalización impulsado por lípidos que empeora el cáncer de mama triple negativo. Para el público general, esto significa que una medición ecográfica no invasiva de cuán duro se siente un tumor puede revelar cuánto está activado este camino perjudicial. En el futuro, los pacientes con IMC alto y tumores muy rígidos en elastografía podrían identificarse como de alto riesgo y considerarse para fármacos que bloqueen PKC, CREB1, TGF-β1 u otros pasos relacionados del circuito, convirtiendo una lectura de imagen simple en una guía para tratamientos más precisos y basados en la biología.
Cita: Wang, S., Zheng, D., Wang, Z. et al. The DAG/PKC/CREB1/TGF-β1 axis drives shear-wave elastography stiffness and malignant progression in triple-negative breast cancer via lipid metabolic reprogramming. Cell Death Dis 17, 327 (2026). https://doi.org/10.1038/s41419-026-08625-0
Palabras clave: cáncer de mama triple negativo, rigidez tumoral, obesidad, metabolismo de lípidos, elastografía por ondas de corte