Clear Sky Science · es
Orquestación metabólica impulsada por GGCT: desviar glutamina hacia la biosíntesis de glutatión mientras se potencia la anaplerosis de la glucosa para la proliferación tumoral
Por qué esto importa para el tratamiento del cáncer
Las células cancerosas crecen rápidamente y, para hacerlo, consumen grandes cantidades de combustible y deben protegerse constantemente de los subproductos tóxicos de su propio metabolismo. Este estudio revela cómo una enzima poco conocida, GGCT, ayuda a los tumores hepáticos y prostáticos a redirigir de forma inteligente dos nutrientes comunes —glutamina y glucosa— de modo que puedan tanto impulsar el crecimiento como mantener bajo control a las moléculas dañinas llamadas especies reactivas de oxígeno. Comprender este malabarismo metabólico podría abrir vías para privar de nutrientes a los tumores o colapsar sus defensas.
Cómo las células tumorales equilibran combustible y protección
Las células tumorales dependen en gran medida de la glutamina, un aminoácido que cumple una doble función: puede descomponerse para alimentar el ciclo principal productivo de energía de la célula y también aporta bloques de construcción para el glutatión, un antioxidante potente que neutraliza las especies reactivas de oxígeno. Los autores confirmaron primero que los niveles de glutamina son más altos en tumores hepáticos que en el tejido sano circundante, y que las células cancerosas cultivadas con más glutamina se dividen más rápido tanto en placas como en ratones. Cuando la glutamina escasea, las células se ralentizan, caen proteínas clave del ciclo celular y los tumores en animales disminuyen de tamaño —en parte porque las defensas antioxidantes se debilitan y se acumulan especies reactivas de oxígeno.
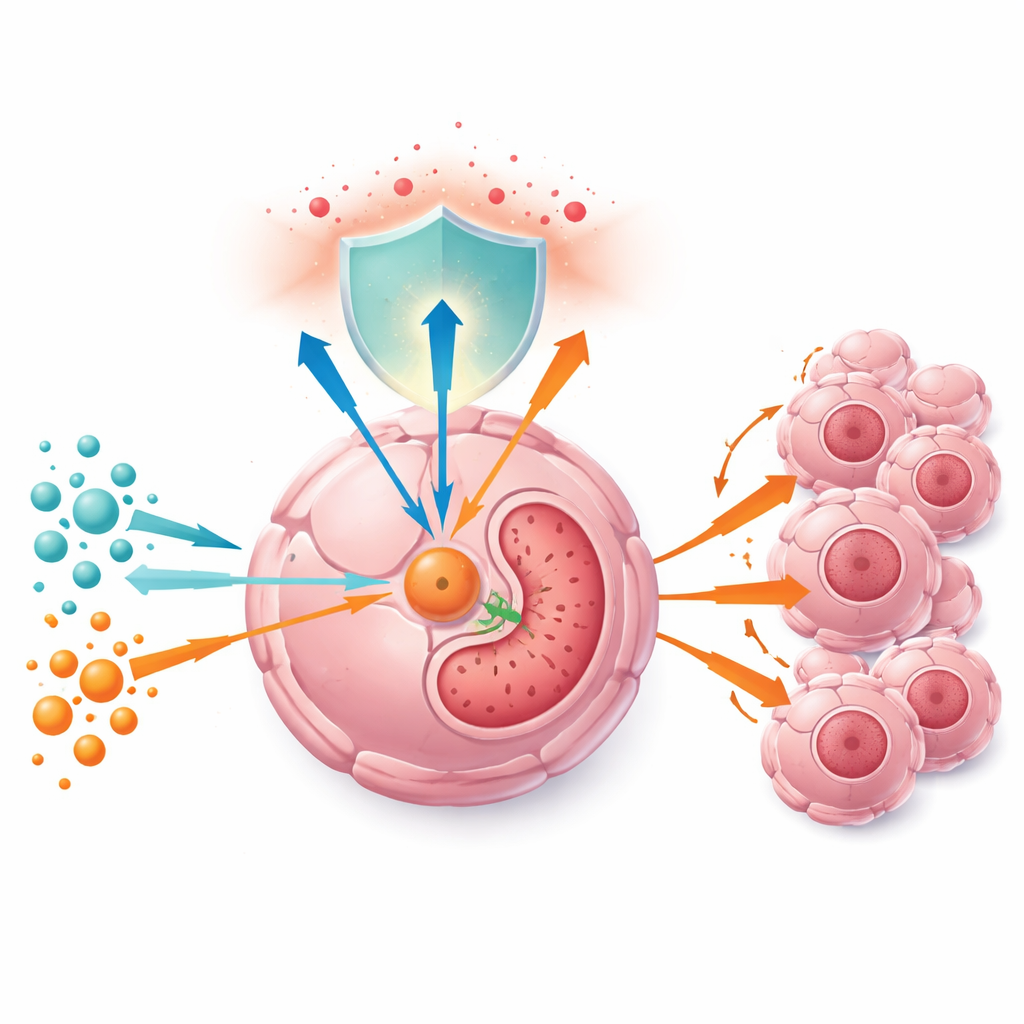
Un interruptor metabólico a la vista de todos
Al analizar muestras de pacientes y grandes bases de datos de cáncer, el equipo halló que la enzima GGCT es consistentemente más abundante en tumores de hígado y próstata que en tejidos normales, y que niveles elevados de GGCT predicen peores resultados. En muestras tumorales y en células en cultivo, los niveles de GGCT aumentan en paralelo con la concentración de glutamina, lo que sugiere que los tumores “detectan” la disponibilidad de glutamina a través de esta proteína. Los investigadores desentrañaron una cadena de control: la glutamina mantiene activa al factor pro‑crecimiento c‑Myc, que suprime un pequeño ARN regulador llamado miR‑29b‑3p; cuando miR‑29b‑3p es bajo, GGCT se libera de su freno y se acumula. Ante la escasez de glutamina, esta cadena se invierte, miR‑29b‑3p aumenta, los mensajes de GGCT se degradan más rápido y el nivel enzimático cae.
Redirigir la glutamina y captar más glucosa
Para ver qué hace GGCT dentro de la célula, los autores redujeron o aumentaron sus niveles y midieron tanto el comportamiento celular como cientos de metabolitos. Silenciar GGCT detuvo a las células en el ciclo de división, redujo sus colonias y bajó drásticamente el glutatión mientras elevaba las especies reactivas de oxígeno; añadir un antioxidante químico rescató el crecimiento en parte. Al microscopio, las mitocondrias se volvieron anormalmente elongadas y menos eficientes en el consumo de oxígeno, aun cuando las células intentaron compensar aumentando la glicólisis, el primer paso de la degradación de la glucosa. El perfil metabólico detallado mostró que los intermedios del ciclo energético central caían cuando GGCT se perdía y aumentaban cuando se sobreexpresaba.
Rastreando el destino de los átomos de carbono
El equipo siguió después átomos marcados de glutamina y glucosa mientras fluían por el metabolismo tumoral. Cuando GGCT se sobreexpresó, menos glutamina marcada terminaba en el ciclo energético y más se canalizaba hacia la síntesis de nuevo glutatión, apoyando las defensas antioxidantes. Al mismo tiempo, la glucosa marcada contribuía con mayor fuerza al ciclo, compensando la glutamina desviada. Una forma mutante de GGCT carente de la actividad enzimática normal no pudo provocar estos cambios ni promover la proliferación, lo que demuestra que la función catalítica de GGCT es crucial. Importante: suministrar piruvato extra o alterar la entrada al ciclo energético restauró los niveles de energía celular pero no redujo las especies reactivas de oxígeno, lo que indica que GGCT controla principalmente el balance redox a través del glutatión, no por simples cambios en el suministro de energía.
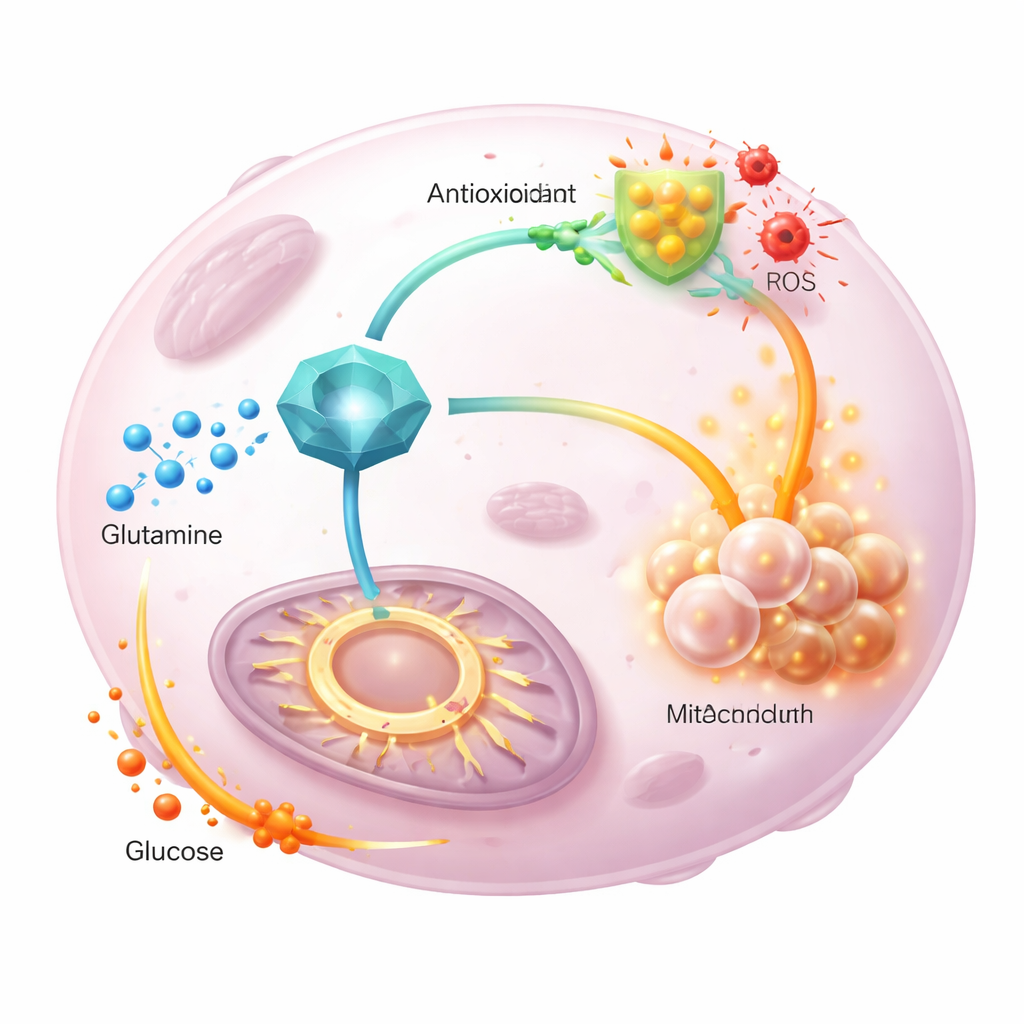
Qué significa esto para terapias futuras
En conjunto, los hallazgos sitúan a GGCT como un coordinador central que permite a los tumores dividir las funciones de la glutamina: dirige más de este nutriente hacia la producción de antioxidantes mientras atrae la glucosa al ciclo energético para mantener la división celular. En modelos animales, reducir GGCT frenó el crecimiento tumoral, redujo el glutatión y aumentó el estrés oxidativo, y estos efectos pudieron revertirse parcialmente con un fármaco antioxidante. Para un observador no especialista, el mensaje es que algunos cánceres sobreviven usando a GGCT como una centralita metabólica; fármacos que desactiven este conmutador podrían debilitar a la vez las defensas tumorales frente al daño oxidativo y perturbar su uso flexible de nutrientes, haciendo los tratamientos estándar más eficaces.
Cita: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Palabras clave: metabolismo del cáncer, glutamina, glutatión, estrés oxidativo, enzima GGCT