Clear Sky Science · es
AATF favorece la proliferación de células de glioblastoma al mantener la respiración mitocondrial mediante un mecanismo dependiente de NRF-1
Por qué importa el uso de energía en los tumores cerebrales
El glioblastoma es la forma más agresiva de cáncer cerebral en adultos y, pese a cirugía, radioterapia y quimioterapia, la mayoría de los pacientes sobrevive poco más de un año. Este estudio plantea una pregunta aparentemente simple con implicaciones de gran alcance: ¿cómo alimentan las células de glioblastoma su crecimiento implacable y puede cortarse esa línea de suministro? Los autores se centran en una proteína reguladora poco conocida llamada AATF y muestran que ayuda a las células tumorales a mantener sus fábricas de energía —las mitocondrias— funcionando a pleno rendimiento. Comprender este sistema de apoyo oculto puede abrir nuevas vías para frenar o detener estos tumores letales.
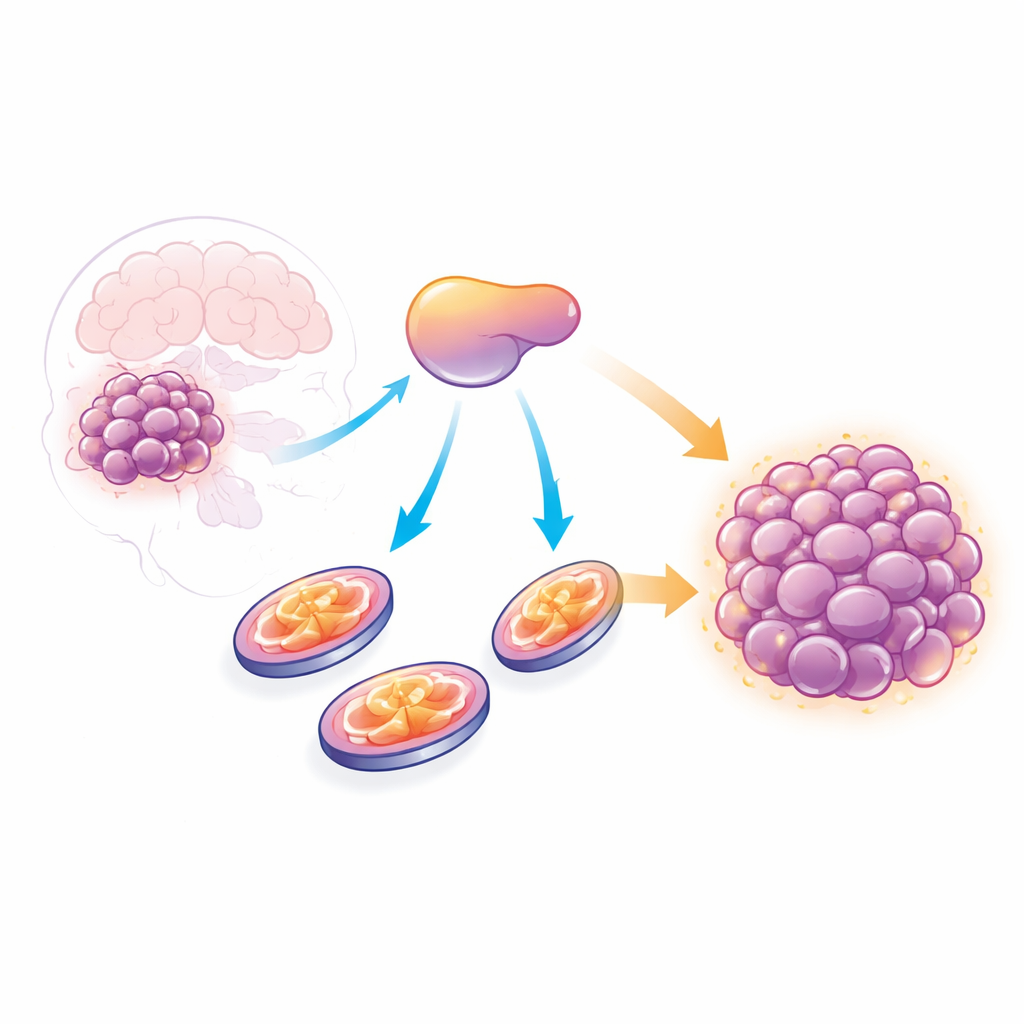
Un ayudante oculto en el crecimiento tumoral
Las células cancerosas a menudo dependen de una estrategia de quema de azúcar llamada glicólisis, durante mucho tiempo considerada su vía energética característica. Sin embargo, trabajos recientes han revelado que muchos tumores, incluido el glioblastoma, también dependen en gran medida de las mitocondrias, que producen energía mediante fosforilación oxidativa (OXPHOS). Al analizar grandes conjuntos de datos de pacientes, los investigadores hallaron que los niveles de AATF son más altos en tejido de glioblastoma que en cerebro normal y aumentan con el grado tumoral. Los pacientes cuyos tumores expresaban más AATF tendían a tener una supervivencia peor, lo que sugiere que esta proteína se asocia a una enfermedad más agresiva.
Apagar AATF ralentiza las células cancerosas
Para comprobar si AATF es solo un marcador o un impulsor activo del crecimiento, el equipo redujo sus niveles en varias líneas celulares de glioblastoma usando herramientas basadas en ARN y la interferencia CRISPR. Las células carentes de AATF se multiplicaron mucho más despacio, se acumularon en la fase de reposo del ciclo celular y formaron muchas menos colonias a largo plazo. De manera importante, esta desaceleración ocurrió sin desencadenar una muerte celular masiva ni senescencia, lo que significa que las células estaban vivas pero estancadas. Cuando las células con depleción de AATF se implantaron en ratones, los tumores resultantes fueron mucho más pequeños y mostraron menos células en división, confirmando que AATF es necesario para un crecimiento tumoral robusto en tejido vivo.
Reconfigurando la red energética tumoral
Como se sabe que AATF influye en la actividad génica, los autores examinaron cómo su pérdida remodela el programa genético de la célula. El secuenciamiento de ARN reveló que cientos de genes cambiaron su actividad cuando AATF fue silenciado. Entre los más consistentemente reducidos figuraron genes que codifican componentes clave de la maquinaria mitocondrial de OXPHOS. Las mediciones de proteínas confirmaron que múltiples partes de los complejos productores de energía en las mitocondrias estaban disminuidas. Cuando los investigadores midieron directamente el consumo de oxígeno y la producción de energía, las células sin AATF mostraron una respiración más baja y niveles reducidos de ATP. Al mismo tiempo, sus mitocondrias produjeron más especies reactivas de oxígeno, adoptaron una morfología fragmentada y en forma de anillo asociada a disfunción, y aumentaron la expresión de genes que promueven la fisión mitocondrial, todos indicios de una red energética estresada y comprometida.
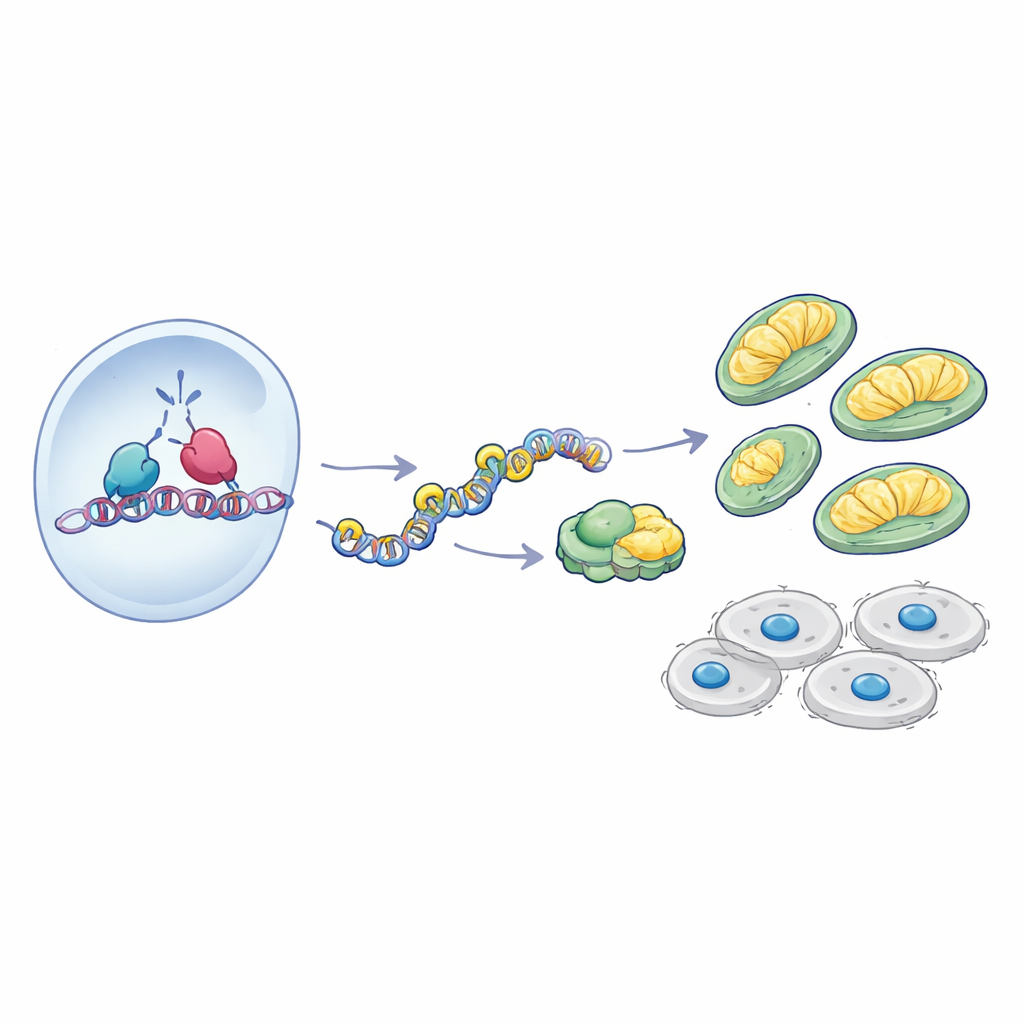
Una asociación a nivel del ADN
¿Cómo ejerce AATF tal control sobre los genes mitocondriales? El estudio se centró en NRF-1, un factor de transcripción ya conocido como regulador maestro de la biogénesis mitocondrial y de la OXPHOS. Los datos de pacientes mostraron que los niveles de AATF y NRF-1 suben y bajan a la par en glioblastoma, y los experimentos en líneas celulares revelaron que ambas proteínas interactúan físicamente. Mediante inmunoprecipitación de cromatina, los autores demostraron que AATF está presente en las regiones promotoras de varios genes de OXPHOS exactamente donde NRF-1 se une. Cuando NRF-1 fue reducido, la unión de AATF a esos promotores cayó bruscamente, indicando que NRF-1 ayuda a reclutar AATF al ADN. Además, en células sin AATF, NRF-1 aún podía unirse al ADN, pero el reclutamiento de la enzima transcripcional ARN polimerasa II se vio perjudicado y la cromatina circundante se volvió más compacta, con menos marcas de histonas activadoras y más marcas represivas. En esencia, sin AATF, NRF-1 se sienta sobre los interruptores, pero las luces no se encienden.
Qué significa esto para tratamientos futuros
Para un público no especialista, la conclusión es que las células de glioblastoma usan una asociación especializada entre AATF y NRF-1 para mantener sus motores mitocondriales funcionando a altas revoluciones, suministrando la energía necesaria para la división rápida y la resistencia al tratamiento. AATF actúa como copiloto en los genes mitocondriales, moldeando el entorno local del ADN para que NRF-1 pueda impulsar una fuerte expresión de los componentes de OXPHOS. Eliminar AATF detiene este sistema: las mitocondrias flaquean, se acumulan subproductos dañinos y las células tumorales pierden su ventaja proliferativa tanto en cultivos como en ratones. Aunque actualmente no existen fármacos que bloqueen directamente AATF, este trabajo lo identifica como un objetivo prometedor en glioblastoma y sugiere que interrumpir el eje AATF–NRF-1–mitocondrias podría debilitar el suministro energético del tumor y mejorar la eficacia de las terapias existentes.
Cita: Sorino, C., Di Giovenale, S., Falcone, I. et al. AATF supports proliferation of glioblastoma cells by sustaining mitochondrial respiration through an NRF-1-dependent mechanism. Cell Death Dis 17, 349 (2026). https://doi.org/10.1038/s41419-026-08617-0
Palabras clave: glioblastoma, respiración mitocondrial, fosforilación oxidativa, regulación transcripcional, metabolismo del cáncer