Clear Sky Science · es
La transdiferenciación adipogénica reprográmala células de PDAC con alta EMT hacia un estado post-mitótico similar a adipocitos y limita la metástasis
Convertir células cancerosas agresivas en grasa inofensiva
El cáncer de páncreas es uno de los más letales, en buena parte porque se disemina temprano y resiste los tratamientos estándar. Este estudio explora una idea sorprendentemente distinta: en lugar de intentar envenenar o privar de nutrientes a las células tumorales, ¿y si pudiéramos inducir a las células de cáncer de páncreas más peligrosas a transformarse en células parecidas a la grasa que ya no se dividen ni viajan por el organismo? El trabajo describe cómo los investigadores empujaron a células pancreáticas altamente agresivas hacia un estado estable similar al de los adipocitos que ralentizó el crecimiento tumoral y redujo la diseminación en ratones, apuntando a una nueva forma de controlar esta enfermedad devastadora.
Por qué el cáncer de páncreas es tan difícil de frenar
El adenocarcinoma ductal pancreático, la forma principal de cáncer de páncreas, tiene un pronóstico muy pobre: solo alrededor de uno de cada ocho pacientes vive cinco años tras el diagnóstico. Parte del problema es que muchas células tumorales en este cáncer se encuentran en un estado cambiante llamado EMT, que las hace más móviles, invasivas y resistentes a fármacos. Los intentos de bloquear las múltiples señales que impulsan este estado han dado beneficios limitados. Al mismo tiempo, el páncreas y sus tumores muestran una sorprendente tendencia a acumular células grasas, lo que plantea la pregunta de si esta flexibilidad oculta en la identidad celular podría aprovecharse. Los autores razonaron que si las células de cáncer pancreático con alta carga de EMT ya están predispuestas a cambiar, quizá puedan redirigirse hacia una identidad tranquila, similar a la grasa, en vez de una invasiva.
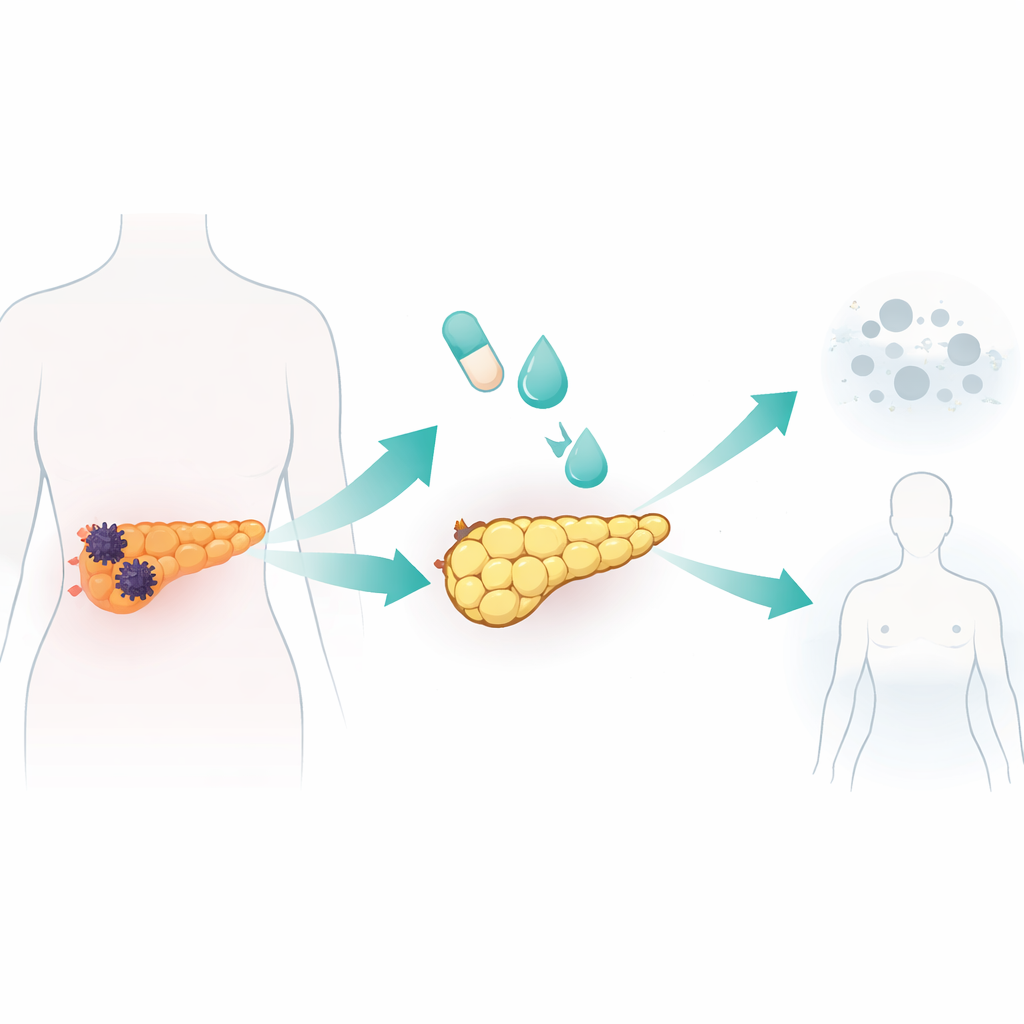
Reprogramar células cancerosas en el laboratorio hacia células similares a adipocitos
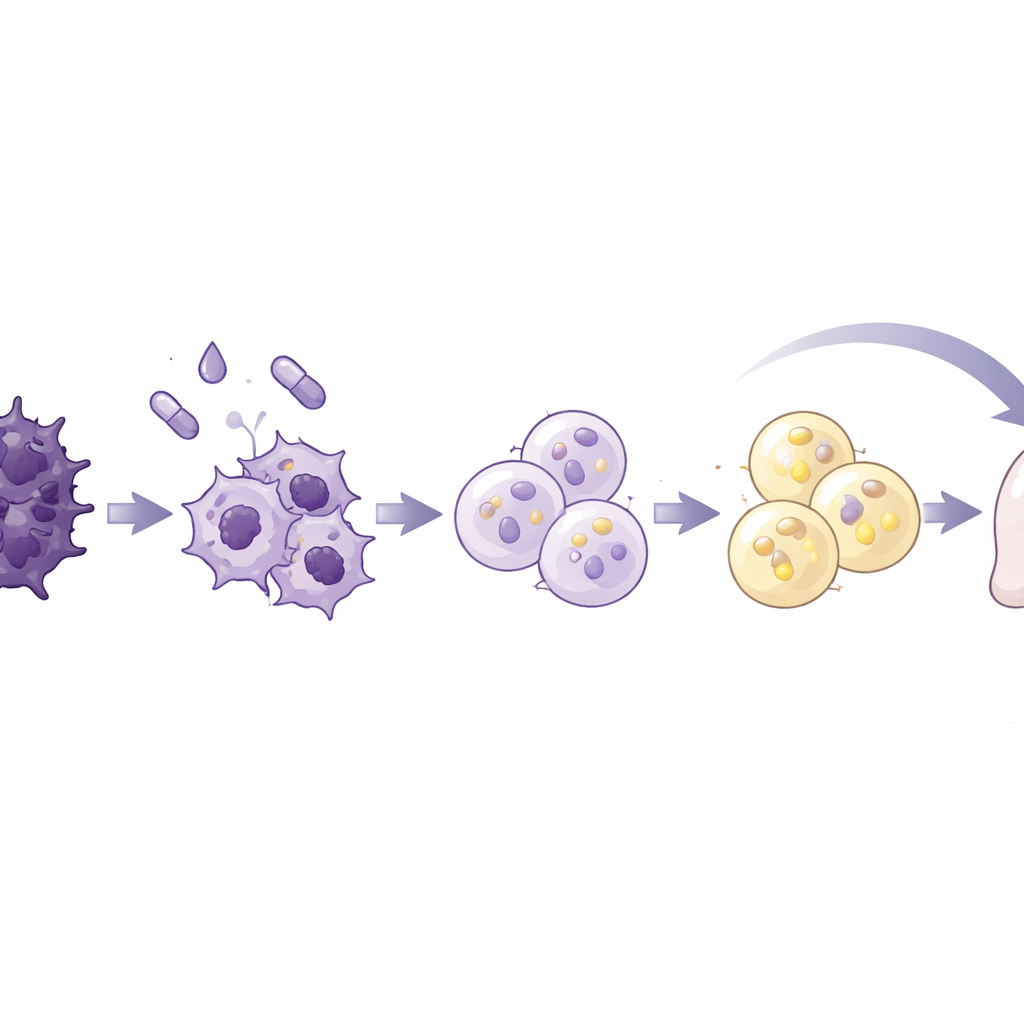
El equipo probó un cóctel estándar de diferenciación a adipocitos, usado en estudios previos de biología de la grasa y cáncer de mama, en siete líneas celulares humanas de cáncer de páncreas y en una línea celular pancreática normal. La mezcla combinaba insulina y un esteroide con rosiglitazona, un fármaco que activa un regulador maestro de la adipogénesis, además de una proteína señal BMP2 para desbloquear la plasticidad celular. Una línea cancerosa, llamada AsPC-1, fue especialmente receptiva. En diez días, estas células se hicieron más grandes y redondeadas y se llenaron de gotas lipídicas, rasgos característicos de los adipocitos. Activaron genes y proteínas típicas de adipocitos maduros y mostraron metabolismo lipídico robusto, incluyendo secreción de adiponectina y movilización de reservas grasas bajo estímulo. Crucialmente, estas células convertidas dejaron de proliferar, se detuvieron en fases tempranas del ciclo celular, y migraron e invadieron mucho menos que las células cancerosas no tratadas.
Apagar el programa canceroso en lo profundo de la célula
Para ver qué ocurría a nivel molecular, los investigadores analizaron el empaquetamiento del ADN y la actividad génica en las células convertidas. Encontraron un endurecimiento amplio de la cromatina, el complejo ADN-proteína que controla el acceso a los genes, junto con una caída global de la expresión génica, ambas características de células no proliferativas. Los genes que apoyan la EMT, la invasión y la metástasis, incluidos enzimas que degradan la matriz y reguladores clave de la EMT, quedaron fuertemente reprimidos, mientras que los genes relacionados con la grasa se vieron reforzados. La firma génica general cambió de una identidad mesenquimal y altamente móvil a otra que se parecía mucho a adipocitos maduros. Las señales vinculadas al crecimiento celular y a la respuesta a un motor principal de la EMT, TGF-beta, se atenuaron, mientras que las rutas relacionadas con el manejo de lípidos y la adhesión celular se realzaron. Estos cambios sugieren que las células no solo se frenaron, sino que fueron fundamentalmente reasignadas.
Probar la estrategia en ratones
Los científicos preguntaron a continuación si esta conversión forzada a un estado similar al adipocito podría ayudar a controlar tumores en animales vivos. Implantaron células humanas de cáncer de páncreas en el páncreas o en el bazo de ratones para modelar tumores primarios y metástasis hepáticas. Los ratones tratados con rosiglitazona y BMP2 desarrollaron tumores pancreáticos más pequeños y mostraron gotas lipídicas más abundantes y marcadores de adipocitos dentro de los tumores, junto con niveles más bajos de genes de EMT e invasión. En el modelo de metástasis, el tratamiento no cambió la siembra tumoral temprana, pero con el tiempo ralentizó la expansión de la carga tumoral hepática en comparación con los animales no tratados. Importante, el tejido pancreático normal vecino no mostró una conversión obvia a adipocitos, y el estado similar a la grasa en los tumores persistió al menos un mes tras la interrupción de los fármacos, lo que sugiere cierto grado de durabilidad y especificidad.
Qué podría significar esto para la atención del cáncer en el futuro
Este estudio respalda un concepto provocador: para los cánceres pancreáticos altamente plásticos y ricos en EMT, podría ser posible "convertir en lugar de matar", redirigiendo las células tumorales peligrosas y errantes hacia células estables, no divisorias y similares a adipocitos que tienen menos capacidad de diseminarse. Aunque este es un trabajo en fase temprana en células y modelos murinos, y no todos los cánceres de páncreas responden por igual, abre una nueva vía terapéutica que actúa cambiando la identidad celular en lugar de limitarse a bloquear señales de crecimiento. En el futuro, tales enfoques de transdiferenciación podrían combinarse con fármacos dirigidos o inmunoterapias para mantener el cáncer de páncreas en un estado más tranquilo y manejable y reducir el riesgo de metástasis letal.
Cita: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Palabras clave: cáncer de páncreas, plasticidad celular, transdiferenciación, transición epitelio-mesénquima, células similares a adipocitos