Clear Sky Science · es
La separación en fases de CBX2 contribuye a la reparación por recombinación homóloga y a la resistencia a fármacos en el cáncer de ovario
Por qué importa esta investigación
El cáncer de ovario es uno de los tumores más letales en mujeres, en gran parte porque muchos tumores dejan de responder a la quimioterapia. Este estudio revela un truco de supervivencia oculto utilizado por los carcinomas serosos de alto grado: forman pequeñas gotitas de aspecto líquido dentro del núcleo celular que potencian la reparación del ADN, ayudando a las células tumorales a resistir el daño causado por los fármacos estándar. El trabajo también señala una pastilla ya existente, Ibrutinib, como posible forma de explotar esta vulnerabilidad en pacientes cuyos tumores dependen de este sistema de reparación basado en condensados.
Células tumorales que reparan demasiado bien su ADN
La mayoría de los fármacos anticancerosos más potentes actúan dañando el ADN hasta un punto en que las células tumorales no pueden dividirse. En el carcinoma seroso de alto grado, sin embargo, muchos tumores se vuelven expertos en parchear ese daño, lo que conduce a resistencia frente a quimioterapia con platino e inhibidores de PARP. Los autores se centraron en una proteína llamada CBX2, que lee marcas químicas en la compactación del ADN y se encuentra en niveles más altos en tumores ováricos que en tejido normal. En conjuntos de datos de pacientes y muestras de tejido, los tumores con más CBX2 tenían más probabilidades de resistir el tratamiento con platino y de recidivar antes, especialmente en este subtipo agresivo de cáncer de ovario.
Gotas en el núcleo: un "banco de trabajo" que potencia la reparación
CBX2 tiene la habilidad inusual de formar agrupamientos densos con aspecto de gotas dentro del núcleo celular, un proceso conocido como separación en fases. Estas gotas se comportan como pequeños bancos de trabajo líquidos que pueden concentrar proteínas específicas. Al comparar células cancerosas con CBX2 normal, sin CBX2 o con una forma mutante que no puede formar gotas, los investigadores demostraron que los condensados de CBX2 son centrales para la forma en que las células tumorales reparan el ADN roto. Cuando se eliminó CBX2, los cromosomas se rompían con más frecuencia, se acumulaban señales de daño en el ADN y se debilitaron ambas principales vías de reparación de roturas de doble cadena. Restaurar CBX2 normal recuperó estas capacidades de reparación, pero una versión defectuosa en la formación de gotas no lo hizo, a pesar de que aún podía unirse al ADN. 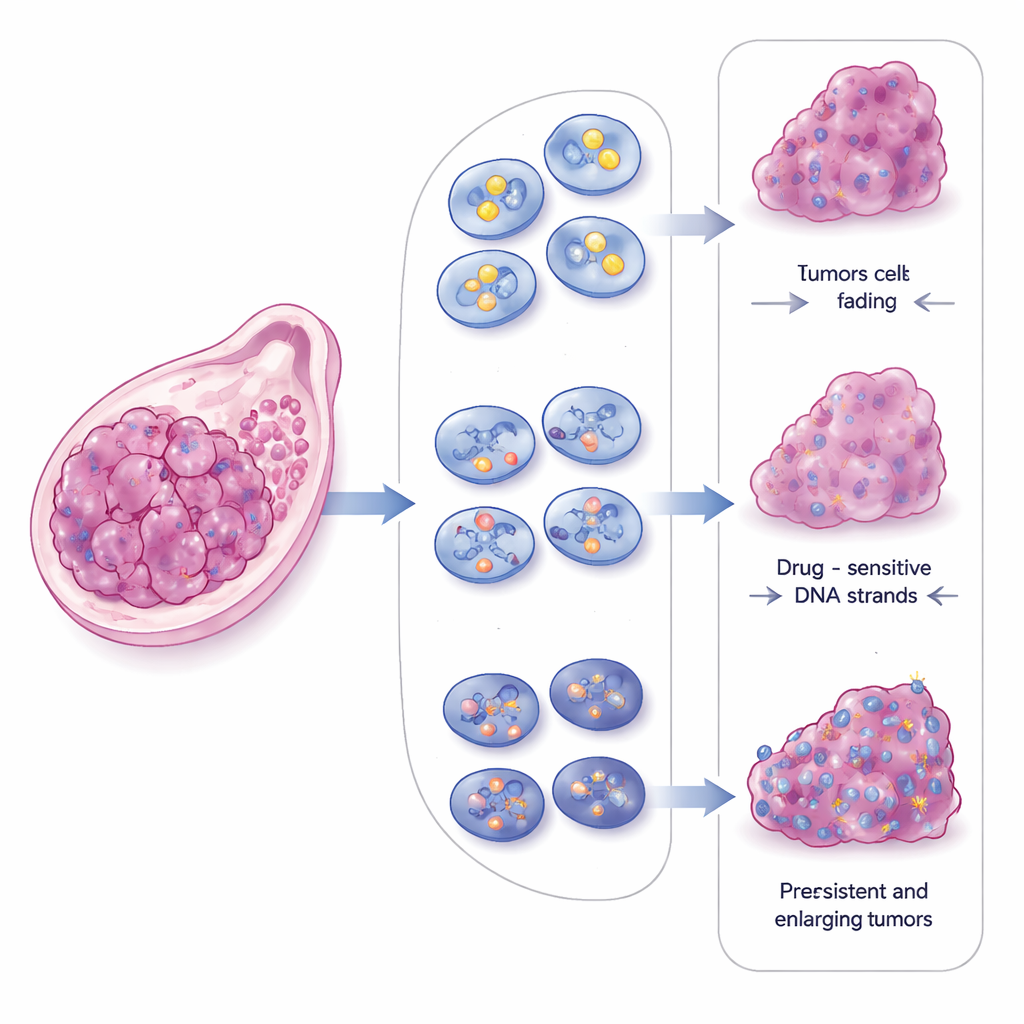
Cómo los condensados de CBX2 organizan al equipo reparador
Profundizando, el equipo examinó qué proteínas reparadoras acababan realmente adheridas al ADN en presencia o ausencia de los condensados de CBX2. Encontraron que las gotas de CBX2 ayudan a reclutar jugadores clave en la respuesta al daño, incluidos PARP1, 53BP1, BRCA1 y RAD51—proteínas que deciden cómo se repara una rotura y luego ejecutan la reparación. La imagen en células vivas reveló dos formas de condensados de CBX2: una forma móvil y líquida que se mezcla dinámicamente con la cromatina dañada, y una forma densa, parecida a un sólido, que no lo hace. Solo las gotas móviles se solaparon con los focos de daño en el ADN y con las principales proteínas de reparación, lo que sugiere que esta fase fluida actúa como el andamiaje funcional que reúne y organiza la maquinaria reparadora precisamente donde se necesita.
Convertir una fortaleza en una debilidad con un fármaco existente
Puesto que los condensados de CBX2 hacen que las células tumorales sean especialmente buenas reparando el ADN, los autores se preguntaron si esa capacidad aumentada podría volverse en su contra. Cribaron una biblioteca de compuestos en células con o sin condensados funcionales de CBX2 y descubrieron que Ibrutinib—un fármaco oral ya aprobado para ciertos cánceres hematológicos—era particularmente tóxico para las células que dependían de los condensados de CBX2. Ibrutinib no impedía la formación de las gotas, pero mermaba de forma selectiva la vía de reparación de alta fidelidad de la que dependen esas células. En modelos animales, los tumores que contenían condensados de CBX2 se redujeron con el tratamiento con Ibrutinib, y organoides tridimensionales derivados de tumores de pacientes con altos niveles de CBX2 fueron más sensibles al fármaco que aquellos con niveles bajos. 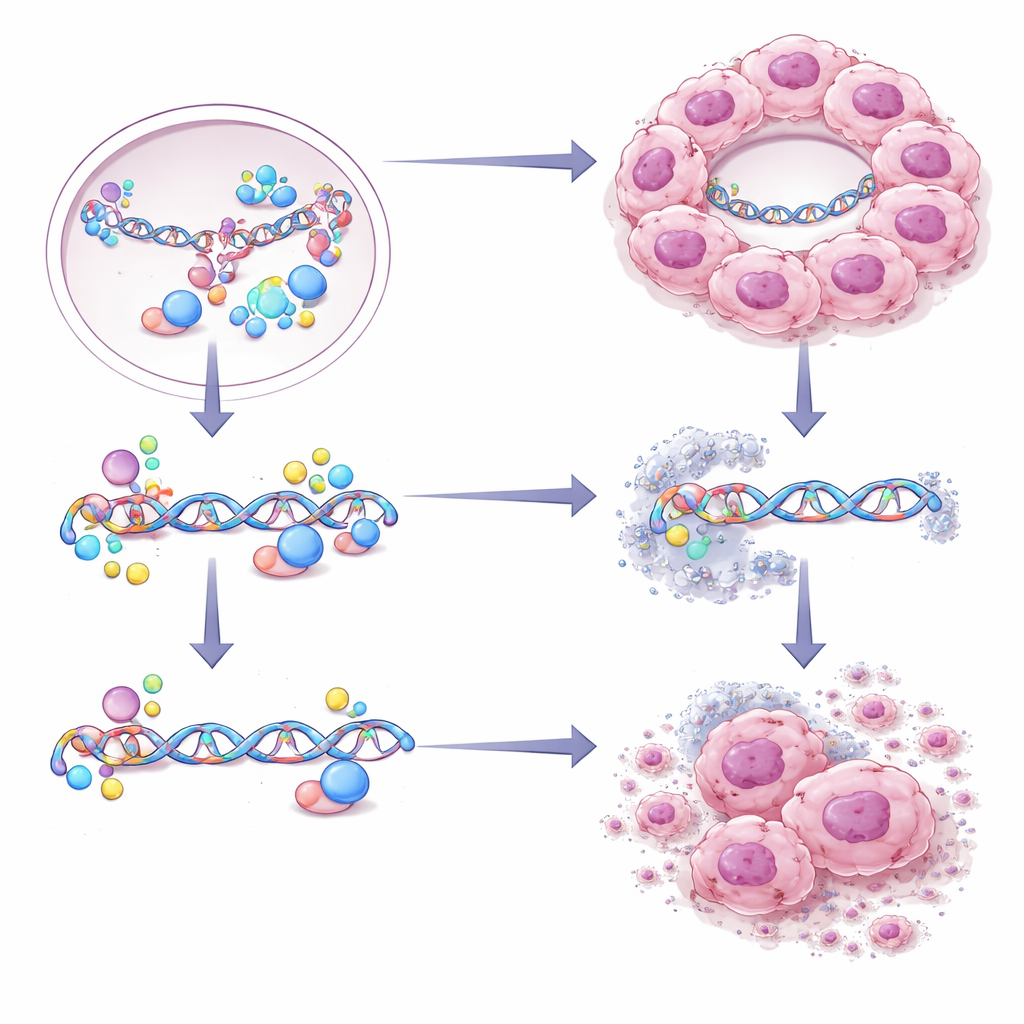
Qué podría significar esto para los pacientes
Para los pacientes, el estudio sugiere dos ideas importantes. Primero, la presencia y el patrón de condensados de CBX2 en tejido tumoral podrían ayudar a predecir la respuesta a la quimioterapia con platino y a los inhibidores de PARP: los pacientes cuyos tumores carecen de CBX2 se comportan mejor, los que muestran CBX2 difuso quedan en un punto intermedio y los que presentan condensados claros de CBX2 tienen peor pronóstico. Segundo, ese mismo patrón de gotas podría señalar a los pacientes que podrían beneficiarse del Ibrutinib, reaprovechando un fármaco para cánceres sanguíneos en un subtipo de cáncer de ovario de difícil tratamiento. En esencia, el trabajo muestra que las mismas estructuras que protegen el ADN tumoral también pueden exponer un nuevo talón de Aquiles—ofreciendo una vía potencial hacia tratamientos más personalizados y efectivos.
Cita: Sun, S., Huang, L., Ma, Y. et al. CBX2 phase-separation contributes to homologous recombination repair and drug resistance in ovarian cancer. Cell Death Dis 17, 366 (2026). https://doi.org/10.1038/s41419-026-08605-4
Palabras clave: cáncer de ovario, resistencia a fármacos, reparación del ADN, separación en fases, Ibrutinib