Clear Sky Science · es
HNRNPH1 impulsa la progresión del glioblastoma regulando el empalme de genes del ciclo celular
Por qué importa este estudio sobre el cáncer cerebral
El glioblastoma es una de las formas más mortales de cáncer cerebral, en parte porque sus células se dividen rápidamente y, aun así, logran evitar la autodestrucción. Este estudio revela cómo una molécula poco conocida dentro de las células tumorales les ayuda a seguir dividiéndose de forma ordenada, en lugar de desmoronarse. Al exponer este sistema de apoyo oculto, el trabajo apunta a nuevas formas en las que los médicos podrían, en el futuro, empujar a las células de glioblastoma más allá del límite y detener el crecimiento tumoral.
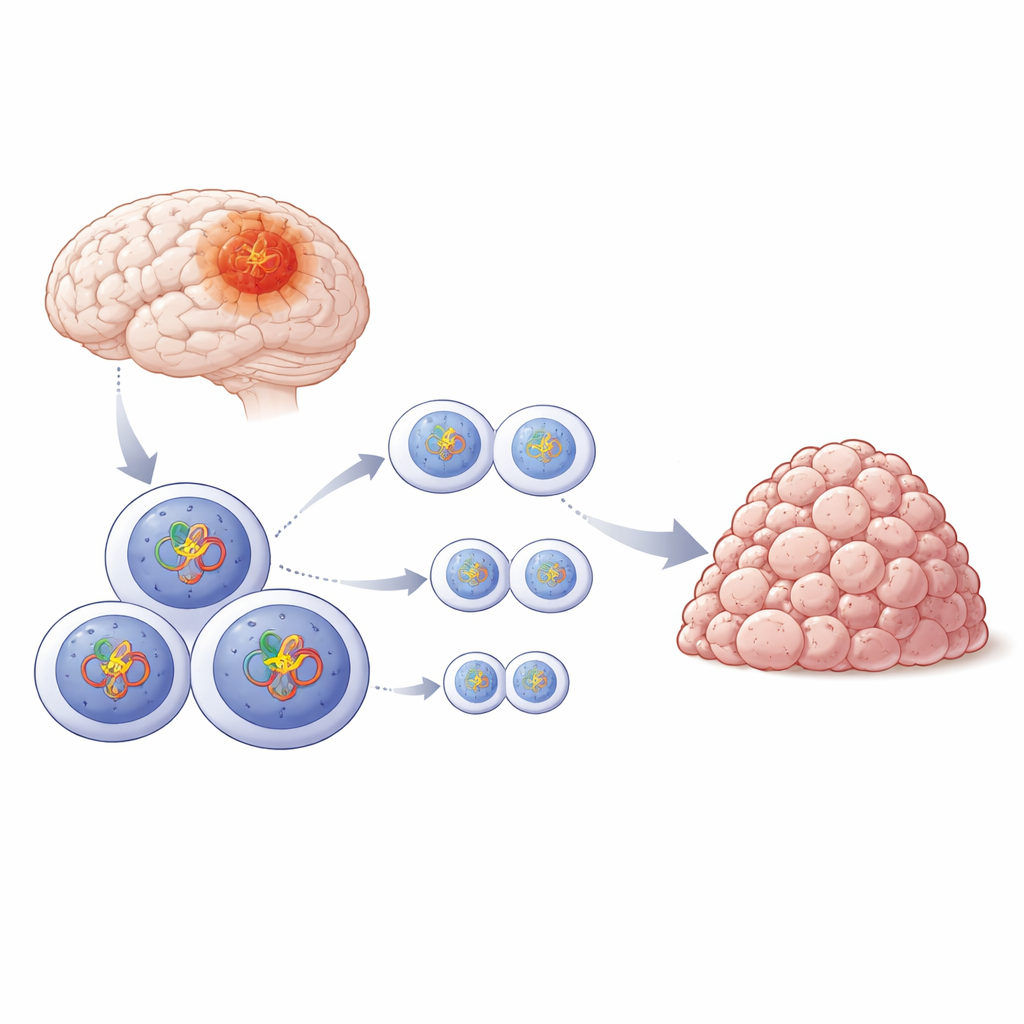
El ayudante oculto dentro de las células tumorales
Los investigadores se centraron en el glioblastoma, un tumor cerebral agresivo que a menudo resiste la cirugía, la radioterapia y la quimioterapia. Las células cancerosas normalmente portan muchas mutaciones en el ADN que las impulsan a dividirse, pero siguen dependiendo de maquinaria intacta para copiar y separar sus cromosomas durante cada ciclo celular. Si esa maquinaria falla, las células pueden morir en un proceso llamado «catástrofe mitótica». El equipo se preguntó qué elementos moleculares ayudan a las células de glioblastoma a preservar este delicado proceso de división, pese a sus genomas dañados.
Un controlador del tráfico para los mensajes genéticos
Se centraron en una proteína llamada HNRNPH1, parte de una familia de moléculas que se unen al ARN —los mensajes de corta vida copiados del ADN. Estas proteínas ayudan a decidir cómo se cortan y cosen los transcritos crudos de ARN antes de convertirse en proteínas, un proceso conocido como empalme. Al analizar grandes conjuntos de datos de pacientes y muestras tumorales, los científicos encontraron que HNRNPH1 se produce en niveles mucho más altos en tejido de glioblastoma que en el cerebro normal. Mapas de una sola célula y espaciales mostraron que es especialmente abundante en células tumorales que se parecen a células cerebrales inmaduras y de rápida división y en regiones bien oxigenadas y altamente proliferativas del tumor, pero mucho más baja en áreas pobres en oxígeno y estresadas.
Cómo HNRNPH1 mantiene la división celular en orden
Para ver qué ocurre cuando se elimina HNRNPH1, el equipo usó herramientas de edición génica y silenciamiento de ARN para reducir esta proteína en células de glioblastoma cultivadas. Esto desencadenó cambios generalizados en la actividad de miles de genes, con efectos particularmente fuertes en los que gobiernan el punto de control G2/M —la última etapa de control de calidad antes de que una célula se divida. Se encontró que HNRNPH1 se une directamente a los moldes de ARN de varios reguladores clave de la división, incluidas proteínas que ayudan a separar correctamente los cromosomas. Cuando HNRNPH1 se perdió, estos ARN se empalmaron de forma incorrecta o se produjeron en cantidades menores, lo que condujo a una reducción de las proteínas necesarias para una mitosis ordenada.
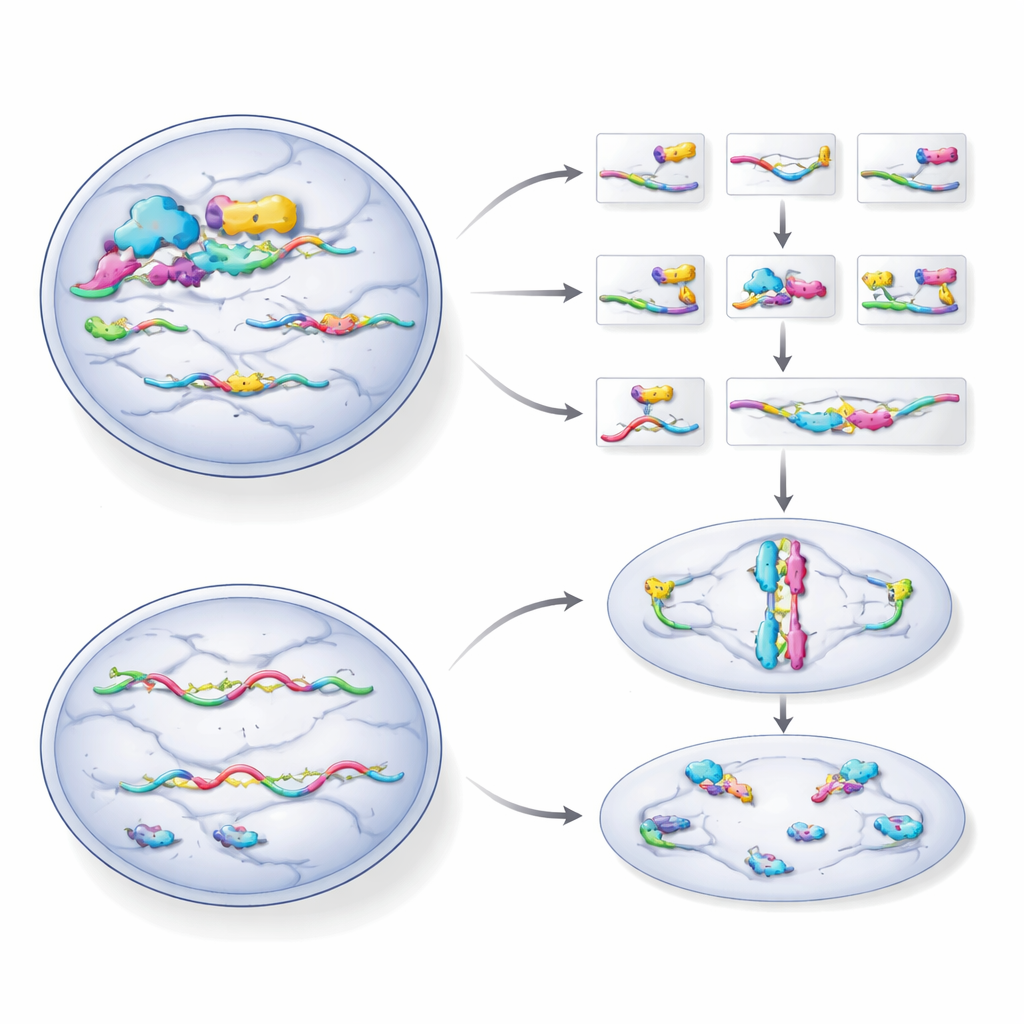
Cuando el ayudante desaparece, la división celular falla
Las células sin HNRNPH1 ralentizaron su crecimiento, se acumularon en las etapas finales del ciclo celular y desarrollaron núcleos agrandados, deformes o fragmentados —señales clásicas de que la división va mal. Bajo el microscopio había menos células en mitosis normal, y su andamiaje interno para separar los cromosomas estaba alterado. El equipo también descubrió que HNRNPH1 dirige el empalme de otro regulador, UHRF2, desplazando su ARN entre una forma productiva y una defectuosa. Sin HNRNPH1, más mensajes de UHRF2 fueron mal editados, disminuyendo la cantidad de proteína funcional y perturbando aún más el control del ciclo celular.
Pruebas a partir de tumores en cerebros vivos
Luego los científicos evaluaron la importancia de HNRNPH1 en modelos de ratón. Implataron células humanas de glioblastoma, normales o modificadas para tener HNRNPH1 reducido, en los cerebros de ratones. Los animales que recibieron células control desarrollaron rápidamente tumores grandes y murieron antes. Los ratones que recibieron células con HNRNPH1 silenciado desarrollaron tumores mucho más pequeños o retrasados y vivieron más tiempo. Sin embargo, los tumores que finalmente crecieron habían recuperado la actividad de HNRNPH1, lo que sugiere que las células incapaces de restaurar esta proteína estaban en clara desventaja y no podían sostener el crecimiento tumoral.
Qué significa esto para futuros tratamientos
En conjunto, el estudio muestra que las células de glioblastoma dependen de HNRNPH1 para procesar correctamente una red de mensajes genéticos que controlan la división celular, lo que les permite proliferar sin autodestruirse de inmediato. Para un lector no experto, esta proteína puede entenderse como un editor tras bambalinas que mantiene legible el manual de instrucciones de la célula cancerosa. Interrumpir HNRNPH1 —o los eventos de empalme específicos que controla— podría hacer que las células tumorales sean más propensas a cometer errores fatales durante la división, abriendo una posible nueva vía terapéutica para llevar al glioblastoma más allá de su punto de quiebre, a la vez que complementa los tratamientos existentes.
Cita: Villa, G.R., Alimonti, P., Toker, J.S. et al. HNRNPH1 drives glioblastoma progression by regulating the splicing of cell cycle genes. Cell Death Dis 17, 352 (2026). https://doi.org/10.1038/s41419-026-08576-6
Palabras clave: glioblastoma, ciclo celular, empalme de ARN, biología tumoral, cáncer cerebral