Clear Sky Science · es
Represión de EGFR por la nueva biguanida 4C potenció la sensibilidad del cáncer de ovario a inhibidores de PARP mediante la regulación a la baja de BRCA2 y Rad51
Por qué importa esta investigación
Para muchas personas diagnosticadas con cáncer de ovario, los fármacos dirigidos actuales solo funcionan en una pequeña minoría cuyos tumores presentan fallos genéticos concretos. Este estudio explora una forma de extender los beneficios de una clase importante de medicamentos, los inhibidores de PARP, al grupo mucho mayor de pacientes cuyos tumores carecen de esas mutaciones. Al combinar un compuesto experimental nuevo con fármacos existentes, los investigadores muestran una estrategia para empujar a las células cancerosas hacia un callejón sin salida letal mientras se preserva el tejido sano.
Un obstáculo en el tratamiento actual del cáncer de ovario
El cáncer de ovario suele detectarse tarde y sigue siendo uno de los cánceres más letales que afectan a las mujeres. Los inhibidores de PARP, como el olaparib, pueden ser notablemente eficaces, pero principalmente en pacientes cuyos tumores ya presentan defectos en una vía de reparación del ADN vinculada a los genes BRCA1 y BRCA2. Sin embargo, la mayoría de los tumores aún tienen la maquinaria de reparación intacta y pueden reparar el daño del ADN causado por estos fármacos, lo que permite que las células cancerosas sobrevivan. Una parte clave de este equipo de reparación incluye dos proteínas, BRCA2 y Rad51, que ayudan a recomponer las hebras de ADN rotas mediante un proceso llamado recombinación homóloga. Encontrar formas de debilitar selectivamente esta vía de reparación en las células tumorales podría hacer que los inhibidores de PARP sean útiles para muchos más pacientes.
El papel de un interruptor de crecimiento bien conocido
El equipo se centró en una molécula vinculada al cáncer y bien conocida, el receptor del factor de crecimiento epidérmico (EGFR), que se encuentra en la superficie de muchas células tumorales y promueve su crecimiento. Descubrieron que EGFR hace más que enviar señales de proliferación: en células de cáncer de ovario con genes BRCA normales, niveles altos de EGFR se asociaron con peor supervivencia de los pacientes y con resistencia a los inhibidores de PARP. Cuando EGFR se redujo o se inhibió en cultivos celulares y en ratones, los tumores se volvieron mucho más vulnerables al olaparib. Los investigadores demostraron que EGFR ayuda a transportar BRCA2 y Rad51 al núcleo celular tras el daño en el ADN, donde pueden reparar las roturas y atenuar el efecto del tratamiento. Bloquear simplemente la actividad enzimática de EGFR no fue suficiente; la cantidad total de proteína EGFR tuvo que disminuir para perturbar significativamente esta vía de reparación.
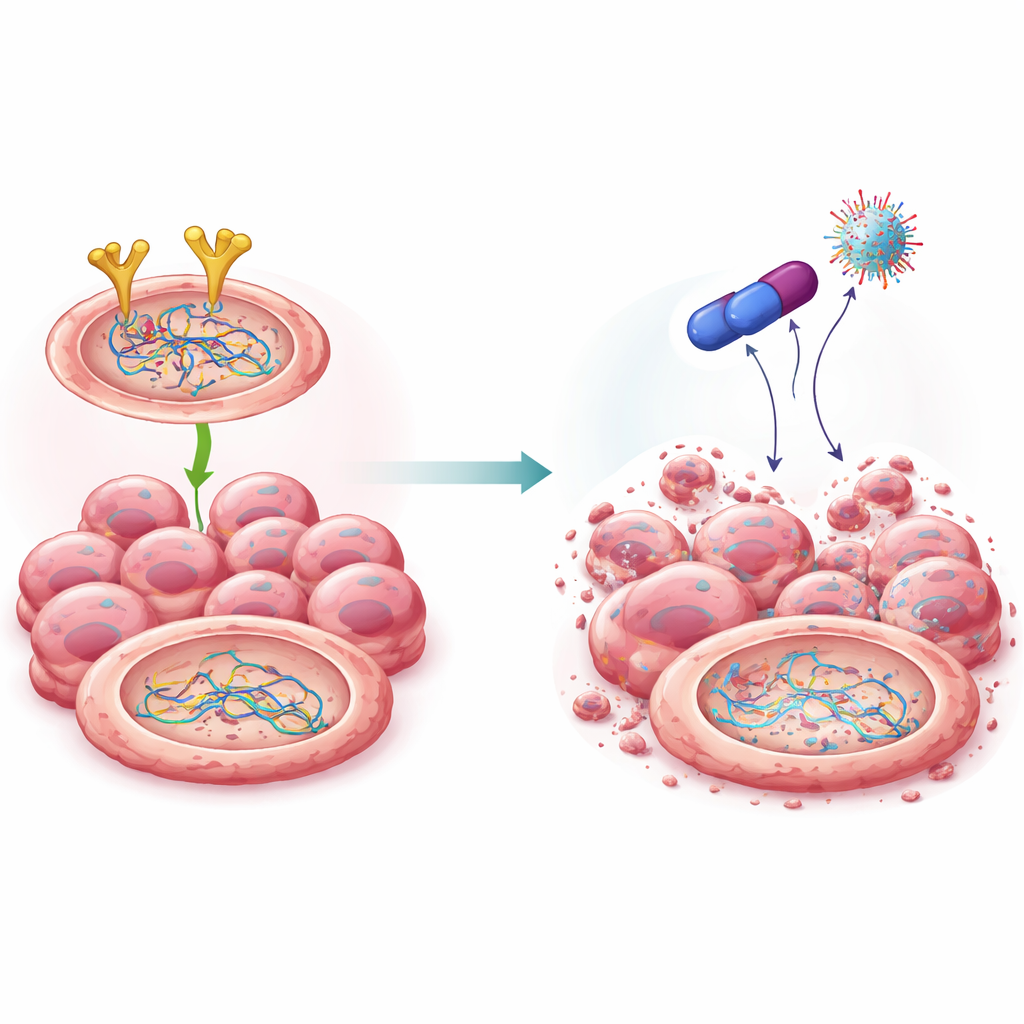
Un compuesto nuevo que desactiva al equipo reparador
Basándose en trabajos previos con una familia de fármacos conocida como biguanidas, los científicos sintetizaron varios análogos químicos e identificaron una molécula destacada, llamada 4C. Este compuesto fue altamente tóxico para las células de cáncer de ovario pero relativamente benigno para las células normales. Modelos informáticos y pruebas de laboratorio indicaron que 4C se une directamente a EGFR y lo marca para su destrucción en la maquinaria celular degradadora de proteínas. A diferencia de algunos fármacos existentes contra EGFR, 4C redujo la cantidad global de EGFR en lugar de limitarse a silenciar su actividad. A medida que los niveles de EGFR disminuyeron, también cayó la estabilidad de BRCA2 y Rad51: fueron etiquetadas para su eliminación, degradadas y dejaron de poder sostener una reparación eficiente del ADN. Es importante que esta poda ocurriera a nivel de proteína sin alterar los genes subyacentes.
Bloquear una vía de rescate dentro de la célula
El estudio desentrañó una cadena de eventos más detallada que conecta el daño del ADN con la supervivencia tumoral. Tras la lesión inducida por los inhibidores de PARP, otra proteína sensor llamada ATM envía un mensaje desde el núcleo al citoplasma. En respuesta, EGFR se asocia con BRCA2 y Rad51 y les ayuda a trasladarse al núcleo, donde reparan el daño. Los investigadores descubrieron que una tercera proteína, c-Cbl, actúa normalmente como una especie de etiquetador para la eliminación de BRCA2 y Rad51. EGFR compite con c-Cbl por el acceso a estas proteínas reparadoras, protegiéndolas de ser marcadas para su destrucción. Cuando 4C reduce los niveles de EGFR, c-Cbl puede unirse más fácilmente a BRCA2 y Rad51, lo que conduce a su marcaje, degradación y pérdida. Con menos proteínas reparadoras en el núcleo, las lesiones del ADN se acumulan y las células cancerosas se vuelven mucho más sensibles a los inhibidores de PARP.
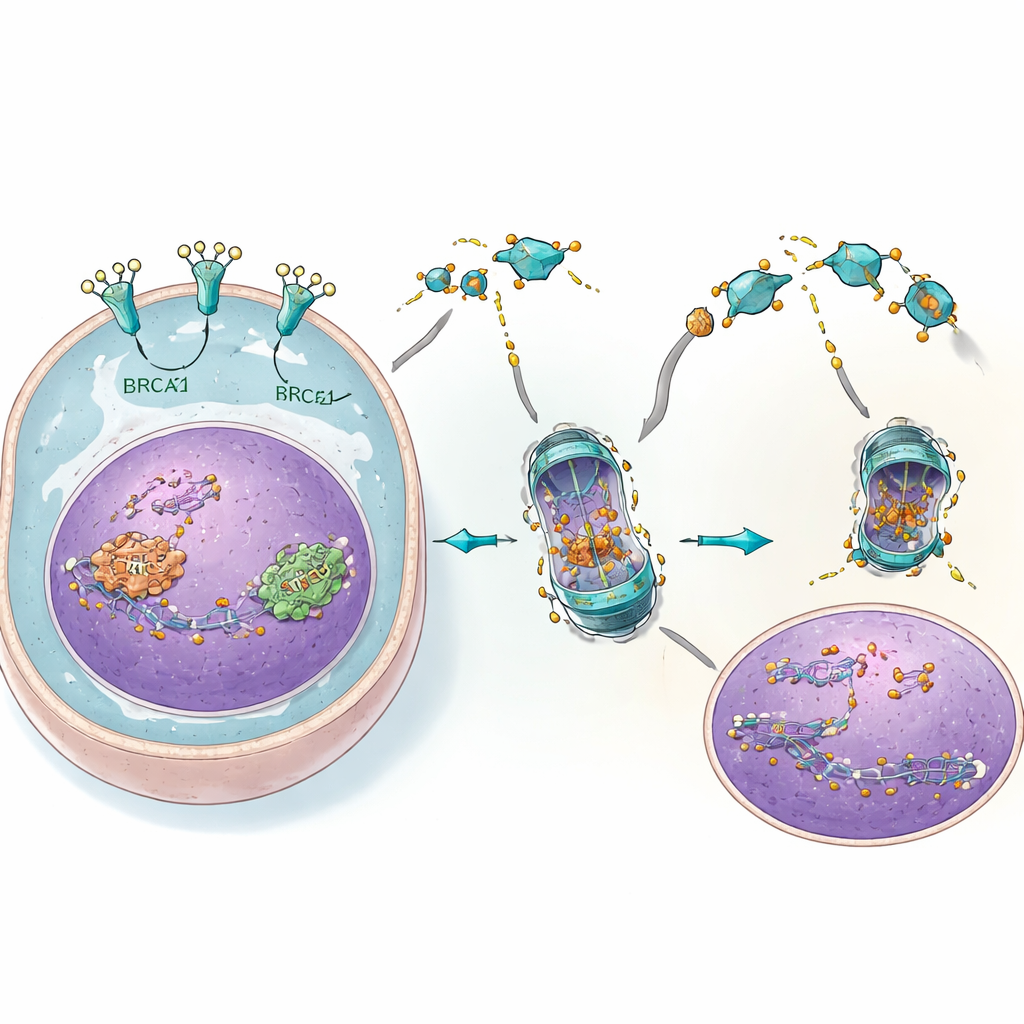
De las células a los animales: una combinación potente
Tanto en cultivos celulares como en modelos murinos, la combinación de 4C con inhibidores de PARP produjo un potente efecto sinérgico. Los tumores con genes BRCA normales que resistían cada fármaco por separado se redujeron drásticamente o dejaron de crecer cuando se expusieron a ambos simultáneamente. Los marcadores de daño en el ADN aumentaron notablemente, coherente con la idea de que la reparación estaba siendo desbordada. Al mismo tiempo, las células normales y órganos clave como el hígado y los riñones mostraron pocas evidencias de daño, probablemente porque presentan niveles mucho más bajos de EGFR y dependen menos de este atajo reparador. Los beneficios de la combinación se extendieron a la reducción de la diseminación de células de cáncer de ovario en el organismo.
Qué podría significar esto para los pacientes
Este trabajo propone una forma de convertir la fortaleza de una célula cancerosa en una debilidad. Al dirigirse a EGFR con el novedoso compuesto 4C, los investigadores eliminan la protección que brindan BRCA2 y Rad51, haciendo que tumores con reparación del ADN aparentemente normal se comporten más como cánceres con mutaciones en BRCA en su respuesta a los inhibidores de PARP. Esta vulnerabilidad forzada, conocida como «letalidad sintética», podría ampliar el alcance de fármacos existentes a muchas más mujeres con cáncer de ovario, manteniendo los efectos secundarios manejables. Aunque 4C sigue siendo experimental y requerirá pruebas extensivas en modelos más avanzados y ensayos clínicos, el estudio ofrece un plano claro de cómo desmantelar ayudantes específicos de la reparación en células tumorales podría mejorar los resultados terapéuticos.
Cita: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Palabras clave: cáncer de ovario, inhibidores de PARP, EGFR, reparación del ADN, terapia dirigida