Clear Sky Science · es
Pérdida de PRKACB facilita la metástasis del cáncer gástrico de tipo difuso mediante la activación de la señalización RhoA
Por qué este estudio importa para el cáncer de estómago
El cáncer gástrico de tipo difuso es una forma particularmente agresiva de cáncer de estómago que con frecuencia se disemina ampliamente dentro del abdomen, lo que lo hace difícil de tratar y letal. Este estudio investiga por qué estos tumores tienden tanto a propagarse, desvelando un sistema molecular de frenado que normalmente impide que las células cancerosas se dispersen, y mostrando lo que ocurre cuando ese freno falla. Comprender este interruptor de control oculto podría abrir nuevas vías para predecir qué pacientes tienen mayor riesgo y para desarrollar fármacos que ralenticen o detengan esa diseminación peligrosa.
Una forma peligrosa de cáncer de estómago
No todos los cánceres de estómago se comportan igual. Los tumores de tipo intestinal tienden a formar masas más estructuradas, mientras que el cáncer gástrico de tipo difuso (CGD) está formado por células dispersas que se desprenden con facilidad del tumor primario. Los pacientes con CGD tienen un riesgo de muerte mayor que los con enfermedad de tipo intestinal, en parte porque sus tumores siembran con más facilidad nuevos crecimientos por toda la cavidad abdominal. Estudios genéticos previos ya habían vinculado el CGD con cambios recurrentes en un gen llamado RHOA, que influye en cómo las células se mueven y cambian de forma. Pero no estaba claro cómo esos cambios se conectaban con las redes de señalización más amplias que controlan si las células cancerosas permanecen en su sitio o migran.
Encontrando un freno perdido en muestras tumorales
Los investigadores se centraron en una proteína llamada PRKACB, una subunidad catalítica de la bien conocida enzima proteína cinasa A, que ajusta muchos comportamientos celulares al añadir grupos fosfato a otras proteínas. Una encuesta proteómica anterior había sugerido que los niveles de PRKACB eran inusualmente bajos en CGD agresivos. Para comprobarlo, el equipo examinó muestras tumorales de 376 pacientes, comparando cánceres de tipo difuso e intestinal y su tejido no canceroso cercano. Encontraron que los niveles de PRKACB estaban marcadamente reducidos en los tumores de tipo difuso, especialmente en estadios avanzados, pero no en los cánceres de tipo intestinal. Los pacientes cuyos tumores tenían poca PRKACB presentaron una supervivencia global significativamente peor, incluso después de tener en cuenta otros factores clínicos, lo que sugiere que PRKACB actúa como supresor tumoral en este contexto.
Cómo el PRKACB bajo alimenta la fuga celular
Para ver qué hace PRKACB dentro de las células cancerosas, el equipo usó líneas celulares en cultivo que modelan el cáncer gástrico de tipo difuso. Cuando redujeron artificialmente PRKACB, las células se volvieron más móviles e invasivas en pruebas de laboratorio, atravesando barreras con mayor facilidad y formando proyecciones digitiformes llamadas pseudópodos que ayudan a las células a desplazarse. Estas células también pasaron de un estado epitelial más ordenado a uno más laxo y semejante al mesenquimal, asociado a la metástasis, perdiendo la molécula de adhesión E‑cadherina que normalmente ayuda a las células a mantenerse unidas. Por el contrario, aumentar los niveles de PRKACB hizo que las células migraran e invadieran menos. Es importante que estos cambios no alteraron la velocidad de proliferación celular, lo que apunta a un papel específico de PRKACB en facilitar la diseminación, no el crecimiento.
Acercándose al interruptor de señalización RhoA
Los investigadores preguntaron entonces cómo ejerce PRKACB este efecto antimetastásico. Utilizando métodos de interacción proteína–proteína y modelado estructural, mostraron que PRKACB se une directamente a RhoA, un interruptor molecular que alterna entre formas inactivas y activas para gobernar la forma y el movimiento celular. PRKACB añade un grupo fosfato en una posición específica de RhoA (serina 188), lo que atenúa RhoA y reduce las vías descendentes ROCK y FAK que impulsan la reorganización del citoesqueleto y la motilidad celular. Cuando PRKACB se redujo, RhoA estaba menos fosforilado, más activo, y la señalización ROCK/FAK se intensificó, conduciendo a un movimiento celular más agresivo. En modelos murinos donde se implantaron tumores con características humanas en la pared del estómago, la disminución de PRKACB produjo más nódulos metastásicos y de mayor tamaño en el abdomen y una aparición más temprana de la diseminación visible, nuevamente sin cambiar la rapidez con que crecían las metástasis ya establecidas.
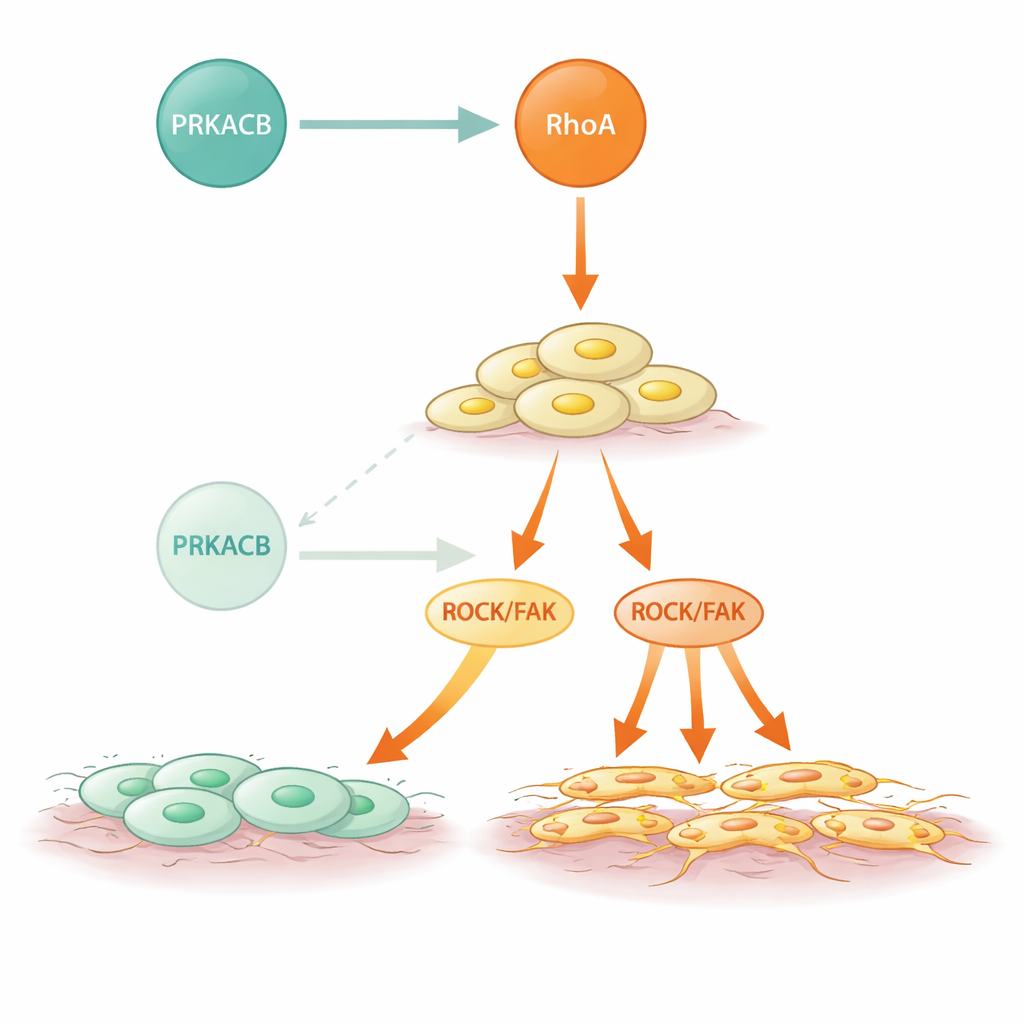
Señalización mutante y una posible forma de intervenir
Los cánceres gástricos de tipo difuso a menudo albergan mutaciones en RHOA, y este estudio muestra cómo algunos de esos cambios amplifican el problema. Varias mutaciones frecuentes asociadas al CGD en RhoA debilitaron o abolieron su unión a PRKACB pero no afectaron la capacidad de RhoA para activar a sus socios posteriores. Como resultado, estas formas mutantes eludieron la fosforilación restrictiva por PRKACB y mostraron una actividad ROCK más elevada y un comportamiento invasivo más intenso. De manera llamativa, cuando los investigadores trataron células y ratones con un compuesto bloqueador de RhoA, la metástasis adicional causada por la baja de PRKACB se revirtió en gran medida. Esto sugiere que incluso en tumores donde el freno natural es débil o está ausente, dirigirse directamente a la vía RhoA hiperactiva podría frenar la diseminación.
Qué significa esto para los pacientes y las futuras terapias
En términos sencillos, este trabajo identifica a PRKACB como una pieza clave de un circuito interno “anti-migración” en el cáncer gástrico de tipo difuso. Cuando los niveles de PRKACB caen, o cuando RhoA está mutado de modo que PRKACB no puede unirse ni modificarlo, la señalización de RhoA se intensifica y las células cancerosas se vuelven más aptas para desprenderse y colonizar la cavidad abdominal. Medir el estado de PRKACB y RhoA en los tumores podría ayudar a los médicos a evaluar la probabilidad de metástasis de un cáncer y a identificar quién podría beneficiarse más de fármacos que inhiban la vía RhoA–ROCK–FAK. Aunque tales tratamientos necesitarán más desarrollo y pruebas clínicas, el estudio traza una ruta molecular clara desde un freno perdido hasta la diseminación mortal, y apunta a nuevas maneras de frenar ese proceso.
Cita: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Palabras clave: cáncer gástrico de tipo difuso, metástasis, PRKACB, señalización RhoA, vía ROCK FAK