Clear Sky Science · es
La señalización leptina-LEPR en la médula ósea reconfigura el metabolismo oxidativo mitocondrial para conferir quimiorresistencia en la leucemia mieloide aguda
Por qué la grasa en la médula ósea importa para el tratamiento de la leucemia
Mucha gente sabe que la grasa corporal puede influir en enfermedades como la diabetes y los problemas cardíacos, pero pocos se dan cuenta de que la grasa oculta dentro de los huesos también puede afectar cómo responden los cánceres de la sangre al tratamiento. Este estudio explora cómo una hormona producida por los adipocitos, llamada leptina, ayuda a proteger a las células de la leucemia mieloide aguda (LMA) frente a la quimioterapia estándar. Comprender este sistema de protección oculto podría señalar nuevas maneras de mejorar la eficacia de los fármacos existentes para los pacientes.
Una hormona que inclina la balanza contra la quimioterapia
Los investigadores comenzaron estudiando muestras de médula ósea de adultos recién diagnosticados de LMA. Midieron los niveles de leptina en la médula y analizaron qué tan bien los pacientes eliminaban las células leucémicas tras recibir un fármaco quimioterápico común llamado citarabina. Los pacientes con mayor leptina en la médula y mayores niveles de su receptor en las células leucémicas respondieron menos al tratamiento y tuvieron una supervivencia más corta. Incluso tras ajustar por otros factores de riesgo, la leptina siguió siendo un indicador fuerte de que la quimioterapia funcionaría peor. Esto sugiere que la hormona derivada de la grasa hacía algo más que reflejar la gravedad de la enfermedad; estaba vinculada activamente a la resistencia.
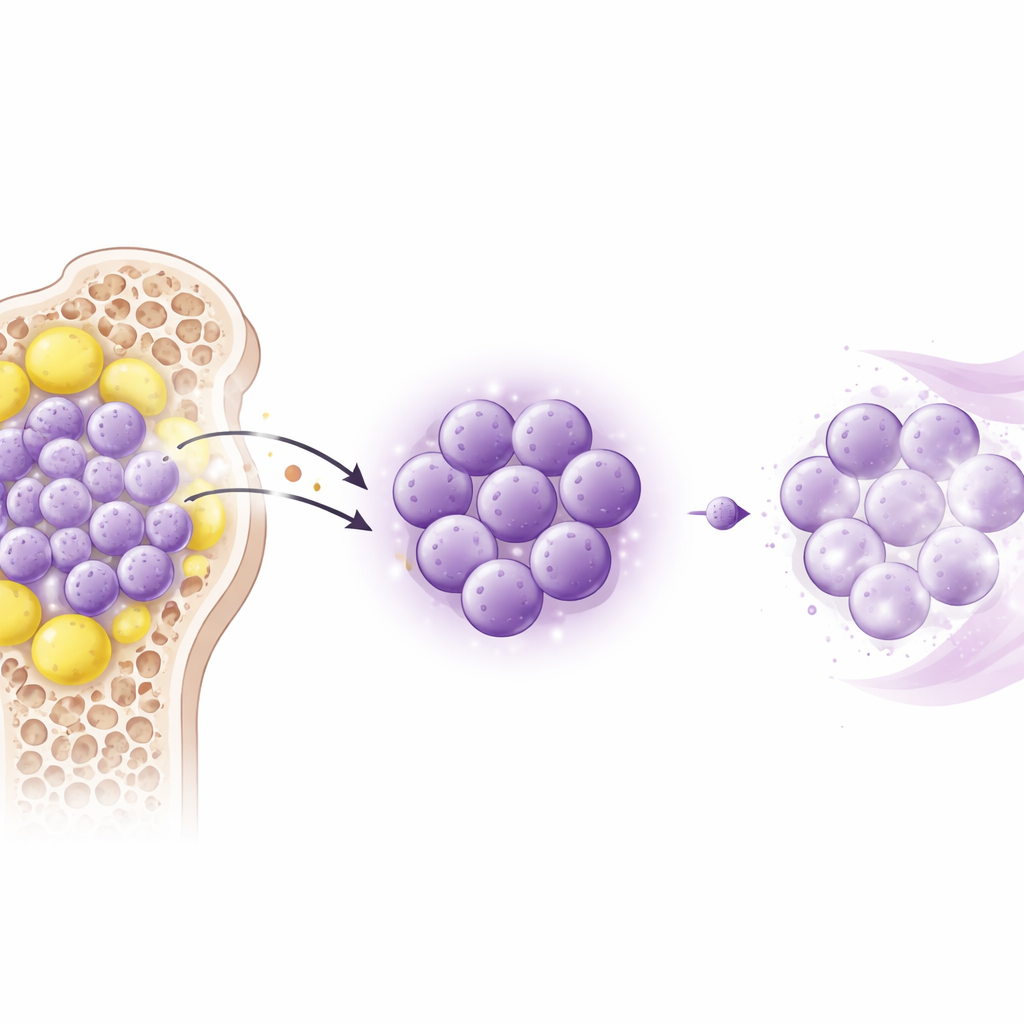
Modelos animales revelan un escudo oculto
Para probar si la leptina causa realmente resistencia a los fármacos, el equipo recurrió a dos modelos murinos de LMA que imitan de cerca la enfermedad humana. Los ratones recibieron citarabina sola, citarabina más leptina adicional, o citarabina junto con un péptido pequeño que bloquea el receptor de leptina. Añadir leptina acortó la supervivencia, agrandó el bazo y el hígado, y permitió que las células leucémicas invadieran estos órganos a pesar de la quimioterapia. En contraste, bloquear el receptor no frenó el crecimiento leucémico por sí solo, pero aumentó significativamente el efecto de la citarabina, reduciendo el tamaño de los órganos afectados y la carga de leucemia. Estos hallazgos muestran que el efecto principal de la leptina no es acelerar directamente el crecimiento tumoral, sino hacer que las células leucémicas sean más difíciles de eliminar cuando se aplica quimioterapia.
Poniendo en marcha los centros de energía de la célula
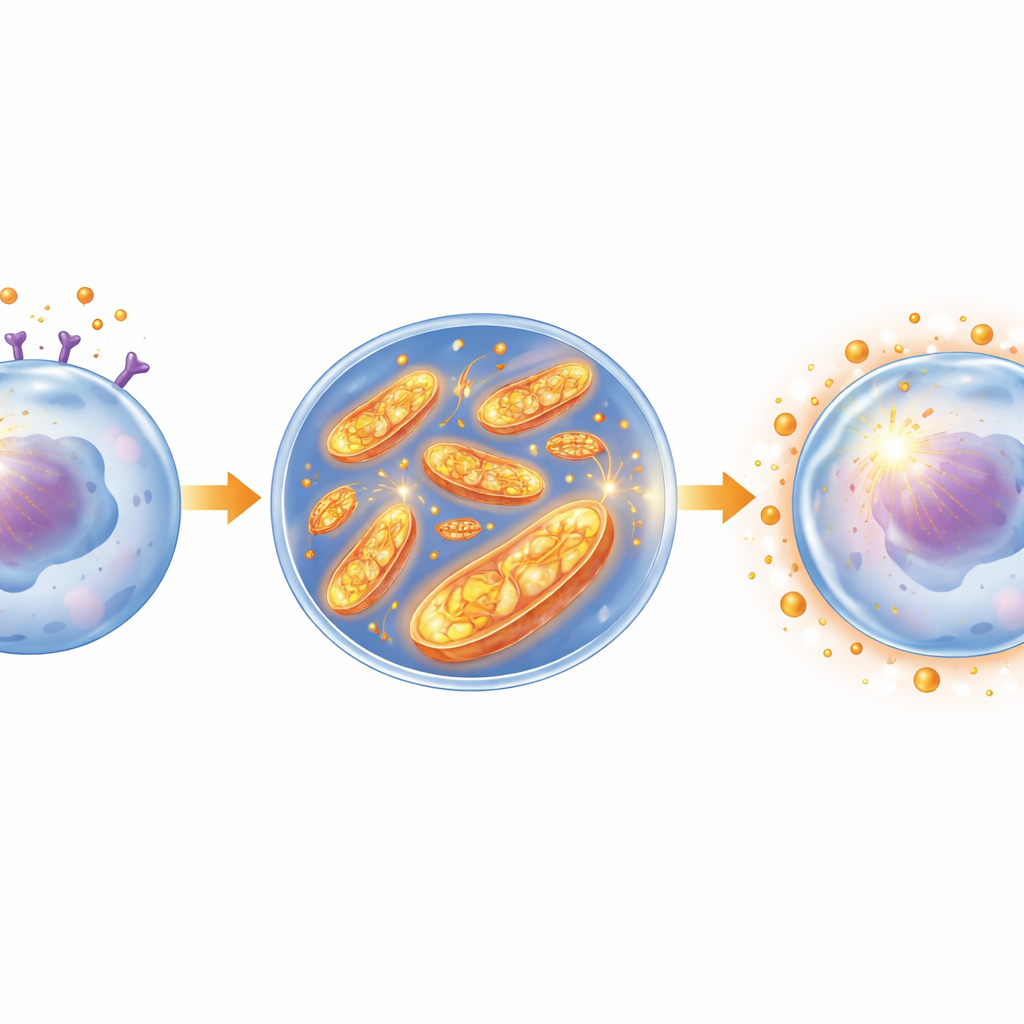
Profundizando, los científicos examinaron cómo la leptina cambia el metabolismo de las células leucémicas. Encontraron que la leptina activa una cadena de señalización dentro de la célula, conocida como JAK2/STAT3, que a su vez aumenta la actividad mitocondrial: las pequeñas centrales energéticas que producen energía. Tanto en células leucémicas murinas como en líneas celulares humanas de LMA, la leptina potenció la actividad de un componente mitocondrial clave, el complejo I, e incrementó el metabolismo oxidativo general. Este cambio generó más especies reactivas de oxígeno dentro de las mitocondrias. Paradójicamente, en lugar de dañar las células, este aumento sostenido de moléculas reactivas desencadenó una respuesta adaptativa: las células leucémicas reforzaron sus defensas antioxidantes, como el glutatión y enzimas detoxificantes, creando un poderoso escudo interno.
Cuando el estrés se convierte en armadura
El equipo demostró que este escudo es central para la quimiorresistencia. Las células leucémicas tratadas con leptina mostraron una mayor capacidad antioxidante total y se vieron menos afectadas por la citarabina y otro fármaco, daunorrubicina. Eliminar el receptor de leptina mediante edición genética debilitó esta red antioxidante, redujo los niveles de moléculas protectoras y volvió a las células mucho más sensibles al tratamiento, incluso en ausencia de leptina. Experimentos adicionales confirmaron que una ráfaga aguda de estrés mitocondrial también puede desencadenar un programa protector similar, mientras que eliminar estas moléculas reactivas desmanteló el escudo y restauró la sensibilidad a los fármacos. De forma importante, bloquear la señalización JAK2/STAT3 o el propio receptor de leptina impidió la activación del complejo I, redujo las señales de estrés mitocondrial, colapsó la barrera antioxidante y volvió a hacer efectiva la quimioterapia.
Convertir una debilidad en un nuevo enfoque terapéutico
Para los pacientes, el mensaje del estudio es que las células leucémicas pueden explotar una hormona producida por adipocitos vecinos para sobrevivir a la quimioterapia. La leptina procedente de la grasa de la médula ósea se une a su receptor en las células leucémicas, reprograma sus mitocondrias hacia un modo de alta producción energética y aprovecha el estrés de bajo nivel resultante para activar una red antioxidante de seguridad. Esta red protege a las células del daño más severo causado por los fármacos contra el cáncer. Al bloquear el receptor de leptina o su señalización descendente, los médicos podrían algún día ser capaces de despojar a las células de esta protección y permitir que las quimioterapias existentes funcionen como corresponde, sin aumentar necesariamente las dosis de fármaco. De este modo, comprender mejor cómo la grasa de la médula ósea se comunica con las células leucémicas podría traducirse directamente en remisiones más duraderas para las personas con LMA.
Cita: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
Palabras clave: leucemia mieloide aguda, leptina, quimiorresistencia, mitocondrias, estrés oxidativo