Clear Sky Science · es
La miosina nuclear 1 vincula la arquitectura genómica con la remodelación del tejido adiposo, la inflamación metabólica y la obesidad en ratones
Por qué importa el esqueleto celular para la grasa corporal
La obesidad suele atribuirse a lo que comemos y a cuánto nos movemos, pero en el interior de nuestras células la forma en que el ADN se empaqueta y se lee también puede inclinar la balanza. Este estudio revela que una minúscula proteína motora, la miosina nuclear 1 (NM1), que ayuda a organizar el ADN dentro del núcleo celular, desempeña un papel sorprendente en cómo se forman las células adiposas, almacenan energía y desencadenan inflamación. Al estudiar ratones que carecen de esta proteína, los investigadores descubrieron un vínculo directo entre la arquitectura física de nuestros genes y el desarrollo de grasa visceral poco saludable y problemas metabólicos.
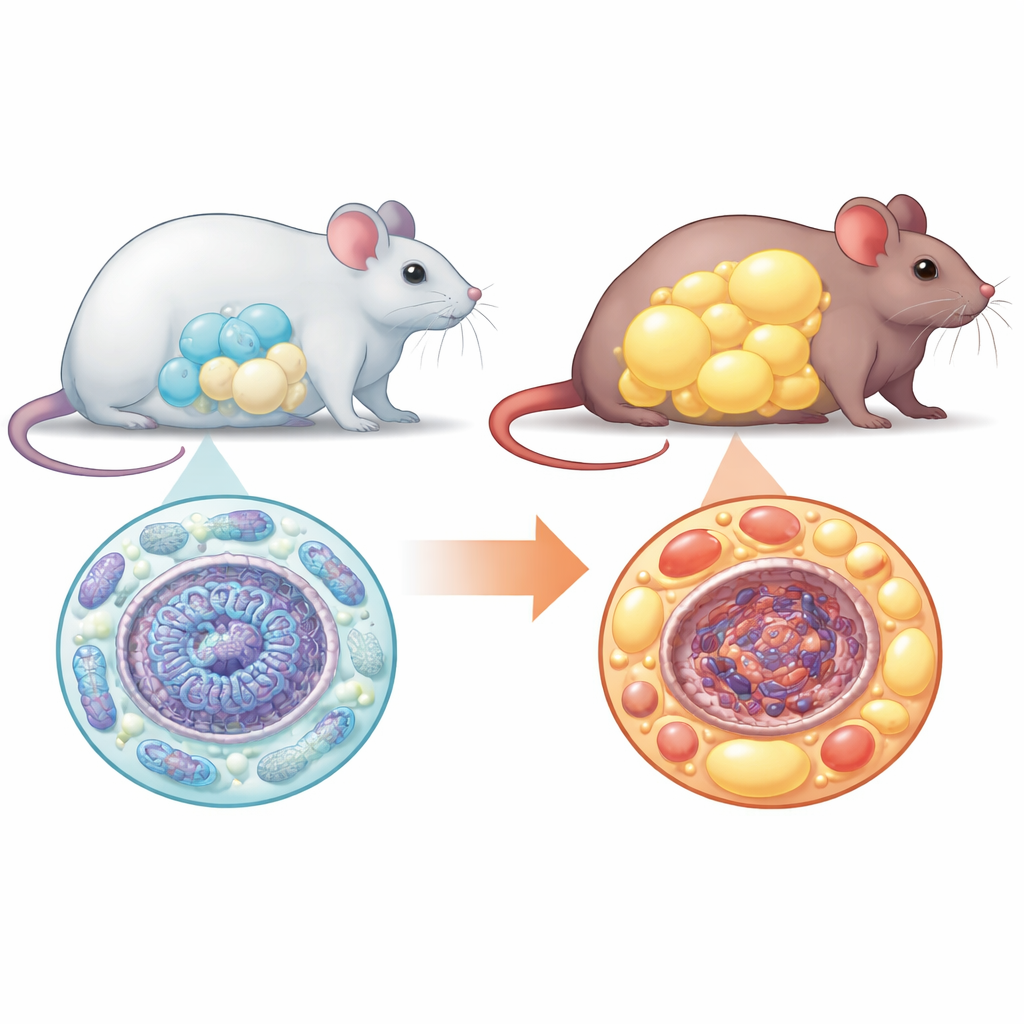
De las células madre a las células grasas
Las células adiposas se desarrollan a partir de precursores versátiles llamados células madre mesenquimales. Normalmente, estos precursores se multiplican, cambian su uso de energía y maduran en muchas células grasas pequeñas y bien funcionantes que almacenan de forma segura las calorías sobrantes. El equipo halló que sin NM1, este proceso ordenado se derrumba. Cuando hicieron crecer en el laboratorio células madre procedentes de ratones normales y de ratones deficientes en NM1 y las indujeron a convertirse en adipocitos, muchas menos células completaron la transición en ausencia de NM1. Las células que sí maduraron eran notablemente más grandes de lo normal, repletas de grasa pero sin la firma habitual de adipocitos saludables a nivel génico y proteico. Este patrón —menos células, pero cada una agrandada— es una marca distintiva del tejido adiposo poco saludable.
Cómo el empaquetamiento génico moldea el comportamiento de las células grasas
NM1 actúa en el núcleo, donde ayuda a mantener tramos de ADN accesibles para que genes importantes puedan activarse. Para entender cómo su pérdida cambia el comportamiento celular, los investigadores superpusieron mapas de regiones de ADN abiertas con medidas de actividad génica en células con y sin NM1. Observaron que muchos genes necesarios para la formación de adipocitos, el manejo de gotas grasas y el mantenimiento mitocondrial perdieron tanto accesibilidad como actividad cuando faltaba NM1. Al mismo tiempo, otros genes vinculados a vías de crecimiento y señalización se volvieron más accesibles y más activos. Esto señaló a NM1 como un controlador del tráfico: ayuda a mantener un paisaje equilibrado de regiones de ADN abiertas y cerradas para que las redes genéticas correctas impulsen el desarrollo y el metabolismo saludables de las células grasas.
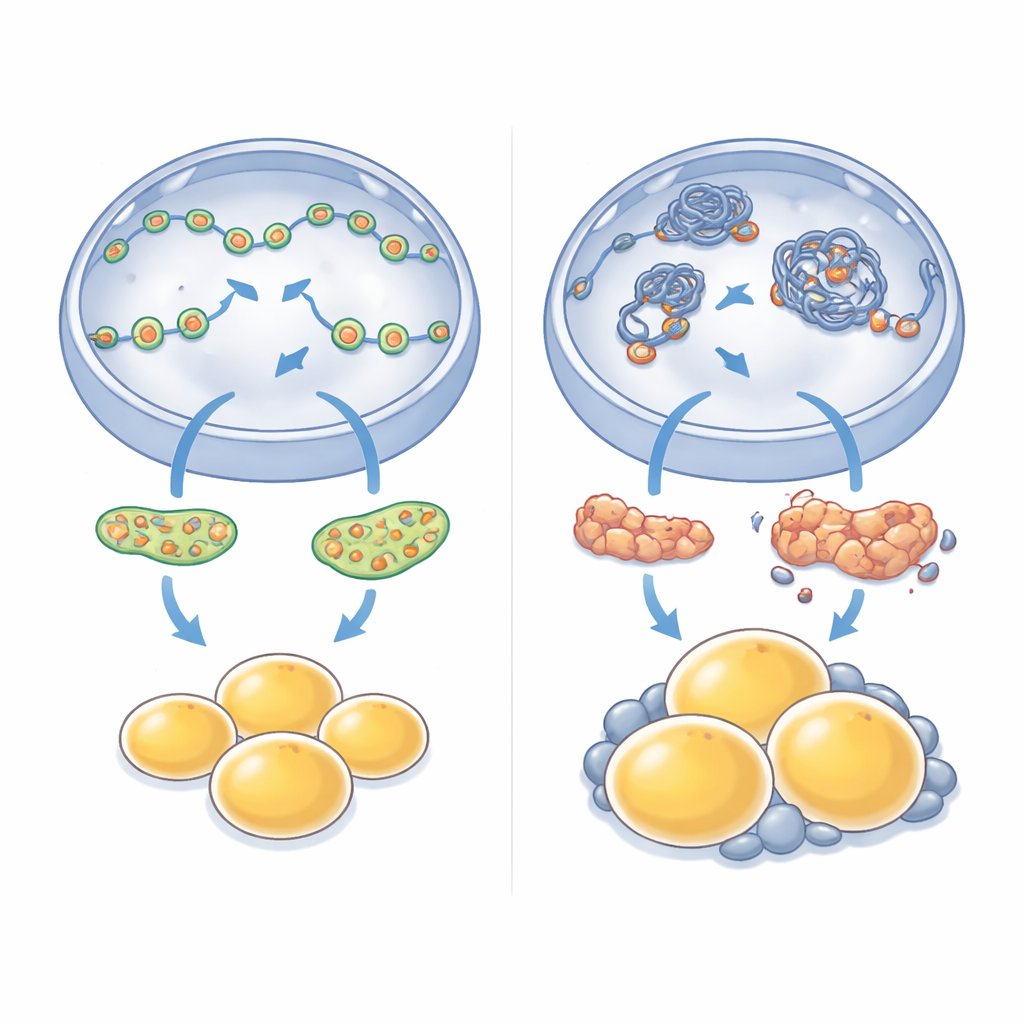
Cuando los cambios locales se traducen en aumento de peso corporal
Las consecuencias de perder este único motor nuclear no se limitaron a las células en un plato. Los ratones sin NM1 se volvieron progresivamente más pesados que sus compañeros normales, aunque no consumían más alimento. Las exploraciones y el análisis de tejidos mostraron una acumulación clara de grasa, especialmente alrededor de los órganos internos del abdomen, y las células adiposas individuales en estas zonas estaban llamativamente agrandadas. Cuando los investigadores midieron qué genes estaban aumentados o disminuidos en esta grasa visceral, encontraron cambios generalizados: las vías implicadas en el uso de energía, la señalización de la insulina y la remodelación tisular fueron reprogramadas. Los genes asociados con el crecimiento y la expansión de adipocitos a menudo se veían potenciados, mientras que varios controladores centrales de la formación saludable de adipocitos estaban atenuados, reflejando los defectos observados en las células madre cultivadas.
Grasa inflamada y motores energéticos alterados
Más allá del tamaño, el tejido adiposo en los ratones deficientes en NM1 mostró signos de inflamación y estrés metabólico. Un análisis detallado de vías destacó una fuerte activación de señales inmunes impulsadas por moléculas como el interferón gamma y el factor de necrosis tumoral, conocidas por contribuir a la resistencia a la insulina y a la enfermedad metabólica. Al mismo tiempo, los reguladores que favorecen un tejido adiposo tranquilo y eficiente energéticamente estaban suprimidos. El estudio también relacionó la pérdida de NM1 con mitocondrias alteradas: los motores energéticos de la célula. Genes que normalmente supervisan el control de calidad mitocondrial y el cambio entre producción de energía eficiente y la vía glucolítica rápida estaban desregulados, lo que sugiere que cuando falta NM1, los adipocitos adoptan una estrategia energética menos eficiente y más propensa al estrés.
Señales compartidas entre ratones y humanos
Para averiguar si esta vía nuclear podría ser relevante en humanos, los autores examinaron grandes conjuntos de datos genéticos de grasa visceral humana. Se centraron en un pariente humano de NM1 llamado MYO1C y estudiaron redes de variantes que ajustan la actividad de genes cercanos. Encontraron que muchos de los mismos temas observados en ratones —control del citoesqueleto, señalización inmune y regulación metabólica— aparecían en redes génicas humanas centradas en MYO1C. Varios genes alterados en la grasa de ratones deficientes en NM1 también estaban integrados en estas redes humanas y se han asociado con la remodelación del tejido adiposo y el metabolismo. Esta superposición entre especies sugiere que mecanismos nucleares similares podrían influir en el riesgo de obesidad en humanos.
Qué significa esto para la obesidad y la salud metabólica
En conjunto, el trabajo muestra que NM1 es mucho más que un ayudante nuclear; es un nodo central que une la organización del ADN con la forma en que los adipocitos crecen, almacenan energía y se comunican con el sistema inmune. Cuando falta NM1, los interruptores génicos en los precursores de grasa se configuran mal, las mitocondrias funcionan de forma deficiente, los adipocitos se agrandan en lugar de multiplicarse y la grasa visceral se inflama: una combinación que se parece a la grasa poco saludable observada en la obesidad y la resistencia a la insulina. Para el lector general, el mensaje es que la disposición física del ADN y sus ayudantes dentro del núcleo puede predisponer a los tejidos hacia una expansión adiposa saludable o dañina. Proteínas como NM1 y su homóloga humana MYO1C podrían algún día convertirse en dianas para terapias destinadas a remodelar el tejido adiposo desde dentro, ofreciendo una forma más precisa de abordar las enfermedades relacionadas con la obesidad.
Cita: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Palabras clave: adipogénesis, cromatina, mitocondrias, grasa visceral, inflamación metabólica