Clear Sky Science · es
Macrófagos M2 fomentan la metástasis linfática regulando la translocación nuclear de PKM2 en cáncer de mama triple negativo
Por qué esta investigación importa
Para las personas diagnosticadas con cáncer de mama triple negativo, una de las mayores preocupaciones es que el tumor se disemine a los ganglios linfáticos cercanos, un paso clave hacia la diseminación por todo el organismo. Este estudio profundiza en cómo ciertos glóbulos inmunitarios que deberían protegernos, en realidad ayudan a este tipo de cáncer de mama a invadir el sistema linfático, e identifica un «interruptor» molecular que podría dirigirse con fármacos para ralentizar o detener esa diseminación.
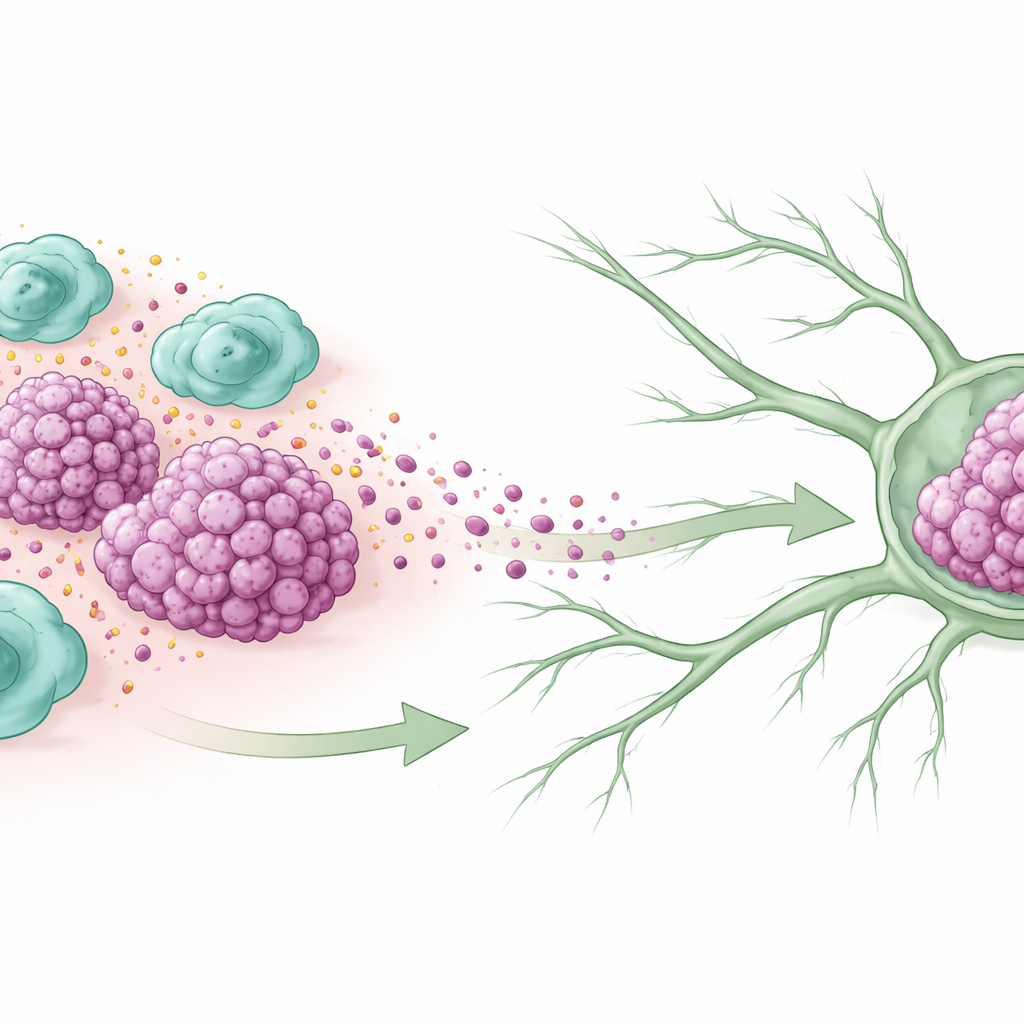
Ayudantes inmunitarios convertidos en cómplices
En el interior de muchos tumores, células inmunitarias llamadas macrófagos se acumulan en gran número. Algunas adoptan un estado reparador y de curación de heridas conocido como M2, que en el contexto del cáncer a menudo termina ayudando a los tumores en lugar de combatirlos. Los investigadores examinaron tejidos de mujeres con cáncer de mama triple negativo y hallaron que los tumores que ya se habían extendido a los ganglios linfáticos contenían muchos más macrófagos de tipo M2. Las pacientes cuyos tumores estaban repletos de estas células tendían a tener cánceres más grandes, características más agresivas y supervivencia más corta, lo que sugiere que estas células inmunitarias de «fuego amigo» están estrechamente vinculadas al empeoramiento de la enfermedad.
Construyendo nuevas «autopistas» linfáticas para las células cancerosas
Las células cancerosas no suelen alcanzar los ganglios linfáticos por casualidad; a menudo viajan a lo largo de vasos linfáticos recién formados, pequeños conductos que drenan líquido de los tejidos. En este estudio, los tumores ricos en macrófagos M2 también presentaban más de estos vasos linfáticos entretejidos. En placas de cultivo, cuando las células de cáncer de mama se cultivaron en presencia de macrófagos M2, liberaron señales que hicieron que células linfáticas humanas formaran redes tubulares y migraran más rápido, imitando el crecimiento de nuevos conductos linfáticos. En ratones, las células cancerosas preexpuestas a macrófagos M2 produjeron más vasos linfáticos en el tumor y metástasis más frecuentes a ganglios linfáticos cercanos, confirmando que estas células inmunitarias ayudan activamente a construir rutas de escape.
La cadena de señales oculta dentro de las células cancerosas
El equipo preguntó luego qué mensajes químicos envían los macrófagos M2 para empujar a los tumores hacia la diseminación linfática. Identificaron una molécula bien conocida, el TGF-β, que se libera en mayores cantidades por los macrófagos M2. Esta señal provocó que las células de cáncer de mama aumentaran la producción de dos factores de crecimiento, VEGFC y VEGFD, potentes impulsores del crecimiento de vasos linfáticos. De manera crucial, los investigadores demostraron que una enzima metabólica dentro de las células cancerosas, PKM2, actúa como un interruptor central en este proceso. Bajo la estimulación por TGF-β, PKM2 no solo potencia la maquinaria de consumo de azúcar de la célula, sino que también se modifica químicamente y se desplaza al núcleo, donde contribuye a activar los genes de VEGFC y VEGFD. Sin PKM2, o cuando se bloqueó su entrada al núcleo, las células cancerosas produjeron mucho menos de estas señales promotoras de vasos linfáticos y tuvieron menor capacidad para estimular la formación de vasos linfáticos.
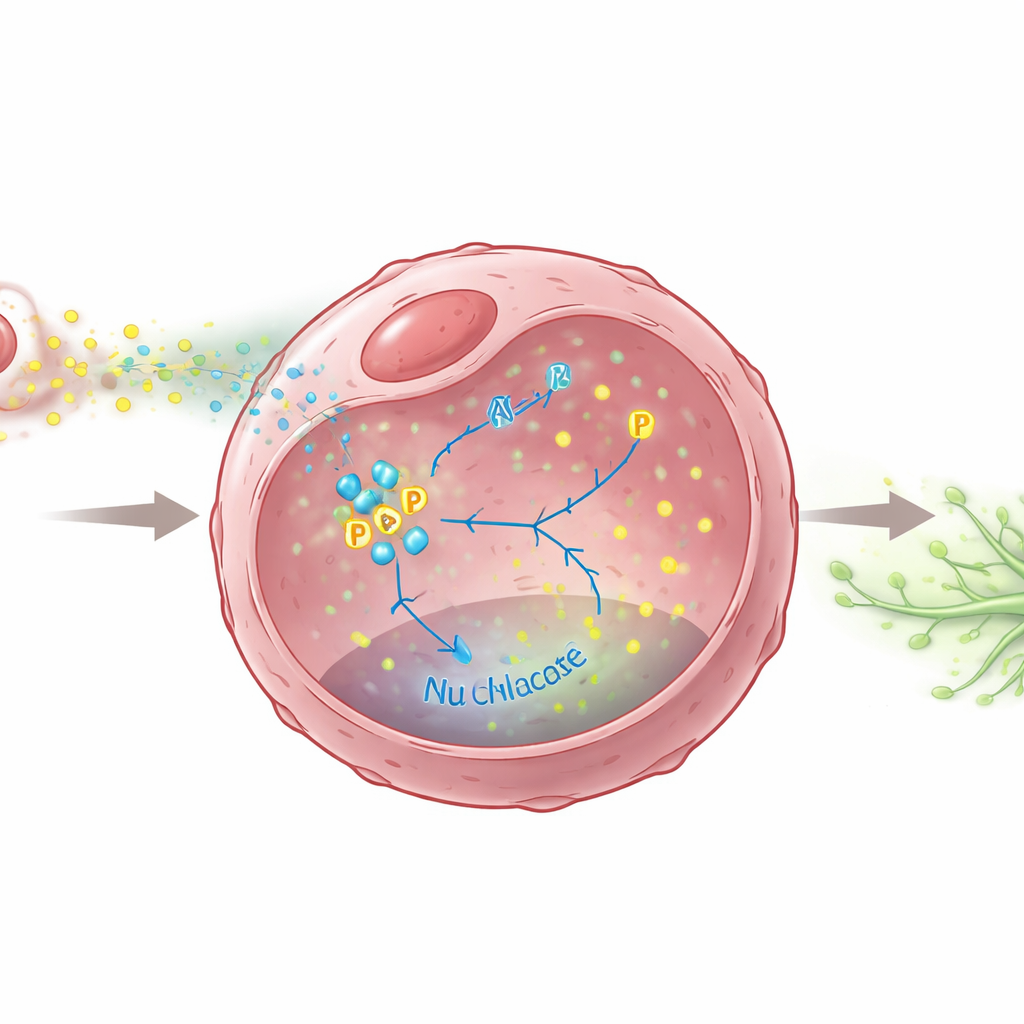
Probando un posible freno a la diseminación
Dado que PKM2 ocupa esta intersección crucial entre el metabolismo alterado y la señalización pro-metastásica, los científicos probaron si inhibirla podría ralentizar la diseminación linfática. Utilizaron shikonina, un compuesto que interfiere con la activación de PKM2 y su entrada al núcleo. En experimentos celulares, la shikonina redujo de forma marcada los niveles de VEGFC y VEGFD y debilitó la capacidad de las secreciones de las células cancerosas para inducir el crecimiento y la migración de vasos linfáticos. En modelos de ratón, el tratamiento con shikonina disminuyó el número y el tamaño de las metástasis en ganglios linfáticos y redujo la densidad de vasos linfáticos dentro de los tumores, sin efectos tóxicos evidentes en los animales. Estos hallazgos sugieren que bloquear PKM2 puede, a la vez, privar a las células cancerosas de algunas ventajas metabólicas y amortiguar su capacidad para remodelar la red linfática a su favor.
Lo que esto significa para los pacientes
En conjunto, el estudio propone una cadena de eventos clara: los macrófagos M2 en tumores de cáncer de mama triple negativo secretan TGF-β, que convierte a PKM2 dentro de las células cancerosas en un elemento de doble función: impulsar un alto consumo de azúcar y actuar en el núcleo para activar VEGFC y VEGFD. Estos factores, a su vez, estimulan el crecimiento de vasos linfáticos que las células cancerosas utilizan para alcanzar los ganglios linfáticos y más allá. Al identificar a PKM2 como un punto crítico en esta cadena, el trabajo sugiere nuevas vías para predecir y tratar potencialmente la diseminación linfática, especialmente en pacientes cuyos tumores muestran altos niveles de macrófagos M2, PKM2 o VEGFC/D. Aunque se necesitan más ensayos en humanos, dirigir esta vía podría ayudar a convertir el sistema linfático de una autopista para el cáncer de nuevo en una barrera.
Cita: Yang, Y., Ye, H., Zhong, D. et al. M2 macrophages promote lymphatic metastasis by regulating PKM2 nuclear translocation in triple-negative breast cancer. Cell Death Dis 17, 262 (2026). https://doi.org/10.1038/s41419-026-08524-4
Palabras clave: cáncer de mama triple negativo, metástasis en ganglios linfáticos, macrófagos asociados al tumor, PKM2, linfangiogénesis