Clear Sky Science · es
La trimetilación de lisina 36 en la histona H3 por SETD2 configura un paisaje epigenético en las células madre intestinales para orquestar el metabolismo lipídico y atenuar la senescencia celular
Por qué importan las células madre intestinales a medida que envejecemos
En lo profundo del revestimiento de nuestros intestinos, diminutas células madre trabajan sin descanso para renovar el tejido que nos ayuda a digerir los alimentos y absorber nutrientes. A medida que envejecemos, estas células madre se agotan, lo que hace que el intestino sea más vulnerable a enfermedades y más lento para sanar. Este estudio explora cómo pequeñas marcas químicas en las proteínas que empaquetan el ADN ayudan a mantener jóvenes a las células madre intestinales, cómo su pérdida altera la quema de grasas dentro de las células y cómo fármacos escogidos con cuidado podrían algún día ralentizar este declive.
Células envejecidas en un entorno exigente
La superficie interna del intestino es uno de los tejidos que más rápidamente se renueva en el cuerpo. Las células madre, ubicadas en la base de pequeñas cavidades llamadas criptas, se dividen para reemplazar miles de millones de células cada pocos días. Este trabajo constante requiere un suministro de energía estable, buena parte del cual proviene de la descomposición de grasas. Al mismo tiempo, estas células madre están reguladas por un código “epigenético”: marcas químicas en proteínas histona que ayudan a determinar qué genes están activos o silenciados. Los autores se centraron en una de esas marcas, conocida como trimetilación de H3K36, creada por una enzima llamada SETD2, y se preguntaron si los cambios en esta marca podrían ayudar a explicar por qué las células madre intestinales pierden vigor con la edad.
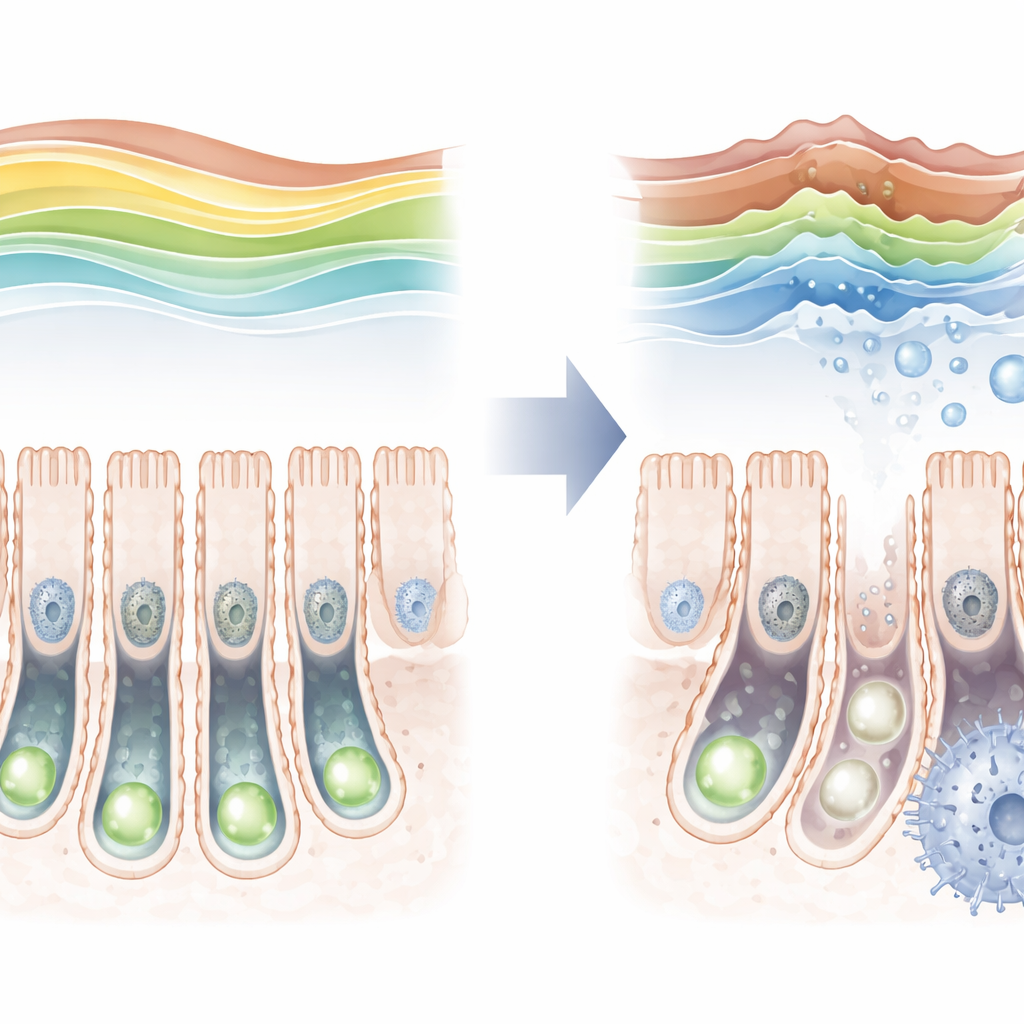
Una marca protectora que se desvanece con la edad
Al examinar intestinos de ratón a lo largo de su vida, los investigadores hallaron que la marca de trimetilación de H3K36 no es estática. Es relativamente baja justo después del nacimiento, luego aumenta hasta un pico en la adultez joven antes de caer de nuevo en la vejez. A medida que esta marca disminuía en animales mayores, los marcadores de envejecimiento celular aumentaban en las células madre, lo que sugiere un vínculo entre ambos. Para probar esto de forma más directa, el equipo diseñó ratones en los que SETD2 podía eliminarse solo en las células madre intestinales. Cuando se suprimió esta enzima, la marca protectora casi desapareció, las células madre se dividieron con menos frecuencia y tuvieron dificultades para producir la gama completa de tipos celulares especializados del intestino.
Cómo los cambios epigenéticos descarrilan la quema de grasas
La pérdida de esta única marca de histona desencadenó una cascada de cambios dentro de las células madre. Las mediciones de la actividad génica mostraron que muchos genes implicados en el ciclo celular y la replicación del ADN se silenciaron, mientras que genes vinculados al estrés y al envejecimiento se activaron. De forma llamativa, la señal más fuerte apuntó a un manejo alterado de los lípidos: los genes que normalmente apoyan la oxidación de ácidos grasos—la quema controlada de grasas para obtener energía—se vieron atenuados, y las grasas comenzaron a acumularse dentro de las criptas. El perfil metabolómico confirmó que se acumulaban ácidos grasos de cadena larga, señal de que las vías habituales de procesamiento de lípidos estaban fallando. Al mismo tiempo, el empaquetamiento físico del ADN en el núcleo cambió, con muchas regiones volviéndose más expuestas o más cerradas, remodelando qué genes podía usar la célula con facilidad.
Remodeladores de la cromatina y la marcha hacia la senescencia
Para entender cómo surgen estos cambios en el empaquetamiento del ADN, los autores cartografiaron tanto las regiones de cromatina abierta como un conjunto de otras marcas de histona a lo largo del genoma. Cuando se perdió la trimetilación de H3K36, tramos amplios de ADN ganaron marcas “activas” y se hicieron más accesibles, especialmente cerca de genes relacionados con el metabolismo y el envejecimiento. Un actor clave en esta transición fue el complejo remodelador de cromatina SWI/SNF, impulsado por una subunidad central llamada SMARCA4. En las células madre sin SETD2, los niveles de SMARCA4 aumentaron, y el complejo pareció ayudar a abrir regiones que activan programas de senescencia. Cuando los investigadores redujeron la actividad de SMARCA4 de forma genética o con un inhibidor específico, las células madre recuperaron parte de su capacidad para formar mini-intestinos saludables en cultivo, y disminuyeron los marcadores de envejecimiento—lo que sugiere que el remodelado excesivo empuja a estas células hacia un estado cansado y senescente.
Reactivar las vías energéticas para rescatar las células madre
Dado que la alteración de la quema de grasas surgió como un problema central, el equipo probó si potenciar esta vía podría contrarrestar el envejecimiento de las células madre. Usaron un fármaco que activa PPARα, un regulador maestro de la oxidación de ácidos grasos. En organoides cultivados a partir de células madre deficientes en SETD2, este tratamiento aumentó el crecimiento, restauró las yemas estructurales características de células madre vigorosas y redujo la acumulación de grasas. En ratones vivos, la misma intervención recompuso parcialmente la reserva de células madre, redujo los marcadores de senescencia y normalizó la acumulación lipídica en las criptas intestinales. Estos hallazgos sitúan la oxidación de ácidos grasos como un vínculo crucial entre el control epigenético y la salud de las células madre.
Qué significa esto para un envejecimiento saludable
En conjunto, el trabajo muestra que una marca específica de histona, depositada por SETD2, ayuda a mantener un paisaje epigenético equilibrado en las células madre intestinales. Cuando esta marca se desvanece, la cromatina se remodela de forma anómala, las vías de quema de grasas fallan, los lípidos se acumulan y las células derivan hacia la senescencia, debilitando el sistema de reparación intestinal. Al reducir la maquinaria de remodelado hiperactiva o restaurar el metabolismo lipídico con fármacos dirigidos, podría ser posible preservar la función de las células madre y la salud intestinal en edades avanzadas. Aunque estos hallazgos provienen de ratones, reflejan patrones observados en trastornos humanos del intestino, lo que sugiere la posibilidad de que terapias metabólicas cuidadosamente ajustadas puedan algún día ayudar a contrarrestar el declive relacionado con la edad en nuestras propias células madre intestinales.
Cita: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Palabras clave: células madre intestinales, epigenética, oxidación de ácidos grasos, senescencia celular, SETD2