Clear Sky Science · es
Un ARN vinculado a Lamp2a secretado por ADSC evita la retroalimentación ENO1–lactilación–glucólisis y el comportamiento maligno celular en el cáncer de mama triple negativo
Por qué esto importa para los pacientes
El cáncer de mama triple negativo es una de las formas más agresivas de la enfermedad y carece de los dianas hormonales o de factores de crecimiento que hacen que otros subtipos sean más tratables. Este estudio revela cómo estos tumores reconectan su uso de energía para sobrevivir en entornos con poco oxígeno y describe una forma ingeniosa de atacar esa reconexión. Para los lectores, ofrece una visión de cómo comprender el metabolismo del cáncer puede conducir a terapias nuevas y muy dirigidas que difieren marcadamente de la quimioterapia tradicional.
Cómo se alimentan estos tumores
Muchos cánceres dependen en gran medida de una vía rápida pero ineficiente de producción de energía llamada glucólisis, que convierte la glucosa en el subproducto lactato. Al examinar muestras de pacientes, bases de datos genómicos públicas y varias líneas celulares de cáncer de mama, los investigadores muestran que los tumores triple negativos se apoyan en la glucólisis aún más que otros cánceres de mama. Una enzima clave en esta vía, ENO1, está presente en niveles especialmente altos en estos tumores y se asocia con peores tasas de supervivencia. Cuando se redujeron los niveles de ENO1 en células triple negativas cultivadas en el laboratorio, las células cambiaron la producción energética desde la glucólisis hacia una producción mitocondrial más normal, crecieron más despacio y tuvieron menor capacidad para invadir o formar colonias.
Un bucle de retroalimentación peligroso dentro de las células cancerosas
Al profundizar, el equipo descubrió que el propio lactato refuerza ENO1 y atrapa a las células cancerosas en un ciclo vicioso. El lactato puede modificar químicamente proteínas en un proceso llamado lactilación. En las células triple negativas, el exceso de lactato aumentó la lactilación de ENO1, lo que a su vez potenció la actividad y la estabilidad de la enzima, acelerando aún más la glucólisis y produciendo más lactato. En condiciones de bajo oxígeno—típicas de tumores sólidos—este bucle se fortaleció, ayudando a las células cancerosas a resistir la muerte celular y a seguir proliferando. Bloquear la actividad de ENO1 con un inhibidor de pequeña molécula, o reducir la producción de lactato, debilitó este bucle, frenó la glucólisis y ralentizó el crecimiento tumoral en ratones.
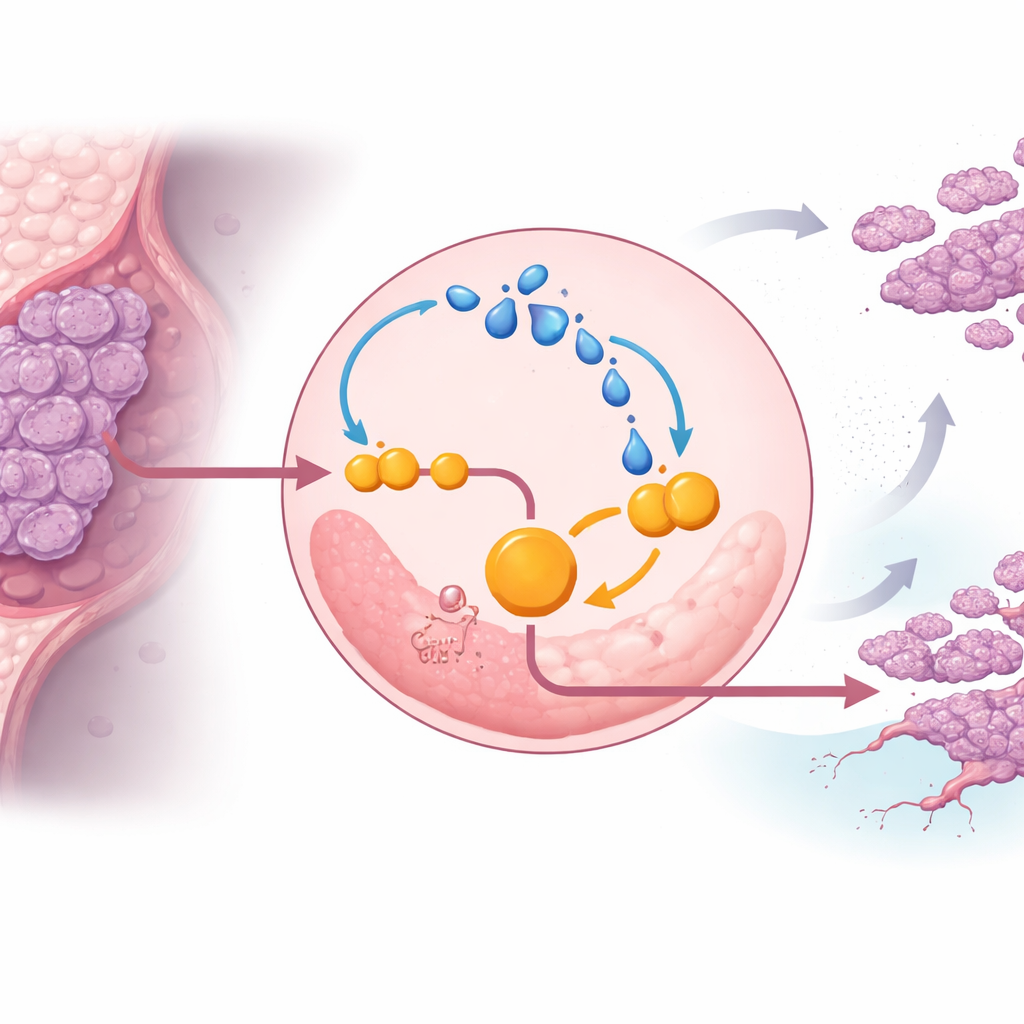
El interruptor molecular que protege ENO1
El estudio identificó un punto de control específico en ENO1 que hace posible este bucle. Una proteína conocida como EP300 añade marcas basadas en lactato a varios sitios de lisina en ENO1, siendo uno de esos sitios, denominado K262, crucial. Cuando este sitio se mutó para que ya no pudiera ser lactilado, ENO1 fue rápidamente dirigido a los centros de reciclaje celular, los lisosomas, y degradado. Sin esta marca protectora, las células triple negativas perdieron gran parte de su impulso glucolítico y su capacidad para formar tumores y metástasis en modelos animales. Esto señala la lactilación de ENO1 en K262 como un interruptor molecular que protege la enzima de la destrucción y mantiene el metabolismo alterado del cáncer.
Una nueva forma de marcar ENO1 para su destrucción
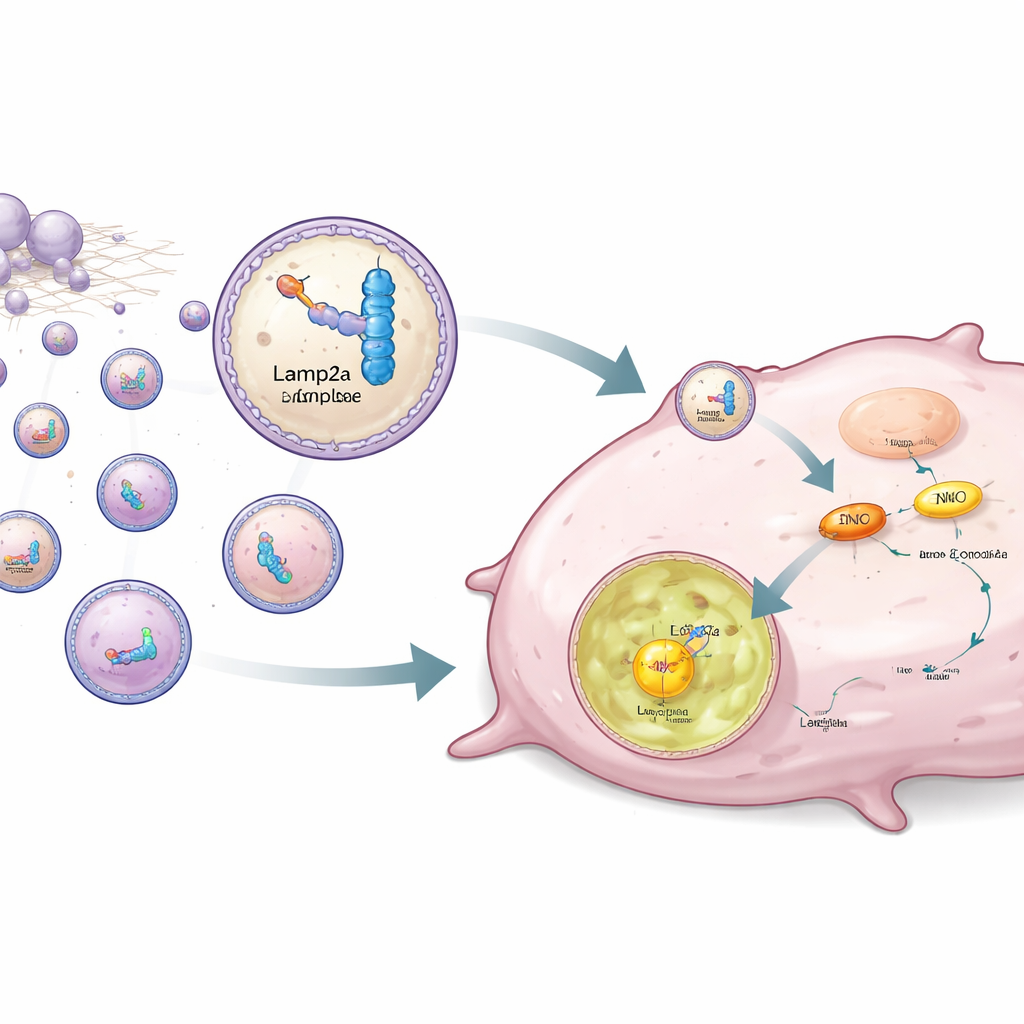
En lugar de limitarse a bloquear ENO1, los autores diseñaron una estrategia para eliminarlo selectivamente de las células cancerosas. ENO1 también actúa como una proteína que se une al ARN, reconociendo secuencias cortas específicas. El equipo diseñó fragmentos de ARN sintéticos que se unen fuertemente a ENO1 y los vinculó a Lamp2a, una proteína de la membrana lisosomal implicada en la degradación proteica dirigida. Células madre derivadas de tejido adiposo humano fueron modificadas genéticamente para producir este par ARN–Lamp2a y empaquetarlo en pequeñas vesículas llamadas exosomas. Cuando estos exosomas modificados se añadieron a células triple negativas, la porción de ARN se aferra a ENO1, mientras que la parte Lamp2a guía todo el complejo hacia los lisosomas, donde ENO1 se degrada incluso si lleva la marca de lactilación estabilizadora.
Probar el enfoque de degradación dirigida en animales
Para acercar esta idea a una terapia práctica, los investigadores cultivaron las células madre modificadas sobre un andamiaje biodegradable e implantaron este constructo bajo la piel de ratones, cerca de tumores triple negativos. Desde esta ubicación, las células madre liberaron continuamente exosomas que portaban los complejos dirigidos a ENO1. Los tumores en estos ratones mostraron niveles de proteína ENO1 notablemente más bajos, menor glucólisis, menos células en división y más señales de muerte celular en comparación con los animales control. Los tumores crecieron más despacio y su comportamiento maligno se atenuó claramente, demostrando que dirigir ENO1 hacia los lisosomas puede privar efectivamente al cáncer de su vía energética preferida.
Qué podría significar esto para tratamientos futuros
Para un público no especialista, la conclusión es que este trabajo revela tanto una vulnerabilidad como un nuevo ángulo de tratamiento para el cáncer de mama triple negativo. La vulnerabilidad es la dependencia del tumor de un circuito energético autorreforzado centrado en ENO1 y el lactato, especialmente en regiones con poco oxígeno. El ángulo terapéutico es un sistema de degradación proteica dirigido que utiliza ARN a medida y exosomas derivados de células madre para arrastrar ENO1 hacia la maquinaria de eliminación celular. Aunque aún está lejos del uso clínico, este enfoque ilustra cómo una comprensión profunda de los trucos metabólicos del cáncer puede inspirar terapias precisas que buscan desarmar, en lugar de simplemente envenenar, las células malignas.
Cita: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Palabras clave: cáncer de mama triple negativo, metabolismo del cáncer, señalización del lactato, degradación proteica dirigida, enzima ENO1