Clear Sky Science · es
La fosfatasa Shp1 regula la estabilidad de la proteína CXCR2 y la invasividad mediada por IL8 en el cáncer de mama
Por qué esta investigación importa para el cáncer de mama
El cáncer de mama sigue siendo una de las principales causas de muerte por cáncer en mujeres, en gran parte porque algunos tumores se vuelven invasivos y se diseminan a órganos distantes. Este estudio desentraña cómo una señal inflamatoria común en los tumores, llamada IL8, se comunica con las células de cáncer de mama y cómo un "freno" molecular llamado Shp1 ayuda a decidir si esas células permanecen en su lugar o se vuelven más agresivas. Comprender esta lucha molecular podría abrir nuevas vías para ralentizar o detener la diseminación de cánceres de mama difíciles de tratar, especialmente la enfermedad triple negativa.
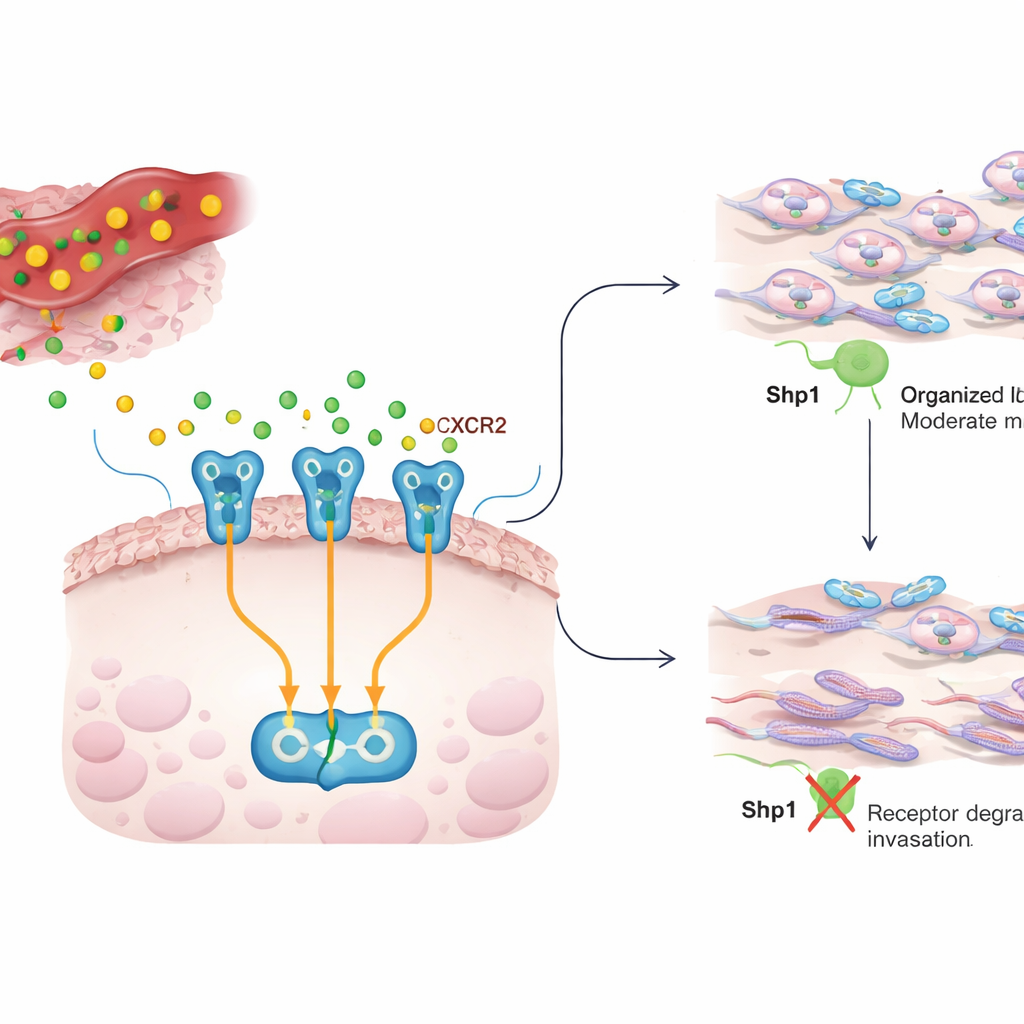
Una conversación entre la inflamación y las células cancerosas
Dentro de un tumor, las células cancerosas están rodeadas por células inmunes y de sostén que liberan mensajeros químicos, o citocinas. IL8 es uno de esos mensajeros y con frecuencia se encuentra en niveles altos en muchos cánceres, donde impulsa el crecimiento, la formación de vasos sanguíneos y la capacidad de las células cancerosas para moverse e invadir. IL8 señaliza a través de un receptor en la superficie de la célula cancerosa llamado CXCR2. Cuando IL8 se une a CXCR2, activa varios circuitos internos que reorganizan el esqueleto celular, ayudando a las células a desplazarse por el tejido y diseminarse. El trabajo actual pregunta cómo se mantiene bajo control esta conversación IL8–CXCR2 y si Shp1, una enzima que suele actuar como un freno supresor de tumores sobre las señales de crecimiento, también modula este comportamiento invasivo.
El papel oculto de Shp1 en el movimiento celular
Los investigadores primero eliminaron o bloquearon químicamente Shp1 en una línea celular de cáncer de mama luminal ampliamente usada (MCF7) y midieron la capacidad de las células para migrar e invadir a través de un gel que imita el tejido. Sin Shp1, las células cancerosas cerraron las heridas más rápido y atravesaron el gel con una eficiencia dos o tres veces mayor, revelando que Shp1 normalmente contiene el movimiento. Usando datos de pacientes, también encontraron que las mujeres cuyos tumores expresaban menos Shp1 tenían una supervivencia peor y un tiempo más corto antes de la recaída. En conjunto, estos resultados sugieren que Shp1 limita el comportamiento agresivo de las células de cáncer de mama y que perder este freno está vinculado a peores resultados.
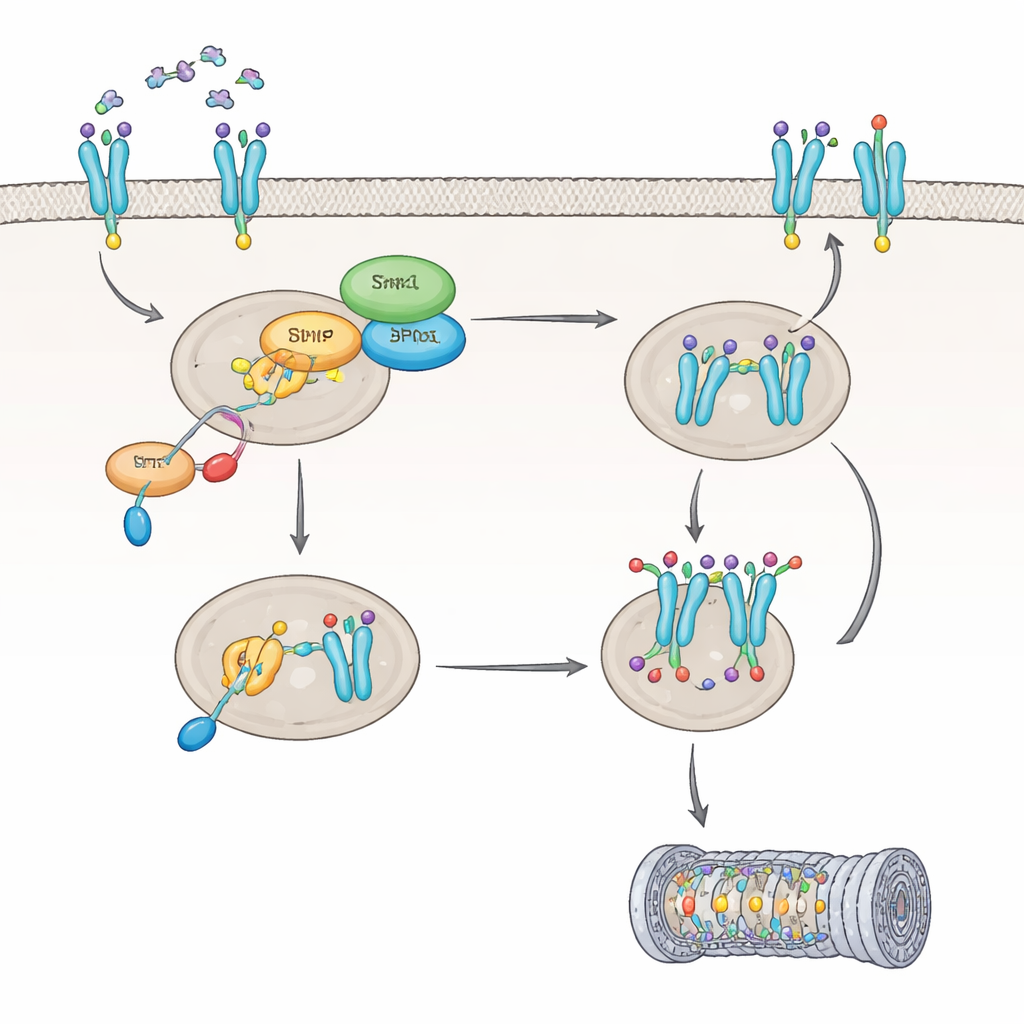
Cómo IL8 apaga el interruptor de Shp1 y reprograma un receptor clave
A continuación, el equipo exploró cómo IL8 afecta a Shp1. Descubrieron que IL8 activa una proteína llamada PKC, que marca a Shp1 en un sitio específico, reduciendo su actividad enzimática en aproximadamente un 60 por ciento. Cuando Shp1 queda atenuado de esta forma, otra enzima, PP2A, se vuelve menos activa, y el receptor CXCR2 permanece en un estado altamente modificado que cambia su destino dentro de la célula. En lugar de ser limpiado y reciclado de vuelta a la superficie celular, CXCR2 queda etiquetado para su destrucción, principalmente vía la maquinaria de degradación proteica de la célula, el proteasoma. Una modificación particular en CXCR2, en un aminoácido llamado Ser347, resultó crucial para la unión de estas marcas de degradación. En células sin Shp1, CXCR2 presentaba más etiquetas y se degradaba más rápidamente, conduciendo a menos receptores en la superficie celular y a una respuesta atenuada a IL8 con el tiempo.
Diferentes tipos de cáncer de mama, diferentes conexiones
El cáncer de mama no es una sola enfermedad; los tumores se agrupan en subtipos luminal, HER2-positivo y triple negativo según sus patrones de receptores. Los investigadores probaron el circuito IL8–CXCR2–Shp1 en varias líneas celulares que representan cada subtipo. En células luminales y triple negativas, IL8 activó la cascada Shp1–PP2A–CXCR2, y bloquear Shp1 aumentó tanto la invasividad basal como anuló el efecto pro-invasivo habitual de IL8. En contraste, las células HER2-positivas aún respondieron a IL8, pero el bloqueo de Shp1 apenas cambió su comportamiento, lo que sugiere que en estos tumores Shp1 está ocupado con otras señales, como HER2, y tiene menos disponibilidad para regular CXCR2. Los análisis a gran escala de expresión génica respaldaron este panorama: las líneas triple negativas tendían a tener menor Shp1, señalización relacionada con GPCR alterada y niveles más altos de IL8, coherente con un perfil más agresivo impulsado por la inflamación.
Qué significa esto para tratamientos futuros
Para un público no especializado, el mensaje central es que la enzima Shp1 actúa como un controlador de tráfico para el receptor de IL8, CXCR2, determinando si el receptor se reutiliza o se destruye y, a su vez, cuán intensamente pueden responder las células de cáncer de mama a las señales inflamatorias. En los cánceres de mama luminales y triple negativos, este punto de control parece especialmente relevante: cuando los niveles de Shp1 son bajos o su actividad está bloqueada, las células se vuelven más invasivas y los resultados para las pacientes empeoran. Dado que Shp1 puede potenciarse o modularse mediante ciertos fármacos existentes, dirigir el eje Shp1–CXCR2, posiblemente junto con bloqueadores de IL8 o CXCR2, podría ofrecer una nueva estrategia para limitar la invasión y la metástasis en subtipos de cáncer de mama agresivos.
Cita: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Palabras clave: invasión del cáncer de mama, señalización de IL8, receptor CXCR2, fosfatasa Shp1, cáncer de mama triple negativo