Clear Sky Science · es
CRMP2 inhibe la formación de metástasis al perjudicar la estabilización de ARNm de CXCL10 dependiente de ILF3 en el cáncer de mama
Por qué importa detener la diseminación del cáncer
La mayoría de las muertes por cáncer de mama no se deben al tumor original, sino a que las células cancerosas viajan a órganos vitales como los pulmones y forman nuevos crecimientos. Este estudio descubre una proteína protectora integrada dentro de las células de cáncer de mama que puede ralentizar o incluso bloquear esa diseminación al modificar la “alfombra de bienvenida” que los órganos distantes preparan para las células cancerosas errantes. Comprender este interruptor de seguridad oculto podría abrir la puerta a nuevos tratamientos que impidan que el cáncer arraigue en otras partes del cuerpo.
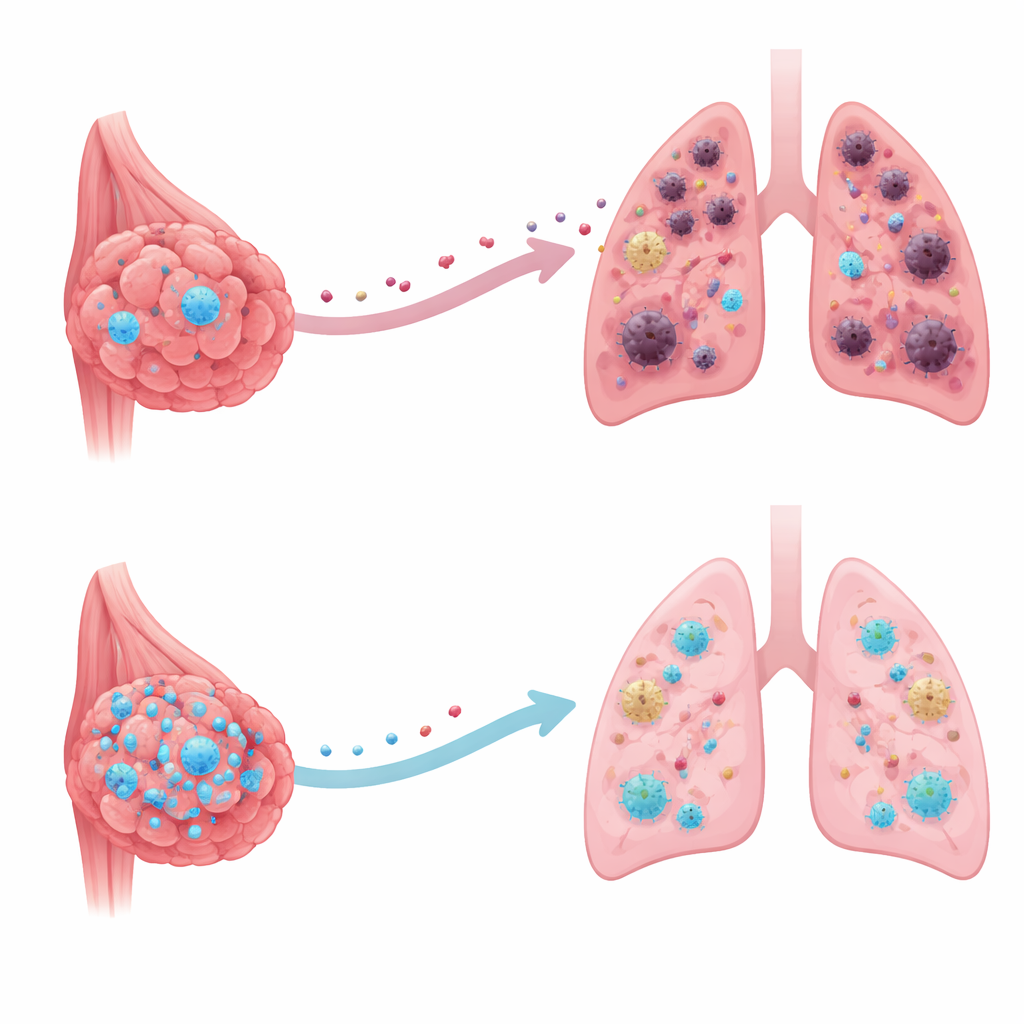
Un defensor silencioso dentro de las células cancerosas
Los investigadores se centraron en una proteína llamada CRMP2, conocida principalmente por ayudar a las neuronas a crecer y mantener su esqueleto interno. Al examinar grandes bases de datos públicas de cáncer y muestras tumorales de pacientes, encontraron que los niveles de CRMP2 eran inusualmente bajos en tumores de mama, especialmente en los cánceres que ya se habían diseminado. Los pacientes cuyos tumores conservaban cantidades más altas de CRMP2 tendían a vivir más tiempo y tenían menos probabilidades de desarrollar metástasis a distancia. Este patrón sugiere que CRMP2 actúa más como un freno que como un acelerador en el cáncer de mama, comportándose como un defensor interno en lugar de un impulsor de la enfermedad.
Cómo se preparan los pulmones para la invasión
Las células cancerosas rara vez llegan a un órgano distante por sorpresa. Mucho antes de su llegada, el tumor original libera moléculas que remodelan ese órgano en lo que los científicos llaman un “nicho premetastásico”: un microambiente que favorece la supervivencia del cáncer. Usando un modelo de ratón bien establecido que imita de cerca el cáncer de mama humano, el equipo mostró que cuando las células tumorales mamarias fueron diseñadas para producir CRMP2 adicional, los tumores primarios crecieron igual de rápido, pero los pulmones se volvieron mucho menos hospitalarios. Los marcadores de inflamación y de remodelado tisular en los pulmones disminuyeron, y se reclutaron menos las células inmunitarias que normalmente suprimen las defensas antitumorales. Como resultado, tras extirpar el tumor principal se formaron muchas menos nódulos metastásicos en los pulmones.
Una cadena de señalización que causa problemas
Indagando más a fondo, los científicos preguntaron qué señales secretadas por el tumor eran responsables de preparar los pulmones. Centraron su atención en CXCL10, una pequeña proteína mensajera (quimiocina) conocida por atraer determinadas células inmunitarias y por reactivar células cancerosas en estado latente. Tanto en células de cáncer de mama humanas y murinas cultivadas en laboratorio, aumentar CRMP2 redujo drásticamente la cantidad de CXCL10 producida y liberada. En ratones, los pulmones expuestos a material tumoral rico en CRMP2 mostraron niveles mucho más bajos de CXCL10 y menos células inmunitarias entrantes que normalmente deprimen la actividad protectora de las células T. Cuando los investigadores bloquearon CXCL10 con un anticuerpo, la colonización pulmonar por células cancerosas disminuyó; cuando añadieron CXCL10 extra, desapareció el efecto protector de CRMP2. Esto situó a CXCL10 claramente aguas abajo de CRMP2 como un instigador clave de un nicho favorable a la metástasis.
El intermediario oculto que estabiliza las señales perjudiciales
Puesto que CRMP2 vive dentro de las células mientras CXCL10 se secreta, el equipo sospechó la existencia de un intermediario molecular. Identificaron a ILF3, una proteína de unión a ARN, como un socio directo de CRMP2. ILF3 se une al ARN que codifica CXCL10 y normalmente lo protege de la degradación, permitiendo que se produzca más proteína CXCL10. CRMP2 se une a ILF3 en puntos de contacto específicos y lo marca para su destrucción a través del sistema de reciclaje de proteínas de la célula, acortando la vida útil de ILF3 y rompiendo su control sobre el ARNm de CXCL10. Cuando los niveles de CRMP2 son altos, ILF3 se degrada más rápido, el ARNm de CXCL10 se vuelve inestable y se secreta menos de la quimiocina inflamatoria. Cuando ILF3 se restauró de forma artificial, pudo anular la supresión de CXCL10 mediada por CRMP2, confirmando su papel como el eslabón crucial en esta cadena.
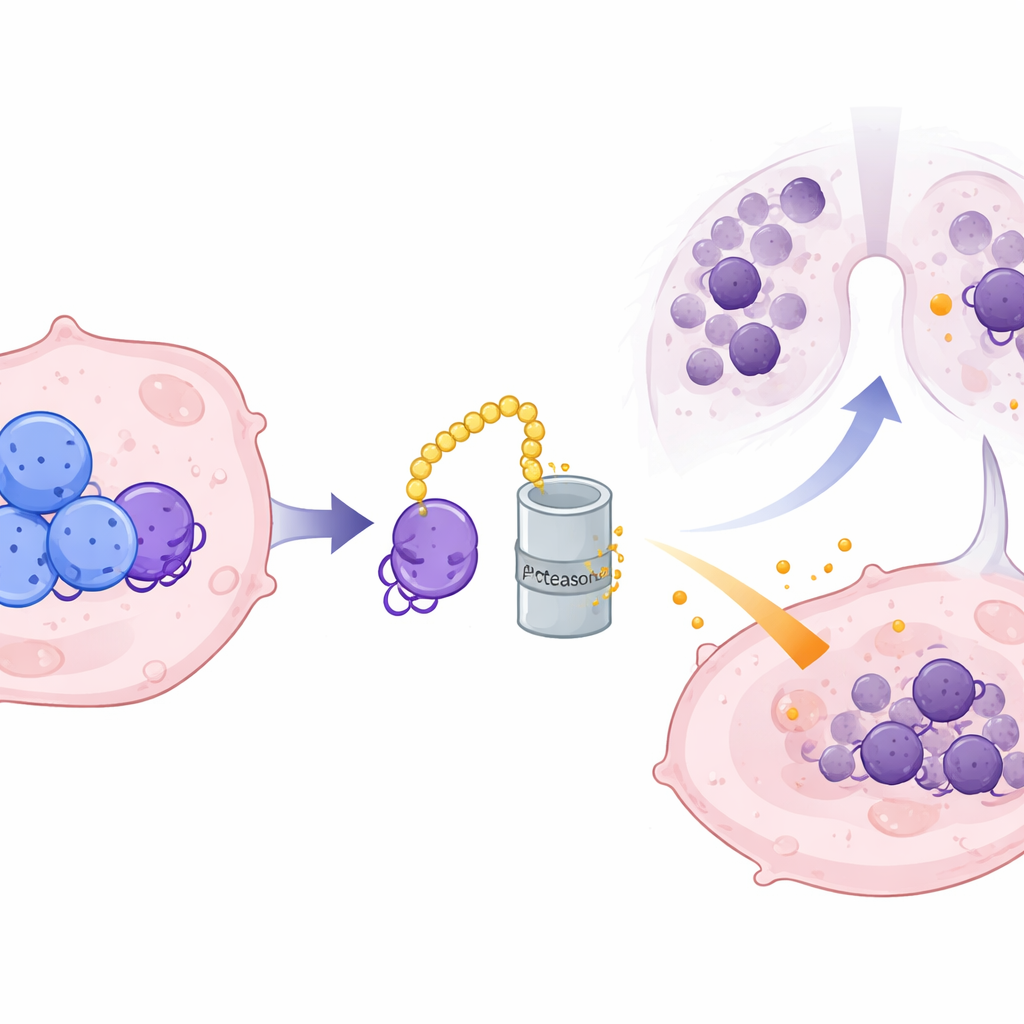
Convertir un compuesto vegetal en un posible aliado
Para probar si esta vía podía aprovecharse terapéuticamente, los investigadores cribaron una biblioteca de compuestos naturales y encontraron que la psoraleno —una molécula de origen vegetal usada desde hace tiempo en tratamientos cutáneos— se une directamente a CRMP2 y lo estabiliza. En experimentos celulares, la psoraleno elevó los niveles de CRMP2, disminuyó ILF3 y CXCL10, y redujo el comportamiento invasivo de las células de cáncer de mama sin dañar su viabilidad general. En múltiples modelos de ratón, la psoraleno no redujo los tumores mamarios primarios, pero sí disminuyó de forma notable las metástasis pulmonares y atenuó la formación del nicho premetastásico, nuevamente de una manera dependiente de CRMP2. Aunque la psoraleno puede causar toxicidad hepática y necesitará ser refinada, estos resultados muestran que pequeñas moléculas pueden potenciar el papel protector de CRMP2.
Qué significa esto para los pacientes
En conjunto, este trabajo revela un eje protector dentro de las células de cáncer de mama en el que CRMP2 desestabiliza ILF3, lo que a su vez reduce CXCL10 y evita que los pulmones se conviertan en terreno fértil para la metástasis. En lugar de atacar directamente a las células cancerosas, esta estrategia pretende desactivar los nichos distantes de los que dependen, inclinando la balanza a favor de las propias defensas del organismo. Aunque queda mucho por hacer antes de que este enfoque llegue a la clínica, dirigir la vía CRMP2–ILF3–CXCL10 —posiblemente con fármacos similares a la psoraleno más seguros— ofrece un nuevo ángulo prometedor para impedir la diseminación del cáncer de mama.
Cita: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Palabras clave: metástasis de cáncer de mama, nicho premetastásico, señalización de quimiocinas, proteínas de unión a ARN, terapéuticos derivados de productos naturales