Clear Sky Science · es
CCL11 promueve la recidiva del carcinoma hepatocelular tras la cirugía al potenciar macrófagos M2-like inmunosupresores CCR5 + CD206 + y favorecer la invasividad tumoral
Por qué el cáncer de hígado puede regresar después de la cirugía
La cirugía hepática suele ser la mejor esperanza para las personas con cáncer de hígado en estadio temprano, pero muchos pacientes ven cómo su cáncer reaparece en pocos años. Este estudio plantea una pregunta simple pero crucial: ¿la propia respuesta inflamatoria del organismo a la cirugía ayuda, de forma involuntaria, a que las células cancerosas residuales crezcan y se diseminen? Los investigadores se centran en una molécula de señalización llamada CCL11 y muestran cómo un aumento de esta molécula tras la cirugía puede tanto debilitar la inmunidad anticancerígena como volver a las células tumorales sobrevivientes más agresivas.
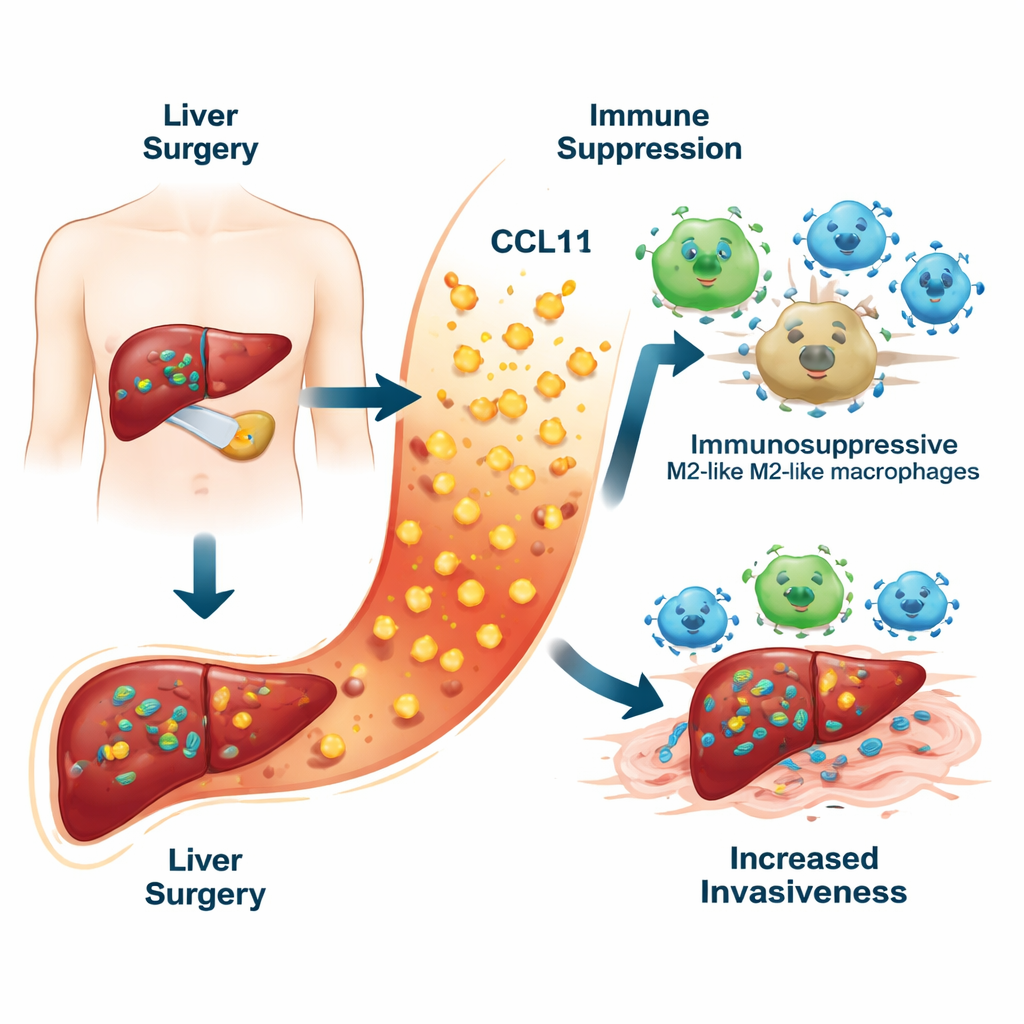
Un peligro oculto en la respuesta de curación
Cuando los cirujanos extirpan un tumor hepático, deben pinzar vasos sanguíneos e lesionar el tejido circundante. Este daño desencadena una ola de inflamación que ayuda al hígado a sanar. Midiendo diez moléculas inflamatorias diferentes en la sangre de los pacientes una semana después de la cirugía, el equipo encontró que una quimioquina, CCL11, destacaba. Los pacientes cuyo cáncer hepático recidivó más tarde tenían niveles de CCL11 significativamente más altos que aquellos que permanecieron libres de cáncer. Los niveles elevados de CCL11 también se asociaron con una peor supervivencia. Al combinar CCL11 con datos clínicos rutinarios, como analíticas sanguíneas y características del tumor, construyeron una “tarjeta de puntuación” de riesgo que predijo la recurrencia a cinco años con mayor precisión que los modelos tradicionales.
El tejido hepático que parece normal también importa
La mayor parte de la atención en la investigación del cáncer se dirige al propio tumor, pero este estudio muestra que el tejido hepático “normal” circundante puede ser igual de importante. En muestras de más de 100 pacientes, CCL11 fue en realidad más alto en el hígado no tumoral que en los nódulos cancerosos o en hígados de donantes sanos. Los pacientes cuyo tejido hepático próximo producía más CCL11 tuvieron más probabilidades de presentar enfermedad avanzada, diseminación a distancia y recaída tras la cirugía. En modelos murinos que imitan la breve pérdida y restitución del flujo sanguíneo durante una operación, la lesión hepática elevó rápidamente los niveles de CCL11. Bajo condiciones de baja oxigenación en el laboratorio, las células que sostienen el hígado, como los miofibroblastos y las células endoteliales, también produjeron más CCL11, lo que sugiere que el estrés quirúrgico prepara el remanente hepático para convertirse en un entorno pro‑tumoral.
Cómo CCL11 convierte a los defensores inmunitarios en espectadores
Para ver cómo CCL11 moldea la inmunidad, los autores se centraron en los macrófagos, glóbulos blancos versátiles que pueden atacar a los tumores o protegerlos. Encontraron que en el tejido hepático no tumoral, niveles más altos de CCL11 iban de la mano con un subtipo de macrófagos que porta el marcador CCR5 y muestra un perfil M2‑like, favorable al tumor. En pacientes, los hígados ricos en estos macrófagos CCR5+ M2‑like se asociaron con una peor supervivencia. En cultivos celulares, añadir CCL11 impulsó la diferenciación de monocitos hacia este tipo de macrófago inmunosupresor, aumentando moléculas como PD‑L1 e IL‑10 y liberando otras señales que atraen y polarizan más células inmunitarias. Estos macrófagos condicionados por CCL11 promovieron entonces que linfocitos T ayudantes naïve se convirtieran en células T reguladoras, una población conocida por atenuar las respuestas antitumorales. Experimentos mecanísticos mostraron que CCL11 activa una cadena de señales dentro de los macrófagos que termina en la vía NF‑κB y en la producción de PD‑L1, ayudando a proteger a las células cancerosas del ataque inmunitario.
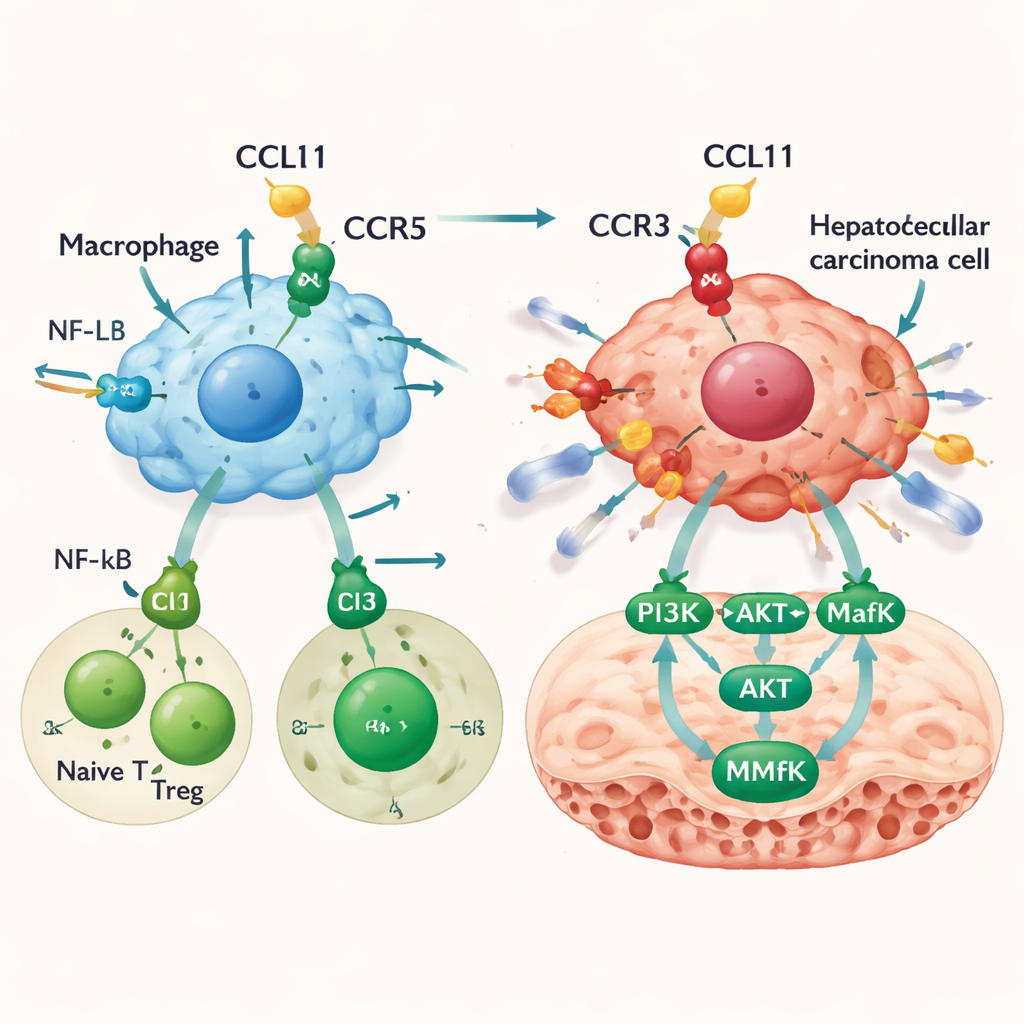
Cómo CCL11 hace que las células cancerosas residuales sean más invasivas
CCL11 no solo remodela el panorama inmune; también actúa directamente sobre las células del cáncer hepático. Aunque las células tumorales en sí producen poca CCL11, expresan uno de sus receptores, CCR3. En ensayos de laboratorio, CCL11 no aceleró la proliferación de las células de cáncer hepático, pero sí las hizo migrar e invadir barreras con mayor facilidad, una característica de potencial metastásico. Bloquear el receptor CCR3 eliminó en gran medida este efecto. Los análisis genéticos señalaron una vía en la que la señalización CCL11–CCR3 activa PI3K y AKT, que a su vez activan un factor de transcripción llamado MafK. MafK incrementa la producción de MMP13, una enzima que degrada el tejido circundante y abre rutas para la diseminación del cáncer. En modelos murinos, la infusión de CCL11 en el hígado aumentó la carga tumoral y llevó a más metástasis, junto con niveles más altos de la vía PI3K–AKT–MafK–MMP13 dentro de los tumores.
Convertir una señal de riesgo en una oportunidad terapéutica
Puesto que CCL11 parece tanto silenciar las defensas inmunitarias como fortalecer las células cancerosas residuales, los investigadores probaron si bloquearla tras la cirugía podría cambiar los resultados. En ratones con tumores hepáticos sometidos a resección quirúrgica, el tratamiento con un anticuerpo que neutraliza CCL11 redujo drásticamente la tasa de recurrencia en el hígado y mejoró la supervivencia, sin efectos secundarios evidentes como pérdida de peso. En conjunto, los hallazgos presentan a CCL11 como un interruptor maestro que enlaza la lesión quirúrgica con un entorno hepático inmunosupresor y favorable a la invasión. Para los pacientes, este trabajo sugiere que medir CCL11 después de la cirugía podría ayudar a identificar a quienes tienen mayor riesgo de recaída, y que fármacos dirigidos al eje CCL11–CCR5/CCR3 podrían algún día formar parte de estrategias para evitar la vuelta del cáncer de hígado.
Cita: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Palabras clave: recurrencia del cáncer de hígado, quimioquina CCL11, microambiente tumoral, supresión inmune, metástasis cancerosa