Clear Sky Science · es
El factor de transcripción ZMYM3 promueve la metástasis del carcinoma hepatocelular al regular al alza CTTN e inducir la formación de invadopodios
Por qué importa este estudio sobre el cáncer de hígado
El cáncer de hígado está entre los cánceres más letales del mundo, en gran parte porque a menudo se detecta tarde y tiene una fuerte tendencia a diseminarse. Este estudio examina tanto a nivel microscópico como en el núcleo celular una pregunta crucial: ¿qué hace que algunos tumores hepáticos sean tan eficaces para desprenderse e invadir otras partes del cuerpo? Al descubrir un impulsor molecular clave de esta propagación, la investigación apunta a nuevas vías para que los médicos, en el futuro, puedan predecir qué pacientes tienen mayor riesgo y diseñar tratamientos para frenar o detener la metástasis.
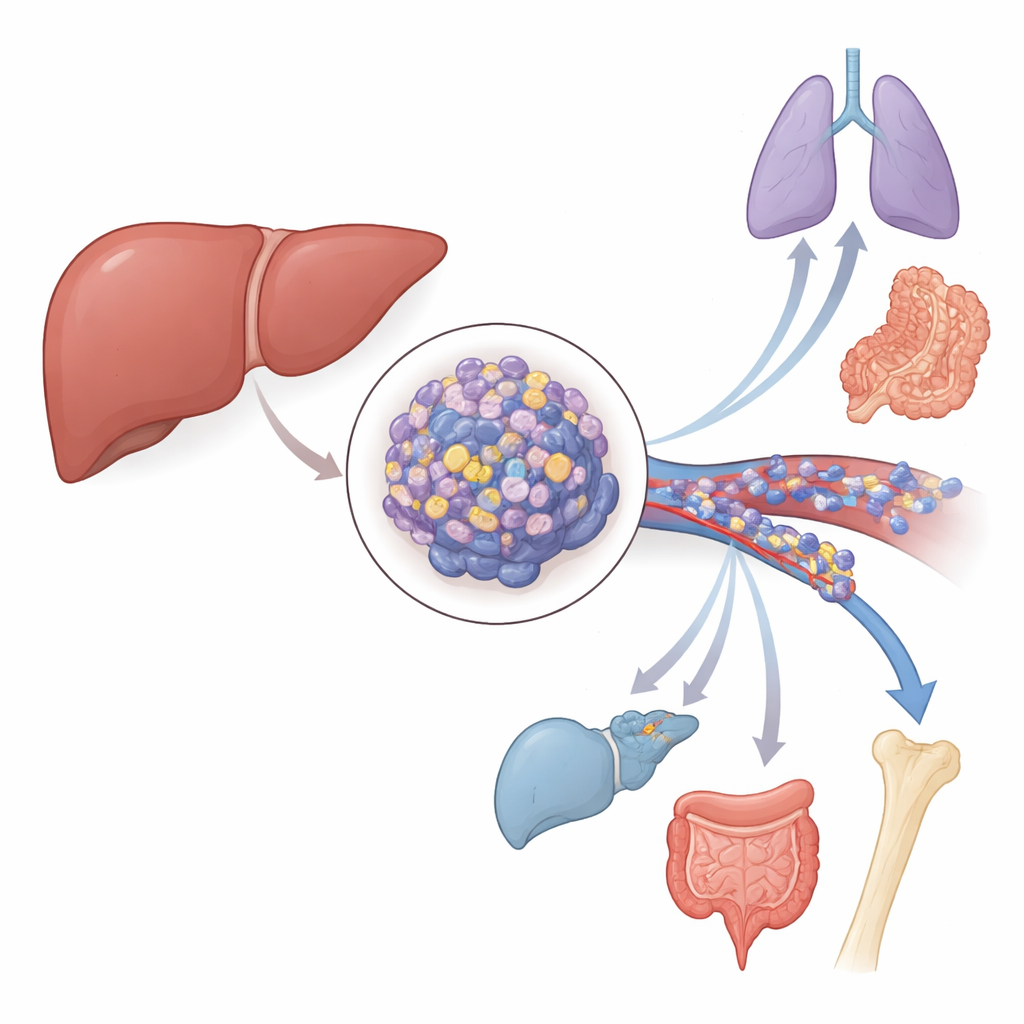
Un interruptor oculto dentro de los tumores hepáticos
Los investigadores se centraron en el carcinoma hepatocelular, el tipo más común de cáncer hepático primario. Mediante el análisis de grandes bases de datos públicas de cáncer y muestras de tejido de pacientes, encontraron que un gen llamado ZMYM3 está activado con mucha más intensidad en los tumores hepáticos que en el tejido hepático sano adyacente. Los pacientes cuyos tumores mostraban niveles más altos de ZMYM3 tendían a tener una supervivencia global peor y periodos libres de enfermedad más cortos. El equipo también examinó coágulos especiales formados por células tumorales dentro de la vena porta, un vaso sanguíneo principal que drena el hígado. En estos coágulos tumorales altamente invasivos, los niveles de ZMYM3 eran aún mayores que en los tumores hepáticos originales, vinculando estrechamente a este gen con la capacidad del cáncer para invadir vasos sanguíneos y diseminarse.
Cómo ZMYM3 hace que las células cancerosas sean más agresivas
Para ir más allá de las correlaciones, los científicos manipularon los niveles de ZMYM3 en líneas celulares de cáncer hepático. Cuando redujeron ZMYM3, las células crecieron más despacio, formaron menos colonias y fueron más propensas a sufrir muerte celular programada. Cuando aumentaron ZMYM3, ocurrió lo contrario: las células se dividieron más rápido, resistieron la muerte y mostraron mayor migración e invasión a través de barreras artificiales en el laboratorio. En modelos de ratón, los tumores diseñados para expresar ZMYM3 extra crecieron más bajo la piel y produjeron más nódulos metastásicos en los pulmones tras inyectarse en el torrente sanguíneo. En conjunto, estos experimentos muestran que ZMYM3 no es solo un marcador sino un promotor activo del crecimiento y la diseminación del cáncer de hígado.
Invadir mediante el crecimiento de pequeñas “patas”
Una característica llamativa de las células cancerosas agresivas es su capacidad para formar pequeñas protrusiones ricas en actina que excavan y disuelven el tejido circundante. Estas estructuras, llamadas invadopodios, actúan como martillos neumáticos celulares, ayudando a las células tumorales a abrirse paso a través de la matriz de soporte alrededor de los órganos y a entrar en los vasos sanguíneos. Mediante perfiles de expresión génica, visualización del esqueleto celular y ensayos funcionales, los investigadores demostraron que ZMYM3 aumenta muchos genes relacionados con los invadopodios y con un programa más amplio de cambio de forma conocido como transición epitelio-mesénquima, que hace a las células más móviles. Cuando los niveles de ZMYM3 eran altos, las células de carcinoma hepático formaban más invadopodios y aflojaban sus uniones con las células vecinas; al reducir ZMYM3, estas estructuras y comportamientos invasivos disminuían.
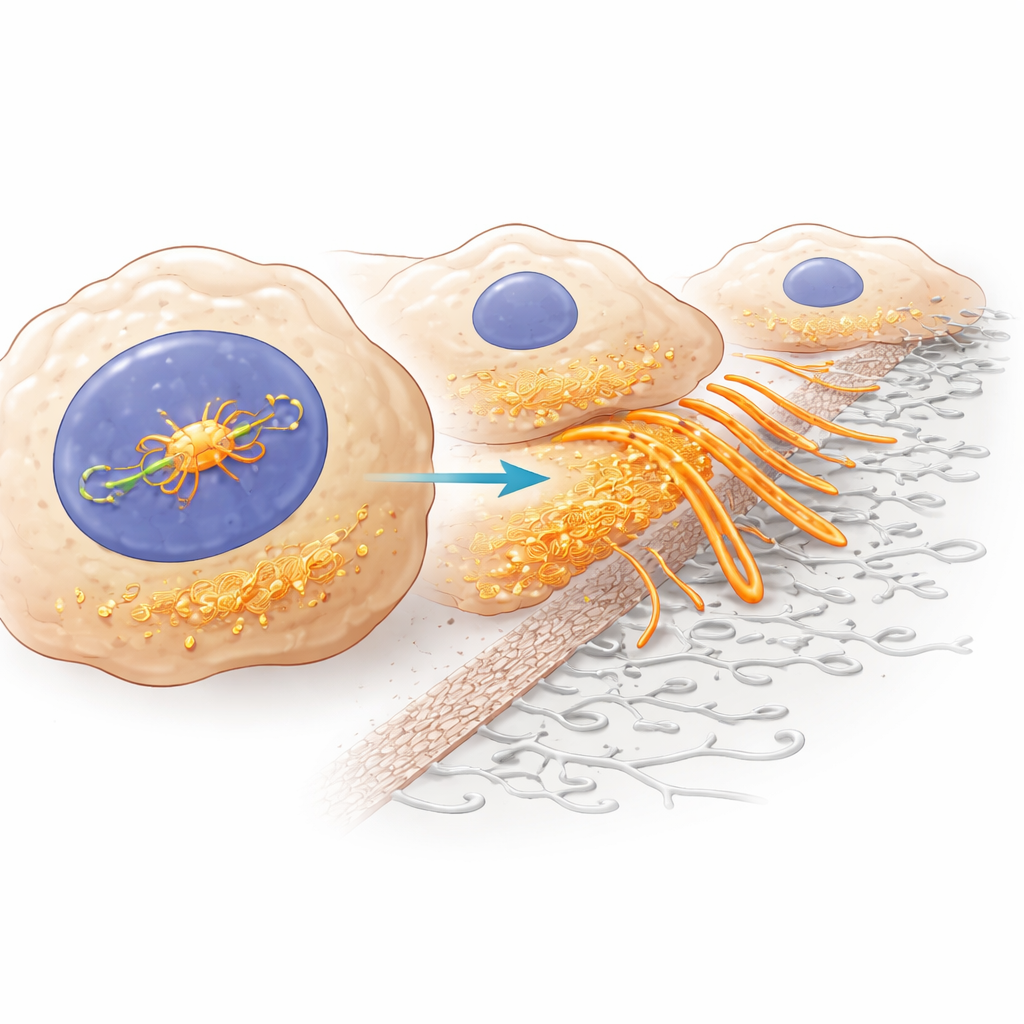
La pareja clave: una proteína andamiaje llamada cortactina
Profundizando en el mecanismo, el equipo empleó una técnica que mapea dónde se unen las proteínas al ADN en todo el genoma. Descubrieron que ZMYM3 se liga directamente a la región reguladora de otro gen, CTTN, que codifica la cortactina, un organizador central de los invadopodios. La activación de esta región aumenta la producción de cortactina. En datos de pacientes, la cortactina también estaba elevada en los tumores hepáticos y se asociaba con peores resultados, y sus niveles subían y bajaban en consonancia con ZMYM3. Cuando los científicos silenciaron la cortactina en células que sobreexpresaban ZMYM3, las células cancerosas perdieron gran parte de su exceso de crecimiento, supervivencia, migración e invasión. Esto demuestra que una gran parte del impacto de ZMYM3 se canaliza a través del aumento de cortactina y, a su vez, del refuerzo de los invadopodios.
Qué significa esto para los pacientes
Para un lector no especialista, la conclusión es que este estudio identifica un “acelerador” molecular —ZMYM3— que ayuda a las células del cáncer de hígado a crecer, resistir la muerte y perforar físicamente su camino hacia los vasos sanguíneos y órganos distantes. Lo hace en gran medida activando otro gen, CTTN, que dota a las células tumorales de unas “patas” invasivas más potentes. Dado que los niveles elevados de ZMYM3 y cortactina se asocian con recurrencia y peor supervivencia, podrían servir como señales de alerta para identificar a los pacientes con mayor riesgo de metástasis. A más largo plazo, fármacos que interfieran con esta vía ZMYM3–cortactina, o con la formación de invadopodios en sí, podrían ofrecer nuevas formas de frenar la diseminación del carcinoma hepatocelular y mejorar los resultados.
Cita: Zeng, F., Zhang, Z., Hu, T. et al. Transcriptional factor ZMYM3 promotes hepatocellular carcinoma metastasis by upregulating CTTN and inducing invadopodia formation. Cell Death Dis 17, 294 (2026). https://doi.org/10.1038/s41419-026-08506-6
Palabras clave: carcinoma hepatocelular, metástasis, ZMYM3, cortactina, invadopodios