Clear Sky Science · es
Los fibroblastos asociados al cáncer promueven la resistencia a osimertinib en células de cáncer de pulmón no microcítico mediante la modificación m7G de NET1 mediada por METTL1
Por qué algunos cánceres de pulmón dejan de responder a un fármaco “inteligente”
Fármacos dirigidos como osimertinib han transformado el tratamiento de muchas personas con un tipo común de cáncer de pulmón, ofreciendo más tiempo de vida con menos efectos secundarios que la quimioterapia tradicional. Sin embargo, para la mayoría de los pacientes estos beneficios son temporales: los tumores acaban encontrando maneras de eludir el fármaco. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿está el tejido que rodea al tumor —específicamente células llamadas fibroblastos asociados al cáncer— ayudando en silencio a las células cancerosas a escapar de los efectos de osimertinib?
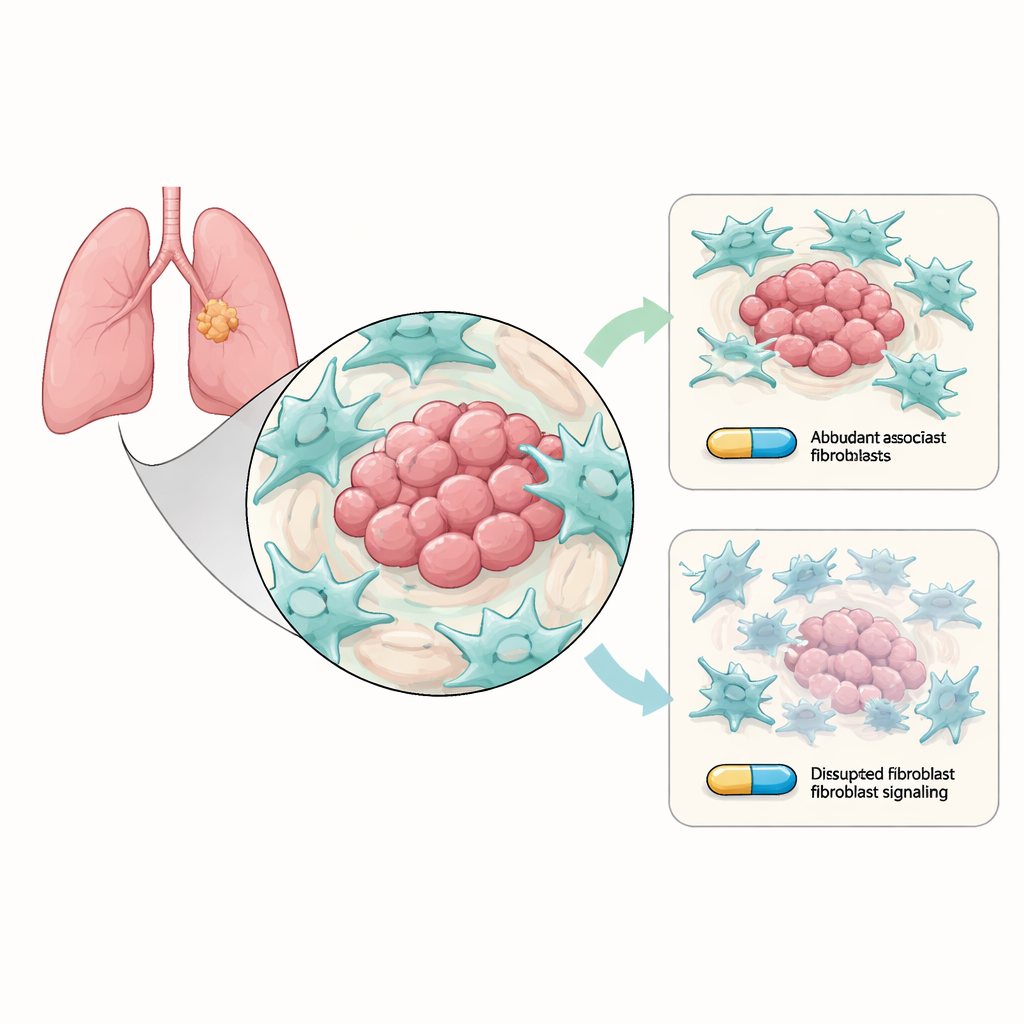
Células auxiliares que protegen al tumor en secreto
El cáncer de pulmón no microcítico crece dentro de un vecindario bullicioso de células no cancerosas conocido como microambiente tumoral. Entre los habitantes más abundantes están los fibroblastos asociados al cáncer (CAF), células del tejido conectivo que remodelan la zona alrededor del tumor. Los investigadores cultivaron células de cáncer de pulmón con las mutaciones habituales sensibles a osimertinib junto con CAF en el laboratorio. Encontraron que cuando los CAF estaban presentes, las células cancerosas eran más difíciles de eliminar con osimertinib: formaban más colonias, se autodestruían con menos frecuencia y mostraban rasgos más fuertes de “tipo madre” ligados a supervivencia a largo plazo y recidiva. En otras palabras, aunque el fármaco seguía apuntando a las células cancerosas, los fibroblastos circundantes las ayudaban discretamente a perdurar.
Una etiqueta química en el ARN que cambia las reglas
El equipo investigó más allá de los propios genes hasta las etiquetas químicas que decoran el ARN —las copias de trabajo de la información genética dentro de las células. Una de esas etiquetas, llamada m7G, puede influir en la estabilidad de una molécula de ARN y en la eficiencia con la que se traduce en proteína. Mediante pruebas bioquímicas y mapeo genómico, los investigadores demostraron que los CAF aumentan el marcado global m7G en los ARN dentro de las células de cáncer de pulmón. Este aumento se debía principalmente a una enzima metiltransferasa llamada METTL1, que coloca marcas m7G en los ARNm. Los niveles de METTL1 eran más altos en tumores pulmonares que en el tejido normal circundante y se asociaban con enfermedad más avanzada y peor supervivencia del paciente, lo que sugiere que esta enzima hace más que ajustar funciones celulares rutinarias.
Una señal secretada y una cadena molecular vulnerable
¿Cómo aumentan los CAF la expresión de METTL1 en las células cancerosas? El estudio señala a una proteína llamada HMGB1, que los CAF liberan a su entorno. En comparación con las células cancerosas, los CAF secretaban cantidades mucho mayores de HMGB1. Cuando los investigadores añadieron HMGB1 a células de cáncer de pulmón, aumentaron los niveles de METTL1 y las marcas m7G; cuando bloquearon HMGB1 en el medio condicionado por CAF, este efecto desapareció. Al indagar más, identificaron un ARN objetivo clave de METTL1: NET1, un gen que impulsa el crecimiento y la movilidad celular. Los CAF aumentaron tanto el marcado m7G como la abundancia del ARN y la proteína NET1, y METTL1 se unía físicamente al ARN de NET1 para estabilizarlo. Menos METTL1 significó menos NET1 modificado, señales de supervivencia celular más débiles y mayor sensibilidad a osimertinib.
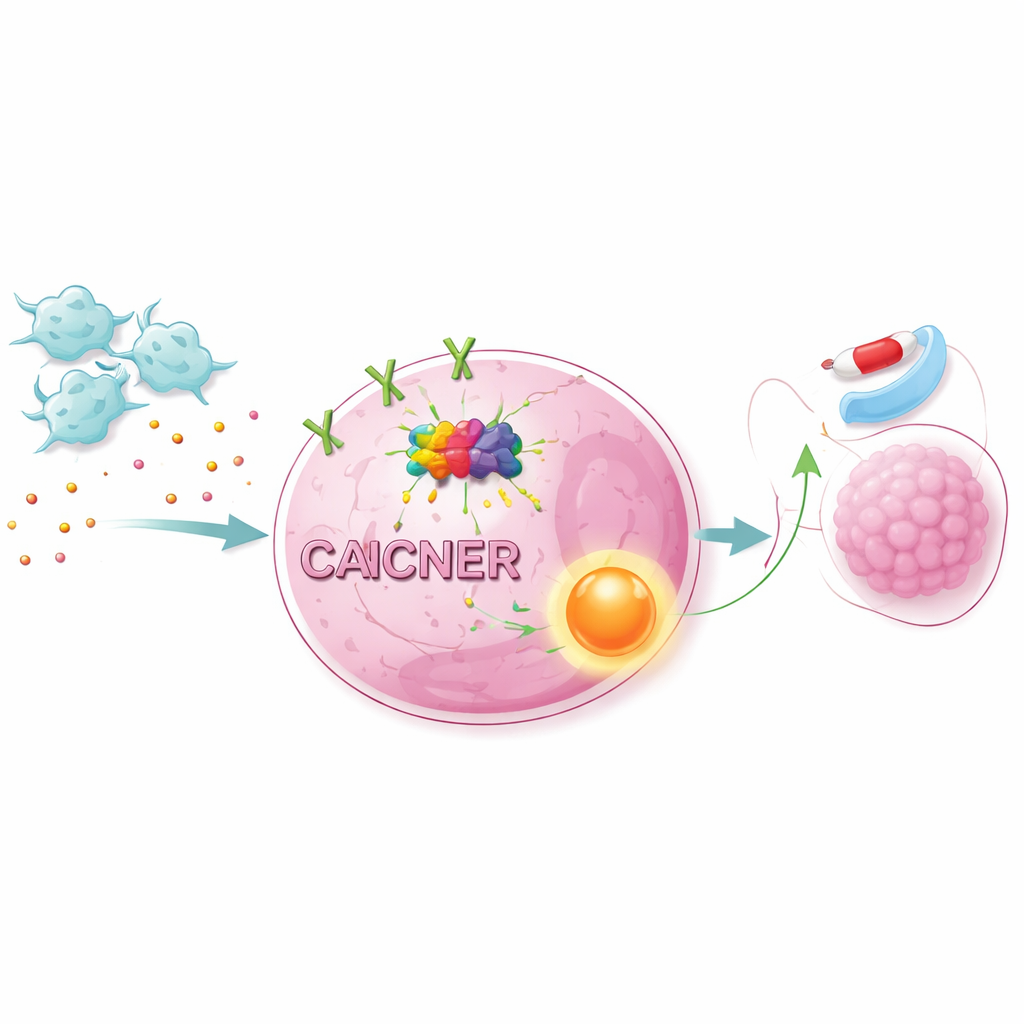
Activación de vías de supervivencia dentro de las células cancerosas
La señal reforzada de NET1 no actuó sola. Al combinar datos de ARN a gran escala con análisis de vías, los científicos mostraron que los CAF activan una ruta principal de crecimiento y supervivencia dentro de las células conocida como vía AKT/NF-κB. Bloquear AKT o NF-κB con inhibidores específicos hizo que las células de cáncer de pulmón fueran más vulnerables a osimertinib, incluso en presencia de CAF. Modificar los niveles de NET1 produjo efectos similares: reducir NET1 debilitó la protección conferida por los CAF, mientras que aumentar NET1 potenció la resistencia. En ratones implantados con células humanas de cáncer de pulmón, la adición de CAF hizo que los tumores crecieran más rápido y fueran menos sensibles a osimertinib. El silenciado de METTL1 en las células cancerosas redujo las marcas m7G, bajó NET1 y la activación de la vía, y disminuyó drásticamente el crecimiento tumoral impulsado por CAF.
Qué significa esto para el tratamiento futuro del cáncer de pulmón
Para las personas con cáncer de pulmón mutante en EGFR, este trabajo ofrece una nueva forma de entender por qué fármacos potentes como osimertinib acaban fallando. En lugar de culpar únicamente a nuevas mutaciones en las células cancerosas, destaca una cadena molecular que comienza fuera de la célula tumoral —con los CAF liberando HMGB1— y pasa por METTL1, las marcas m7G en NET1 y la activación de vías de supervivencia que amortiguan el impacto del fármaco. Interrumpir esta cadena en cualquier punto podría, en principio, restaurar o prolongar la sensibilidad al tratamiento. Aunque los fármacos que atacan directamente METTL1, HMGB1 o ARNm específicos marcados por m7G aún están en fases iniciales, el estudio sugiere que combinar osimertinib con terapias dirigidas a las células de soporte del tumor o sus señales modificadoras del ARN podría ayudar a mantener este tipo de cáncer de pulmón bajo control por más tiempo.
Cita: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Palabras clave: resistencia a osimertinib, cáncer de pulmón no microcítico, fibroblastos asociados al cáncer, metilación de ARN, vía METTL1 NET1