Clear Sky Science · es
La supresión de la autofagia impulsada por mTOR define una vulnerabilidad metabólica en el cáncer de mama HR+/HER2− resistente a inhibidores de CDK4/6
Por qué esto importa para las pacientes con cáncer de mama
Muchas mujeres con cáncer de mama avanzado viven ahora más tiempo gracias a fármacos llamados inhibidores de CDK4/6, que ralentizan la velocidad de división de las células tumorales. Desafortunadamente, la mayoría de los tumores acaban encontrando la forma de escapar a estos medicamentos. Este estudio aborda una pregunta esperanzadora: cuando el cáncer de mama se vuelve resistente a los fármacos CDK4/6, ¿adquiere una nueva debilidad que los médicos podrían explotar con medicinas metabólicas ya existentes y relativamente sencillas, como la metformina o el dicloroacetato (DCA)?
Cuando los fármacos contra el ciclo celular dejan de funcionar
Los médicos suelen tratar el tipo más común de cáncer de mama —enfermedad con receptor hormonal positivo y HER2 negativo— con terapia hormonal más inhibidores de CDK4/6 como palbociclib o ribociclib. Estos fármacos se dirigen a proteínas que empujan a las células a través del ciclo de división. Con el tiempo, sin embargo, algunas células cancerosas se adaptan y se vuelven fuertemente resistentes, continuando su crecimiento incluso en presencia de dosis altas de la droga. Los investigadores recrearon este problema en el laboratorio exponiendo líneas celulares de cáncer de mama (T47D y MCF7) a cantidades crecientes de inhibidores de CDK4/6. Terminaron con dos tipos de supervivientes: células parcialmente resistentes y un grupo más pequeño de clones altamente resistentes que ya no respondían bien al tratamiento.
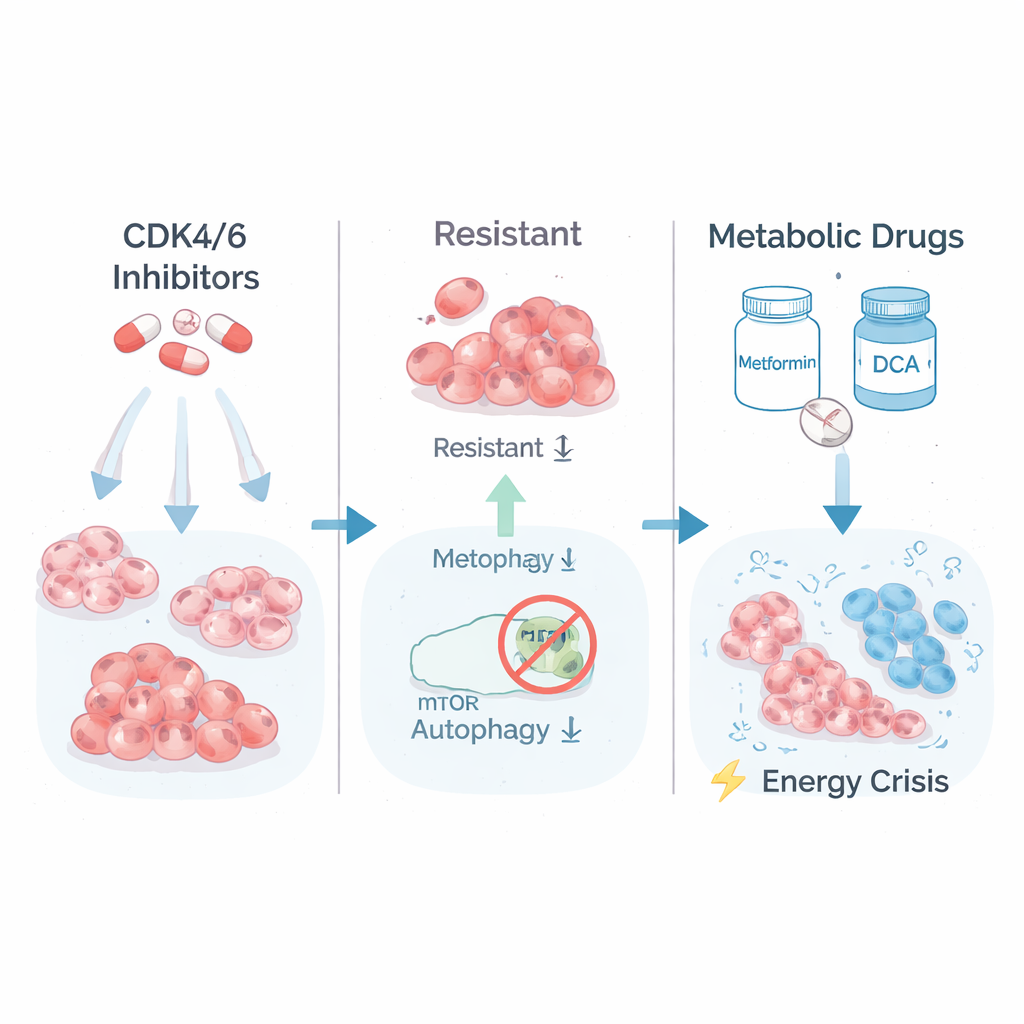
Una debilidad oculta en el uso de energía del tumor
Para entender qué hacía diferentes a las células altamente resistentes, el equipo examinó qué genes estaban activos o inactivos. Descubrieron que las células más resistentes habían aumentado las vías implicadas en la quema de azúcar (glucólisis) y en la señalización de crecimiento controlada por un complejo proteico llamado mTORC1. Dicho de otro modo, estas células vivían a toda marcha, consumiendo combustible a un ritmo alto para seguir creciendo. Los científicos probaron entonces si este metabolismo “a toda máquina” podía volverse en su contra. Trataron las células resistentes y las parentales con metformina, un fármaco antidiabético común que estresa las “centrales energéticas” de la célula, y con DCA, que obliga a las células a procesar el combustible de forma más eficiente. Sorprendentemente, los clones más resistentes a los fármacos fueron ahora los más vulnerables: su crecimiento a largo plazo en cultivos colapsó bajo el tratamiento metabólico, mientras que las células parentales y las solo parcialmente resistentes se vieron mucho menos afectadas.
Limpieza interna bloqueada y un colapso energético
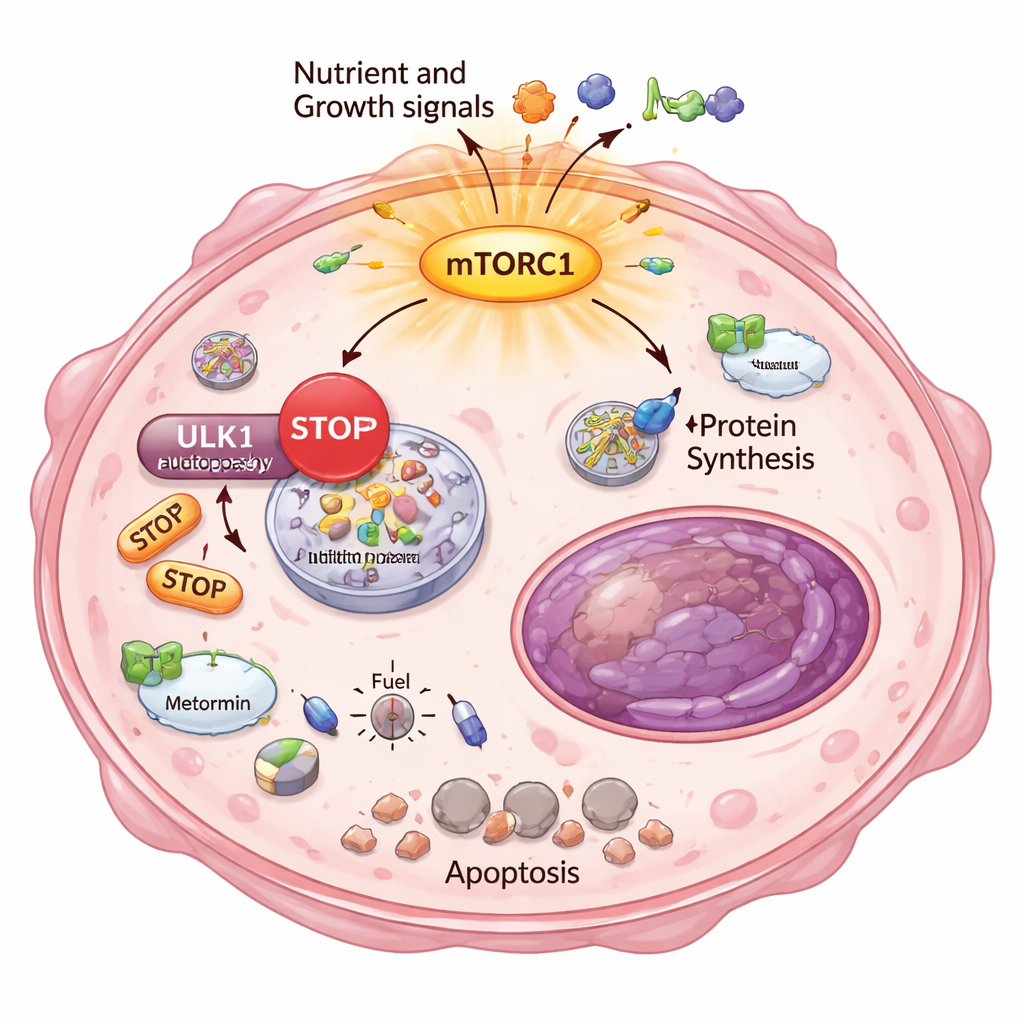
¿Por qué serían tan sensibles estas células cancerosas que escaparon al tratamiento frente al estrés energético? La respuesta residía en otro proceso básico de supervivencia: la autofagia, el sistema interno de “reciclaje y limpieza” de la célula. Normalmente, cuando la energía escasea, las células descomponen y reutilizan sus propios componentes para sobrevivir. Los investigadores demostraron que en los clones altamente resistentes mTORC1 estaba sobreactivado y ponía un freno químico sobre ULK1, un iniciador clave de la autofagia. Usando un ensayo reportero sensible, mostraron que estas células ya no podían activar ni aumentar la autofagia correctamente, ni siquiera al ser estimuladas con fármacos metabólicos. Como resultado, la metformina y el DCA provocaron una crisis energética severa: se activaron sensores de baja energía, se suprimió la producción de lípidos y aparecieron marcadores de muerte celular irreversible, específicamente en las células fuertemente resistentes.
Pruebas en tumores reales de pacientes
Los modelos de laboratorio no siempre reflejan lo que ocurre en los pacientes, por lo que el equipo se dirigió a muestras humanas de tumores de mama. Tiñeron más de cien cánceres buscando un marcador de actividad de mTORC1 (4E-BP1 fosforilada) y p62, una proteína que se acumula cuando la autofagia está bloqueada. Los tumores con alta actividad de mTORC1 tendían a tener más p62, lo que respalda la idea de que existe en tumores reales de mama —no solo en líneas celulares— un patrón de “señal de crecimiento sobreactivada más reciclaje deficiente”. Esto sugiere que un subconjunto de pacientes puede albergar tumores con la misma debilidad metabólica observada en el laboratorio.
Qué podría significar esto para tratamientos futuros
Para una persona no experta, el mensaje clave es que cuando los cánceres de mama evolucionan para escapar a fármacos potentes como los inhibidores de CDK4/6, también pueden encerrarse en una esquina metabólica. Al mantener las señales de crecimiento permanentemente activadas y apagar el reciclaje celular, estos tumores pasan a depender en gran medida de un suministro energético constante. El estudio muestra que esta configuración puede explotarse con medicinas metabólicas como metformina y DCA, ya bien conocidas en otras enfermedades. Importante: los autores proponen que pruebas simples en tejido para la actividad de mTORC1 y marcadores de autofagia podrían ayudar a identificar a las pacientes cuyos tumores resistentes están preparados para este tipo de ataque metabólico, abriendo la puerta a tratamientos de rescate más personalizados tras la falla de los inhibidores de CDK4/6.
Cita: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Palabras clave: cáncer de mama, resistencia a inhibidores de CDK4/6, mTOR, autofagia, terapia metabólica