Clear Sky Science · es
Conmutación de empalme del isoforma oncogénica BCS1L suprime la progresión del cáncer de ovario al alterar la función mitocondrial
Plantas de energía dentro de las células cancerosas
Cada célula de nuestro cuerpo depende de pequeñas plantas de energía llamadas mitocondrias. Las células cancerosas, que crecen y se diseminan con rapidez, tienen un apetito especial por la energía. Este estudio revela cómo el cáncer de ovario reconfigura uno de sus ayudantes mitocondriales clave y muestra que activar suavemente un “interruptor” molecular en ese ayudante puede privar de energía a los tumores mientras protege en gran medida los tejidos sanos.
Por qué los tumores dependen de sus motores
Las células de cáncer de ovario, como muchas cancerosas, pueden aprovechar distintas fuentes de energía con flexibilidad. Al examinar grandes bases de datos de pacientes y perfiles de una sola célula, los investigadores hallaron que muchos tumores ováricos ejecutan sus mitocondrias en un modo de alta marcha conocido como fosforilación oxidativa, u OXPHOS. Los tumores con esta actividad mitocondrial aumentada eran más agresivos y más frecuentes en enfermedad avanzada. Entre las muchas proteínas que ensamblan la maquinaria energética mitocondrial, destacó una: BCS1L, una chaperona que ayuda a montar el Complejo III, un núcleo central en la cadena energética celular. Los tumores con alta OXPHOS y ciertos subtipos celulares tumorales mostraron actividad especialmente intensa de BCS1L, lo que sugiere que las células cancerosas dependían mucho de este ayudante para mantener sus motores en funcionamiento.
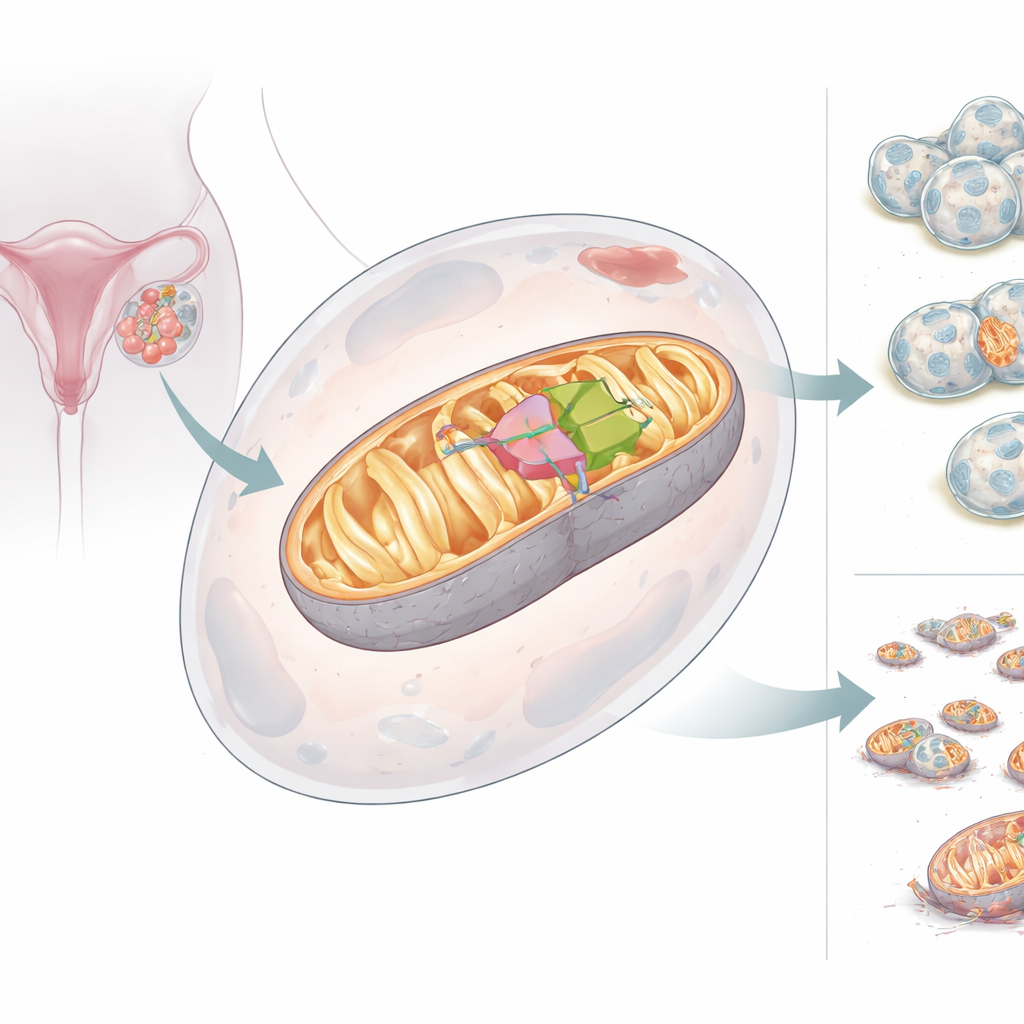
Dos caras de un ayudante mitocondrial
El equipo descubrió que el gen BCS1L puede producir dos versiones, u isoformas, de su proteína. La forma de longitud completa, BCS1L-L, lleva una etiqueta de localización que la envía a las mitocondrias, donde favorece el ensamblaje correcto del Complejo III y una alta producción de energía. La forma más corta, BCS1L-S, carece de un segmento clave y no puede llegar a las mitocondrias; en cambio, permanece en el citosol y en el núcleo y no apoya la producción de energía. En tejidos sanos la versión corta es habitual, pero en los cánceres de ovario el equilibrio cambia: predomina la forma larga, ligada a las mitocondrias. Cuando las células forzaron la producción de más BCS1L-L, sus mitocondrias generaron más energía, mantuvieron un mayor potencial de membrana, produjeron menos subproductos oxigenados dañinos y resistieron la muerte celular. Al reducir BCS1L, las mitocondrias se fragmentaron, la producción de energía cayó, aumentaron las moléculas oxidantes dañinas y las células cancerosas fueron más propensas a morir.
Cómo el cáncer reconfigura el mensaje
Producir la versión larga o corta de BCS1L depende de cómo la célula edita su mensaje de ARN, un proceso llamado empalme. Los investigadores buscaron proteínas que se unan al ARN de BCS1L e influyan en esa elección. Se centraron en USP39, un factor de empalme ya vinculado a varios cánceres. En células de cáncer de ovario, USP39 se une cerca del segmento de ARN que se convierte en el exón 2 de BCS1L y fomenta su inclusión, favoreciendo así la versión larga dirigida a las mitocondrias. Cuando se silenció USP39, las células omitieron ese segmento con mayor frecuencia, desplazándose hacia la forma corta BCS1L-S. Este cambio debilitó el Complejo III, redujo la respiración mitocondrial y la producción de ATP, aumentó el estrés oxidativo y desencadenó la muerte de células cancerosas. Restaurar BCS1L-L en estas células recuperó gran parte de la función mitocondrial y la supervivencia, demostrando que USP39 impulsa un interruptor mitocondrial crítico, en gran medida a través de BCS1L.
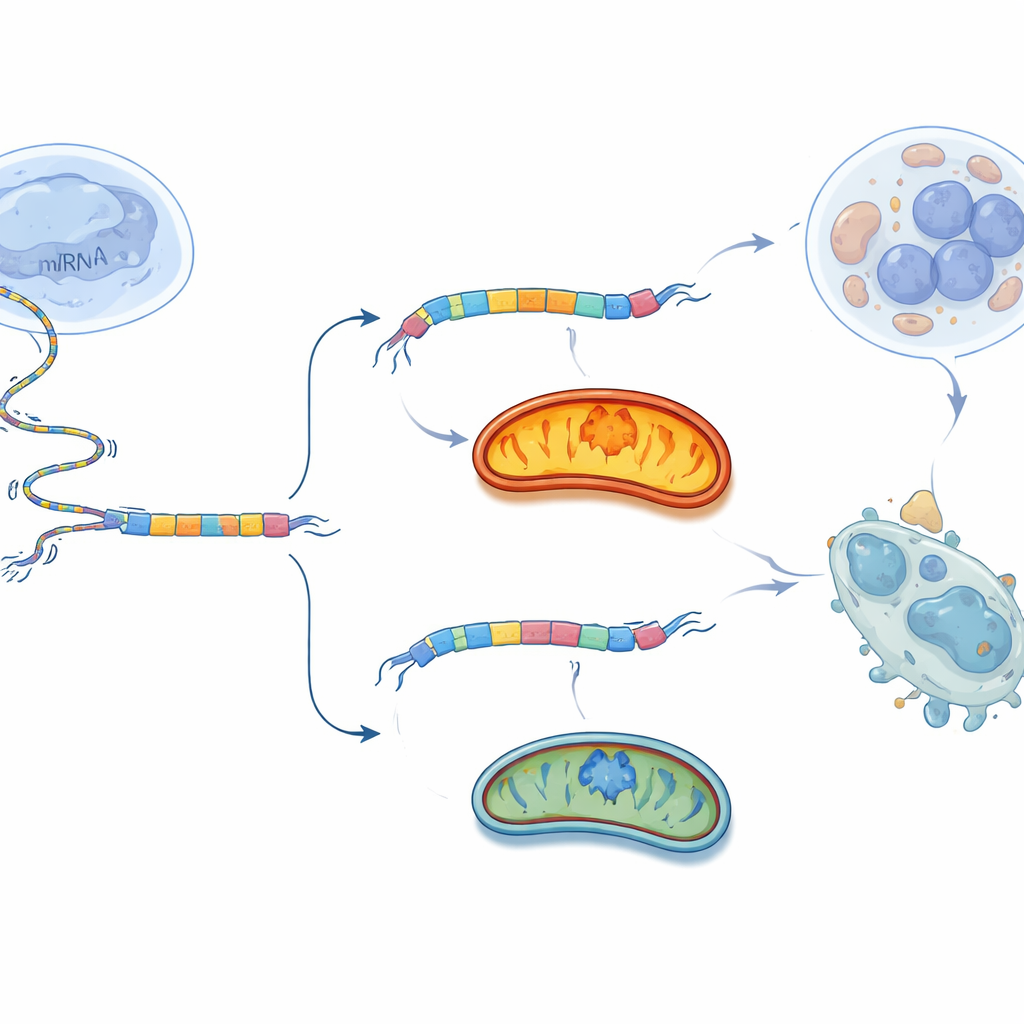
Girar el interruptor contra el tumor
En lugar de bloquear las mitocondrias de forma general, lo que podría dañar muchos tejidos, el equipo probó una táctica más quirúrgica: influir en la elección de empalme de BCS1L misma. Diseñaron fragmentos cortos de material genético llamados oligonucleótidos antisentido (ASO) que se unen justo alrededor del exón 2 del ARN de BCS1L. Estos ASO actúan como pequeñas pinzas, cambiando cómo la maquinaria de empalme lee el mensaje e incentivando a la célula a omitir el exón 2. En células de cáncer de ovario cultivadas en placa, el mejor ASO redujo fuertemente la forma larga BCS1L-L y aumentó la forma corta BCS1L-S. Como resultado, la respiración mitocondrial y la producción de ATP cayeron, los niveles de especies reactivas de oxígeno aumentaron y muchas más células entraron en muerte programada. Cuando el mismo ASO se inyectó en tumores de cáncer de ovario en ratones, el crecimiento tumoral se ralentizó y los tumores pesaron menos, con un efecto mucho más pronunciado sobre las células cancerosas que sobre fibroblastos normales.
Qué podría significar esto para los pacientes
En términos sencillos, este trabajo muestra que muchos cánceres de ovario dependen de una versión “turbo” de una proteína ayudante mitocondrial para alimentar su crecimiento. Un factor de empalme, USP39, inclina la maquinaria de edición del ARN de la célula para que se produzca más de esta versión turbo, manteniendo las plantas de energía del tumor en óptimas condiciones. Al usar ASO diseñados con precisión para revertir la elección de empalme hacia la versión más débil, los investigadores pueden dañar selectivamente las mitocondrias de las células cancerosas, desencadenando su muerte mientras dejan la mayoría de las células normales menos afectadas. Aunque la entrega de estos fármacos ASO a los tumores sigue siendo un desafío importante, este estudio apunta al interruptor de empalme de BCS1L como una diana prometedora y muy específica para tratar el cáncer de ovario.
Cita: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Palabras clave: cáncer de ovario, mitocondrias, empalme de ARN, BCS1L, oligonucleótidos antisentido