Clear Sky Science · es
PGC-1α protege frente a MASH mediante la inhibición dependiente de Tim23 de la ferroptosis mediada por DRP1
Por qué importa esto para la salud cotidiana
Muchas personas con obesidad o diabetes tipo 2 desarrollan sin saberlo un problema hepático grave llamado esteatohepatitis asociada a disfunción metabólica (MASH). En esta enfermedad, los hepatocitos cargados de grasa se inflaman y comienzan a morir, abriendo paso a la formación de cicatrices, cirrosis y cáncer de hígado. Este estudio descubre un sistema de autoprotección oculto dentro de las células hepáticas —centrado en las pequeñas centrales energéticas llamadas mitocondrias— que puede proteger al hígado del daño o, cuando falla, acelerar la enfermedad. Comprender este interruptor interno de seguridad podría abrir puertas a nuevos tratamientos para una de las amenazas hepáticas más comunes en todo el mundo.
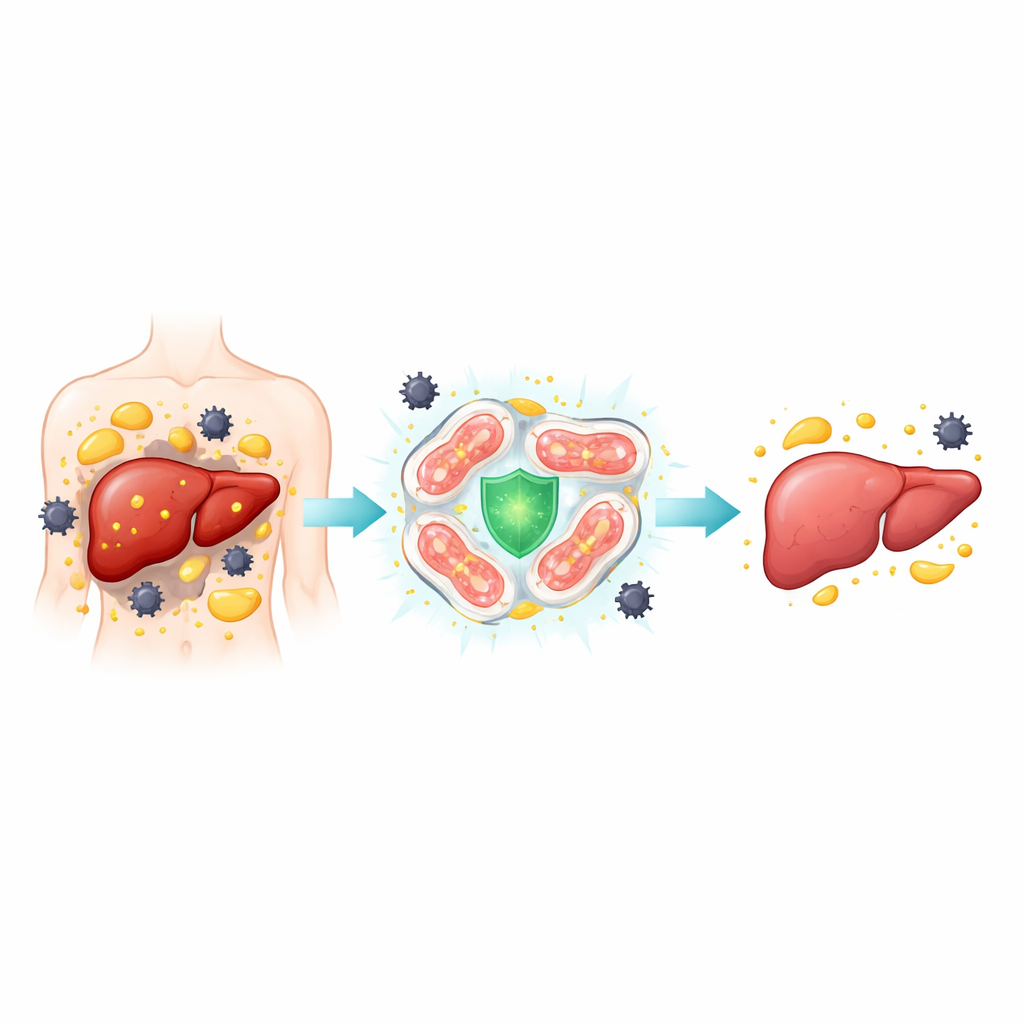
Una mirada más cercana a una enfermedad hepática silenciosa
La MASH se desarrolla cuando un hígado graso simple evoluciona hacia un estado más peligroso caracterizado por hepatocitos hinchados y lesionados, inflamación y, finalmente, tejido cicatricial. Los autores examinaron muestras de hígado de pacientes con MASH y de modelos de ratón alimentados con dietas ricas en grasa y azúcar o deficientes en nutrientes que imitan la condición humana. Se centraron en un tipo particular de muerte celular llamada ferroptosis, en la que el hierro y los lípidos dañados se combinan para generar moléculas tóxicas que perforan las membranas celulares. Tanto en personas como en ratones con MASH, las células hepáticas mostraron signos característicos de esta muerte impulsada por hierro y lípidos: depósitos excesivos de hierro, mitocondrias distorsionadas y altos niveles de proteínas que promueven el daño lipídico, junto con niveles bajos de proteínas que normalmente desintoxican los subproductos dañinos.
Pruebas de que bloquear la muerte por hierro ayuda
Para comprobar si la ferroptosis es solo un espectador o un impulsor de la enfermedad, los investigadores trataron a ratones con dieta alta en grasas con ferrostatina-1, un compuesto que bloquea específicamente la ferroptosis. Los ratones que recibieron el inhibidor tuvieron menos acumulación de grasa, menor sobrecarga de hierro y menos signos de inflamación y formación de cicatrices en el hígado. Los análisis de sangre mostraron una función hepática mejorada y mejor salud metabólica, incluida una reducción del colesterol y una mejor sensibilidad a la insulina. En hepatocitos aislados de ratón expuestos al ácido palmítico —una grasa que imita la sobrecarga observada en MASH— el mismo fármaco redujo la acumulación de grasa, la carga de hierro, el daño oxidativo y las señales inflamatorias. En conjunto, estos resultados sostienen que la ferroptosis es un motor clave del daño en la MASH y que interrumpir este proceso puede mitigar significativamente la enfermedad.
El guardián integrado del hígado dentro de las mitocondrias
El equipo se centró entonces en PGC-1α, un regulador maestro que ayuda a las mitocondrias a producir energía y afrontar el estrés. En hígados humanos con MASH, así como en ratones enfermos y hepatocitos estresados, los niveles de PGC-1α eran notablemente más bajos, mientras que una proteína de fisión mitocondrial llamada DRP1 y una enzima activadora de lípidos llamada ACSL4 eran más altas. Usando ratones modificados genéticamente que carecían de PGC-1α solo en las células hepáticas, los autores observaron que la pérdida de este guardián hacía que las dietas ricas en grasa fueran mucho más dañinas: los hígados eran más grasos, más inflamados, con mayor carga de hierro y mostraban señales de ferroptosis más intensas. A nivel celular, la deficiencia de PGC-1α aumentó la actividad de DRP1, incrementó ACSL4 y las proteínas importadoras de hierro, y debilitó las defensas antioxidantes que normalmente mantienen la ferroptosis bajo control.
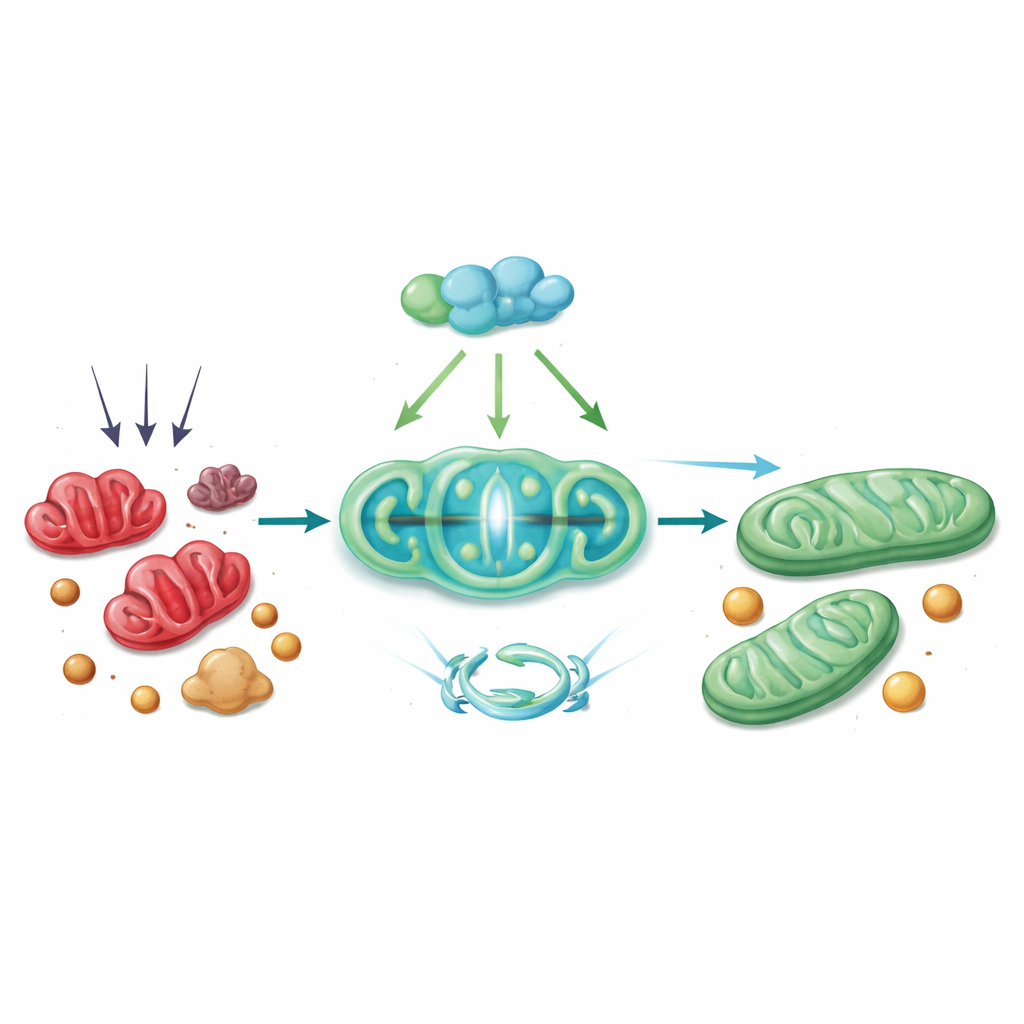
Una reacción en cadena protectora dentro de la célula
Mecánicamente, PGC-1α actúa a través de una cadena de colaboradores. Trabaja con un factor de transcripción llamado Nrf1 para aumentar la producción de Tim23, un canal en la membrana interna mitocondrial esencial para importar proteínas y mantener una estructura sana. Cuando los niveles de Tim23 disminuyen, el potencial de membrana mitocondrial se deteriora, lo que desencadena a DRP1 para fragmentar el orgánulo. El estudio muestra que con Tim23 reducido, DRP1 está más activo y tiende a asociarse con ACSL4 en la superficie mitocondrial, atrayendo esta enzima modificadora de lípidos hacia las mitocondrias. Allí, ACSL4 contribuye a iniciar los cambios lipídicos que hacen a las células vulnerables a la ferroptosis. Restaurar PGC-1α —ya sea en ratones mediante un vector viral de entrega génica o en hepatocitos en cultivo con un activador basado en CRISPR— revirtió muchos de estos pasos: Tim23 aumentó, la actividad de DRP1 y ACSL4 disminuyó, las mitocondrias parecieron más sanas y los marcadores de ferroptosis y daño hepático se redujeron.
Cómo este descubrimiento podría orientar terapias futuras
Para un público no especializado, la conclusión principal es que el hígado posee un freno interno contra la muerte celular impulsada por hierro y lípidos, y que este freno está integrado en las mitocondrias. La cadena PGC-1α–Tim23–DRP1–ACSL4 funciona como un circuito de seguridad: cuando PGC-1α es robusto, Tim23 mantiene las mitocondrias estables, DRP1 y ACSL4 están contenidos y los hepatocitos tienen menos probabilidad de autodestruirse. Cuando este circuito falla, la ferroptosis se acelera y la MASH empeora. Al identificar esta vía en tejido humano y modelos animales, el estudio destaca dos estrategias complementarias para tratamientos futuros: bloquear directamente la ferroptosis y potenciar la actividad de PGC-1α o Tim23 para estabilizar las mitocondrias, ofreciendo esperanza para intervenciones más tempranas y efectivas antes de que se instale la cicatrización hepática irreversible.
Cita: Zhao, Y., Zhang, L., Li, B. et al. PGC-1α protects against MASH via Tim23-dependent inhibition of DRP1-mediated ferroptosis. Cell Death Dis 17, 246 (2026). https://doi.org/10.1038/s41419-026-08493-8
Palabras clave: enfermedad del hígado graso, mitocondrias, muerte celular, metabolismo del hierro, inflamación hepática