Clear Sky Science · es
NSD2 inhibe la expresión de PD-L1 vía la fosforilación oxidativa para controlar la vigilancia inmunitaria en el carcinoma hepatocelular
Por qué importa esta historia sobre el cáncer de hígado
El carcinoma hepatocelular, la forma más común de cáncer de hígado, suele diagnosticarse en fases avanzadas y es resistente a muchos tratamientos. Los fármacos de inmunoterapia que bloquean la “capa de invisibilidad” PD-L1 en las células tumorales benefician a algunos pacientes, pero no a la mayoría. Este estudio descubre un actor inesperado, una proteína llamada NSD2, que conecta cómo las células de cáncer de hígado generan energía con la visibilidad que tienen ante el sistema inmune. Comprender este vínculo puede señalar nuevas maneras de reforzar las terapias actuales e identificar a los pacientes con más probabilidades de beneficiarse.
Un papel sorprendente para una proteína del cáncer conocida
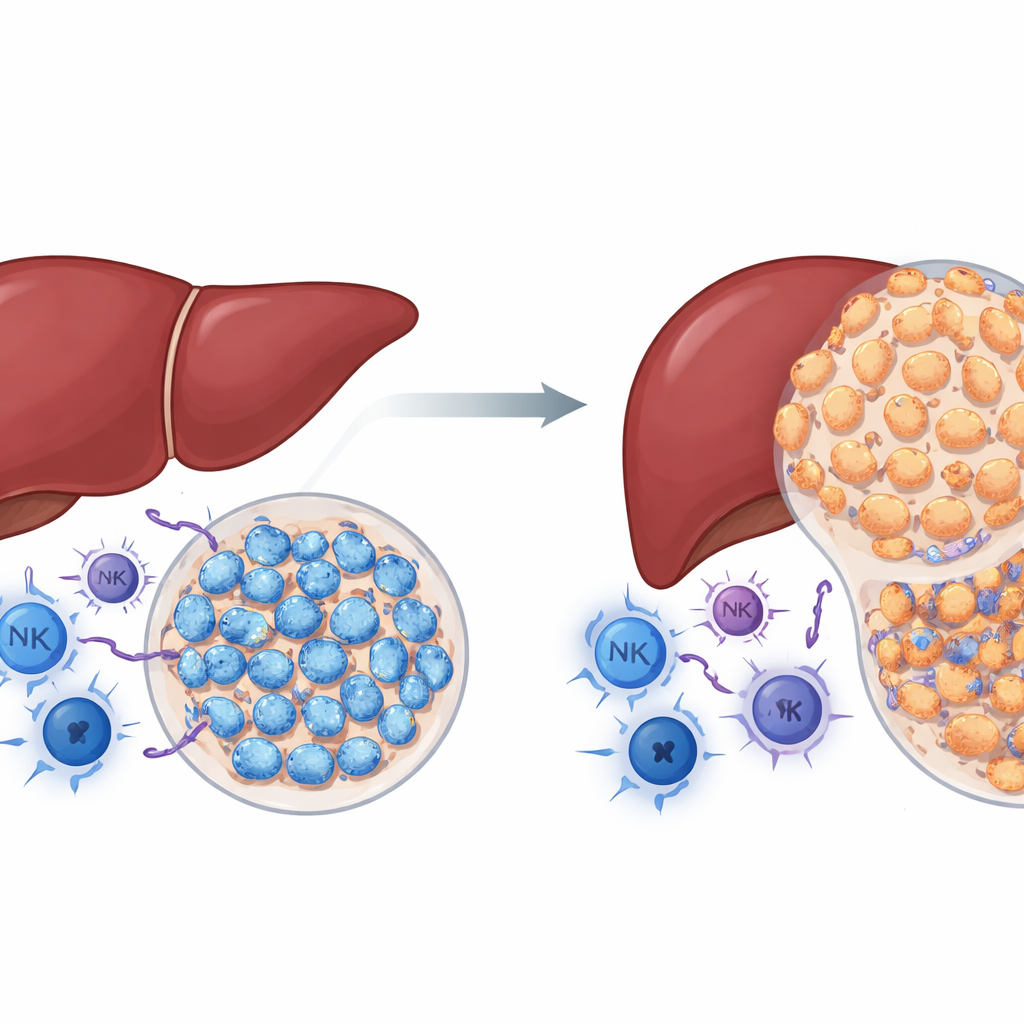
NSD2 es una enzima que modifica histonas, las proteínas alrededor de las cuales se enrolla el ADN. En muchos cánceres, NSD2 se ha considerado un impulsor del crecimiento tumoral. Los autores se preguntaron si lo mismo ocurre en el cáncer de hígado. Usando ratones genéticamente modificados en los que NSD2 se activa específicamente en las células hepáticas, trataron a los animales con un químico que induce de forma fiable tumores hepáticos. Contrariamente a lo esperado, los ratones con sobreexpresión de NSD2 desarrollaron muchos menos y más pequeños tumores que los ratones normales, y sus hígados mostraron menos daño, cicatrización y proliferación celular. Al mismo tiempo, los tumores de hígados con NSD2 sobreexpresada contenían más células inmunitarias contra el cáncer, incluidos linfocitos T colaboradores y citotóxicos y células NK. Estos hallazgos sugieren que, en un sistema inmune intacto, NSD2 se comporta menos como un acelerador y más como un freno del carcinoma hepatocelular.
Fábricas de energía y consumo de combustible en las células tumorales
Para entender cómo NSD2 restringe los tumores, el equipo perfiló la actividad génica en tejido hepático. Encontraron que la sobreexpresión de NSD2 suprimía de forma marcada genes implicados en la fosforilación oxidativa, el proceso por el cual las mitocondrias —las “centrales eléctricas” de la célula— generan energía usando oxígeno. Experimentos de seguimiento en líneas celulares de cáncer hepático de ratón y humano mostraron que aumentar NSD2 reducía la expresión de muchos genes de fosforilación oxidativa, disminuía el consumo de oxígeno y la producción de ATP, y reducía el potencial de membrana mitocondrial, señal de una menor actividad mitocondrial. Al mismo tiempo, estas células consumían menos glucosa pero no desplazaban su dependencia hacia la glucólisis, lo que indica una reducción neta en la producción energética. La pérdida de NSD2 tuvo efectos opuestos, reforzando la potencia mitocondrial y el uso de combustible.
Cómo NSD2 reconfigura la energía y la visibilidad inmune
Profundizando, los investigadores combinaron mapeo cromatínico a escala genómica con datos de expresión génica e identificaron un conjunto de genes activados directamente cuando NSD2 está presente. Dos de ellos, Camk2d y Prkce, se conocen por restringir la actividad mitocondrial. NSD2 aumentó una marca histónica particular (H3K36me2) en sus promotores, potenciando su expresión. Reintroducir estos genes en células de cáncer hepático deficientes en NSD2 redujo el uso de oxígeno mitocondrial y la producción de ATP, confirmando que actúan como frenos aguas abajo de NSD2 sobre la fosforilación oxidativa. De forma importante, trabajos previos sugirieron que mitocondrias altamente activas favorecen niveles altos de PD-L1 en las células tumorales. En consonancia con esto, los autores hallaron que la sobreexpresión de NSD2 reducía los niveles de PD-L1, mientras que la pérdida de NSD2 aumentaba PD-L1 en células de cáncer hepático y en tejido tumoral.
Bajar el escudo y despertar el ataque inmune
El impacto funcional de estos cambios moleculares se probó en ratones que recibieron inyecciones hepáticas de células cancerosas modificadas para ganar o perder NSD2. Las células carentes de NSD2 formaron rápidamente tumores más grandes, expresaron más PD-L1 y fueron infiltradas por menos linfocitos T y células NK, especialmente menos linfocitos T citotóxicos activados. Cuando los investigadores bloquearon químicamente el complejo V mitocondrial, un componente clave de la fosforilación oxidativa, los niveles de PD-L1 en células deficientes en NSD2 volvieron a bajar hacia lo normal y las células inmunitarias pudieron inducir mejor la muerte de células tumorales. De modo similar, sobreexpresar Camk2d o Prkce en células sin NSD2, o tratar los tumores con un anticuerpo que bloquea PD-L1, redujo el tamaño tumoral y restauró la infiltración de células inmunitarias. En conjuntos de datos de pacientes, la baja expresión de NSD2 se asoció con peor supervivencia pero, de forma intrigante, con una mejor respuesta a la terapia dirigida a PD-L1, lo que sugiere que el estado de NSD2 podría ayudar a predecir quién se beneficia de estos fármacos.
Qué significa esto para el futuro cuidado del cáncer de hígado
Para un lector general, el mensaje clave es que este estudio redefine a NSD2 como un factor supresor de tumores en el cáncer de hígado, al menos en presencia de un sistema inmune funcional. Al reducir la producción de energía basada en oxígeno de la célula, NSD2 disminuye indirectamente PD-L1 en las células tumorales, quitando parte de su capa de invisibilidad y permitiendo que las células inmunitarias las reconozcan y ataquen. Esta cadena recientemente descrita NSD2–energía–PD-L1 sugiere dos ideas prácticas: primero, los pacientes cuyos tumores carecen de NSD2 podrían ser candidatos especialmente buenos para fármacos bloqueadores de PD-L1; y segundo, combinar fármacos que inhiban la producción de energía mitocondrial con inmunoterapia podría ofrecer un golpe combinado potente contra el carcinoma hepatocelular.
Cita: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Palabras clave: carcinoma hepatocelular, NSD2, fosforilación oxidativa, PD-L1, inmunoterapia tumoral