Clear Sky Science · es
La regulación del empalme de DDX39B mediada por SNRPD2 promueve la progresión del cáncer de endometrio al suprimir la activación de exones crípticos de CTSC
Por qué importan los mensajes ocultos en los genes del cáncer
El cáncer de endometrio, un tumor frecuente del útero, está aumentando en todo el mundo, y muchos pacientes con enfermedad avanzada siguen teniendo pocas opciones efectivas. Este estudio revela cómo un proceso sutil dentro de las células—la manera en que recortan y pegan los mensajes genéticos—puede impulsar a los tumores endometriales a crecer y diseminarse. Al exponer un frágil “diagrama de cableado” del que dependen las células cancerosas, el trabajo señala nuevas formas de apagar los tumores mediante medicinas genéticas de precisión.
Un cáncer en crecimiento que necesita nuevas respuestas
El cáncer de endometrio es ahora el cáncer ginecológico más frecuente en muchos países occidentales, con casos y muertes en aumento tanto en Occidente como en China. Se emplean cirugía, radioterapia, quimioterapia, tratamientos hormonales e inmunoterapia, pero están lejos de ser perfectos. La extirpación del útero elimina la fertilidad, los tratamientos hormonales con frecuencia fracasan y los tumores agresivos suelen reaparecer. Estos desafíos han llevado a los investigadores a buscar puntos débiles moleculares dentro de las células cancerosas que puedan ser atacados con terapias más precisas.
La maquinaria de empalme celular como punto débil
Para funcionar, nuestros genes se copian primero en largas moléculas de ARN que deben ser recortadas y cosidas en un proceso llamado empalme. Máquinas proteicas especializadas denominadas espliceosomas deciden qué fragmentos se conservan y cuáles se descartan, efectivamente editando el guion que las células usan para fabricar proteínas. El equipo se centró en un componente del espliceosoma llamado SNRPD2, parte de una familia de proteínas “Sm” que ayudan a ensamblar la maquinaria de empalme. Al explorar grandes bases de datos de genes y proteínas de cáncer y examinar muestras de pacientes, hallaron que los niveles de SNRPD2 son notablemente más altos en tumores endometriales que en el revestimiento uterino normal, y que los pacientes cuyos tumores tienen más SNRPD2 tienden a evolucionar peor.
Apagar a un editor maestro frena los tumores
Para comprobar si SNRPD2 es solo un espectador o un impulsor activo, los investigadores redujeron su expresión en líneas celulares de cáncer de endometrio cultivadas en el laboratorio. Cuando SNRPD2 se silenciaba, las células se dividían más despacio, formaban menos colonias y eran menos capaces de moverse e invadir a través de membranas—comportamientos asociados a la metástasis. Cuando estas células alteradas se implantaron en ratones, los tumores resultantes fueron mucho más pequeños y mostraron menos células en división activa. De forma importante, el equipo diseñó oligonucleótidos antisentido—fragmentos cortos y similares a fármacos de ADN sintético—que atacan específicamente el ARN de SNRPD2. En un modelo de xenoinjerto derivado de pacientes, en el que fragmentos tumorales humanos crecen en ratones inmunodeficientes, estos fármacos antisentido redujeron drásticamente los niveles de SNRPD2 y el tamaño tumoral, lo que sugiere que SNRPD2 podría ser abordable terapéuticamente de manera clínicamente relevante.
Una cadena de tres pasos: del error de empalme al crecimiento canceroso
Al profundizar en los datos genéticos, los investigadores preguntaron cómo la pérdida de SNRPD2 reconfigura los mensajes de ARN en todo el genoma. Descubrieron que cuando SNRPD2 se reduce, una enzima clave del procesamiento del ARN llamada DDX39B comienza a fallar. Normalmente, DDX39B ayuda a eliminar un intrón particular—un segmento de ARN que debe ser recortado—de su propio mensaje. Sin suficiente SNRPD2, ese intrón permanece, creando una versión defectuosa del ARN de DDX39B que la célula destruye rápidamente. La reducción de DDX39B tiene entonces un efecto en cascada sobre otro gen, CTSC, que codifica una enzima proteolítica conocida por favorecer el crecimiento y la diseminación tumoral. En condiciones sanas, un exón “críptico” oculto dentro del ARN de CTSC se ignora, permitiendo que las células produzcan la proteína CTSC completa y activa. Con menos DDX39B, ese exón críptico se incluye por error, insertando señales de parada prematuras en el ARN. El mensaje malformado de CTSC se degrada antes de producir mucha proteína, y las células cancerosas pierden parte de su agresividad.
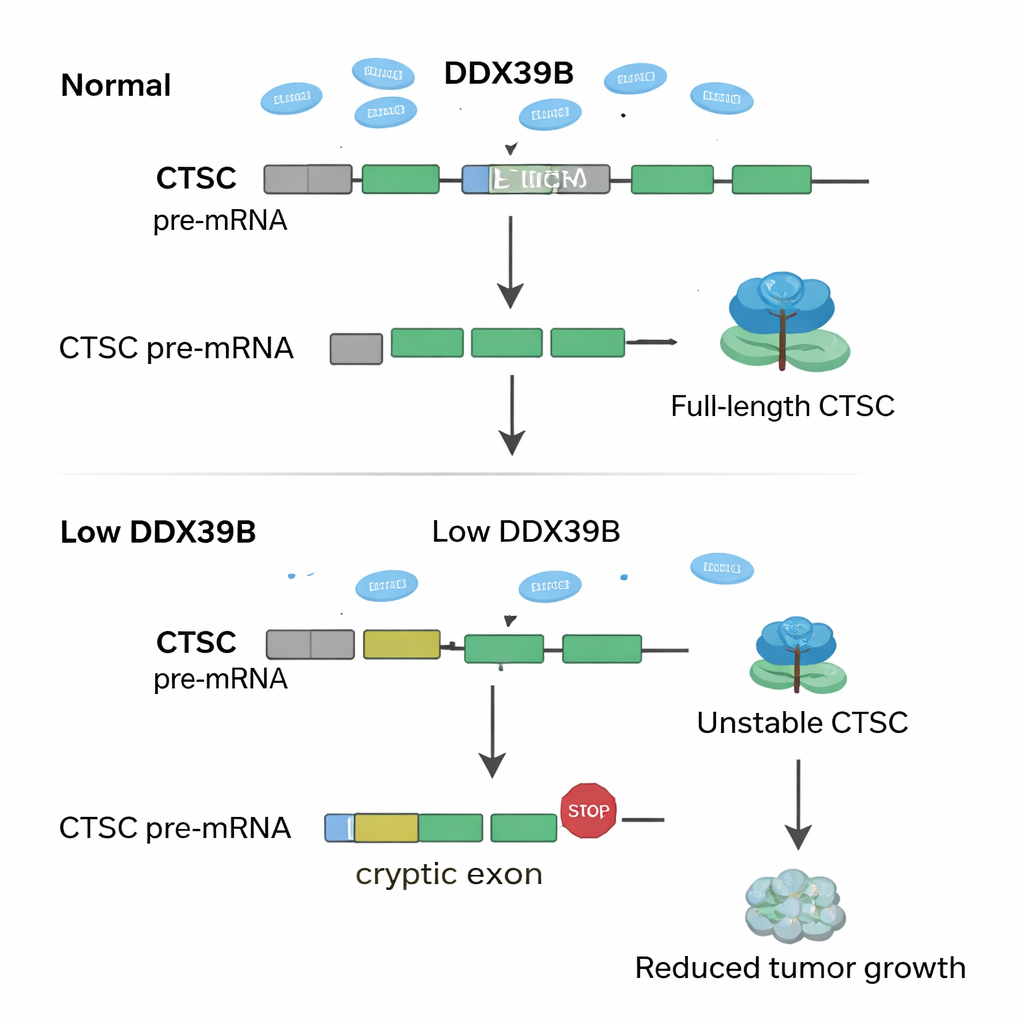
Qué significa esto para tratamientos futuros
En pocas palabras, los autores descifran un sistema de relevo—SNRPD2 → DDX39B → CTSC—que las células del cáncer de endometrio explotan para prosperar. Un SNRPD2 alto mantiene abundante a DDX39B; DDX39B, a su vez, evita que CTSC use exones crípticos dañinos, preservando la proteína CTSC en su forma completa que ayuda al tumor a crecer y diseminarse. Cuando SNRPD2 se bloquea, esta cadena se desploma, los niveles de CTSC caen y los tumores se debilitan. Para los no especialistas, la idea clave es que las células cancerosas dependen de un empalme de ARN muy preciso, y pequeñas “errores” forzadas pueden envenenar selectivamente su crecimiento. Apuntar a SNRPD2 con fármacos antisentido, o forzar directamente el uso de exones crípticos en CTSC, podría ofrecer nuevas terapias más adaptadas para pacientes con cáncer de endometrio.
Cita: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Palabras clave: cáncer de endometrio, empalme de ARN, SNRPD2, DDX39B, CTSC