Clear Sky Science · es
DNMT2 inhibe la progresión del cáncer de tiroides anaplásico al reducir la producción de 5’tiRNAGly-GCC
Por qué importa esta química oculta del ARN
El cáncer de tiroides anaplásico es uno de los tumores humanos más letales, y a menudo provoca la muerte de los pacientes en cuestión de meses pese a cirugía, radiación y quimioterapia. Este estudio revela a un culpable sorprendente en el interior de las células cancerosas: pequeñas marcas químicas en el ARN de transferencia, las moléculas que ayudan a fabricar proteínas. Los autores muestran que cuando una enzima concreta, DNMT2, se pierde o reduce, los tumores tiroideos crecen más rápido, se diseminan con mayor facilidad y resisten al fármaco quimioterápico habitual doxorrubicina. Aún más intrigante, identifican un pequeño fragmento de ARN que aparece cuando DNMT2 está bajo y demuestran que bloquear ese fragmento podría convertirse en una nueva estrategia terapéutica.
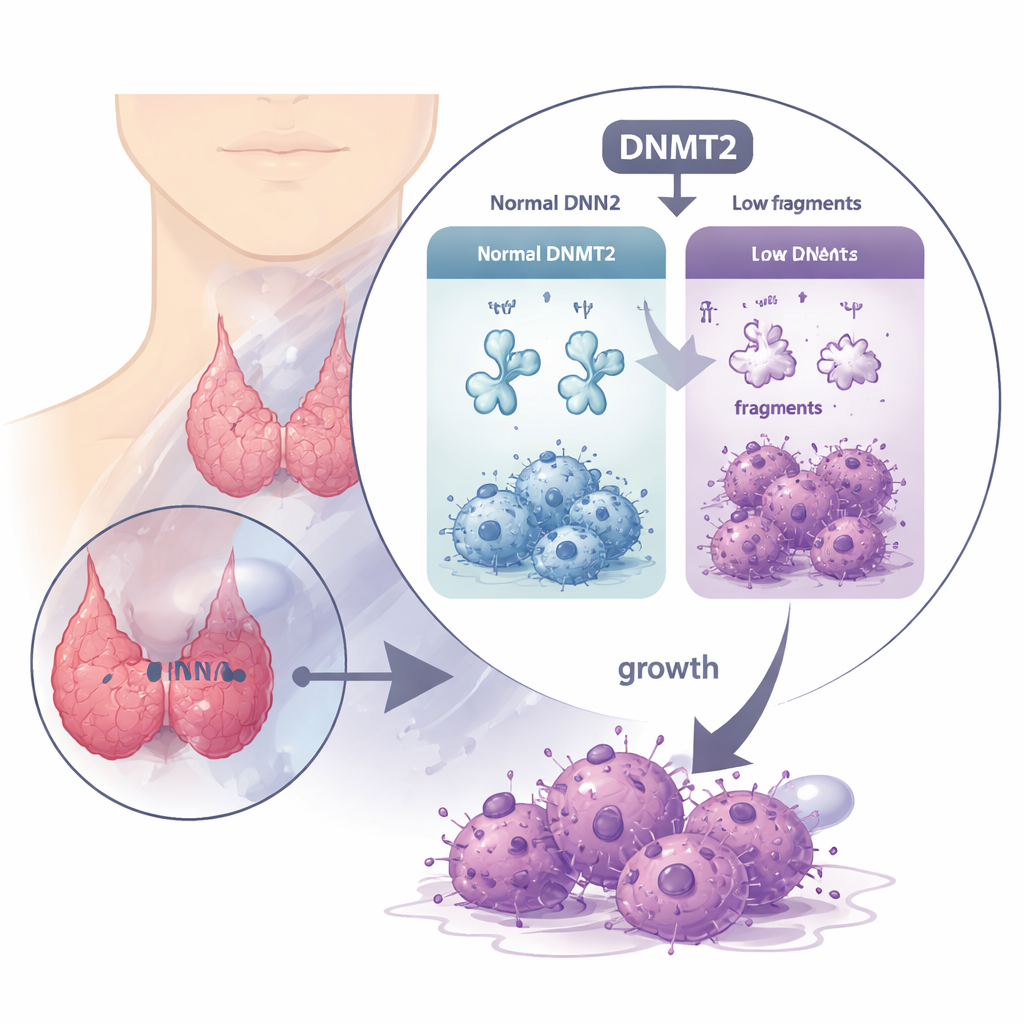
Una enzima protectora que desaparece
Los ARN de transferencia (ARNt) normalmente transportan aminoácidos a la maquinaria celular que fabrica proteínas, y su estabilidad depende de delicadas decoraciones químicas. DNMT2 es una enzima que añade una de esas marcas, llamada grupo metilo, en puntos específicos del ARNt. En muchos cánceres DNMT2 está elevado y se piensa que ayuda a los tumores, pero aquí la historia es la inversa. Mediante el análisis de grandes bases de datos de pacientes y muestras tumorales, los investigadores hallaron que los niveles de DNMT2 son significativamente más bajos en tejido de cáncer de tiroides anaplásico que en tiroides normal. Los pacientes cuyos tumores contenían más DNMT2 tendieron a vivir más tiempo sin empeoramiento de la enfermedad, lo que sugiere que DNMT2 actúa más como un freno que como un acelerador en esta enfermedad.
Cómo el descenso de DNMT2 alimenta el comportamiento agresivo
Para ver qué hace realmente DNMT2 en las células cancerosas, el equipo manipuló sus niveles en líneas celulares de cáncer de tiroides anaplásico cultivadas en placa y en modelos murinos. Cuando DNMT2 se redujo, las células se multiplicaron más rápido, invadieron membranas con mayor facilidad y formaron más colonias, todos rasgos de un tumor agresivo. Estas células también se volvieron menos sensibles a la doxorrubicina, un fármaco estándar para este cáncer. En ratones, los tumores diseñados para tener menos DNMT2 crecieron más y se diseminaron a los pulmones con mayor facilidad, mientras que aumentar la expresión de DNMT2 produjo el efecto opuesto. Los investigadores atribuyeron estos cambios en parte a la activación de un programa celular conocido como transición epitelio–mesénquima, que hace a las células cancerosas más móviles e invasivas.
Del ARNt dañado a fragmentos pequeños y nocivos
Profundizando, el estudio muestra que DNMT2 coloca una marca metilo en una posición específica (llamada C38) en solo tres tipos de ARNt. Sin esta protección, los ARNt se vuelven más vulnerables al corte por otra enzima, la angiogenina. Ese corte genera un fragmento corto de ARN derivado del ARNt-Gly-GCC, denominado 5’tiRNAGly-GCC. Mediante secuenciación y pruebas bioquímicas, los autores encontraron que cuando DNMT2 es bajo, este fragmento se acumula, especialmente a partir del ARNt que transporta glicina. En experimentos in vitro, añadir la marca metilo protegió fuertemente al ARNt de ser cortado, confirmando que DNMT2 normalmente resguarda estas moléculas de ser fragmentadas en piezas más pequeñas y potencialmente dañinas.
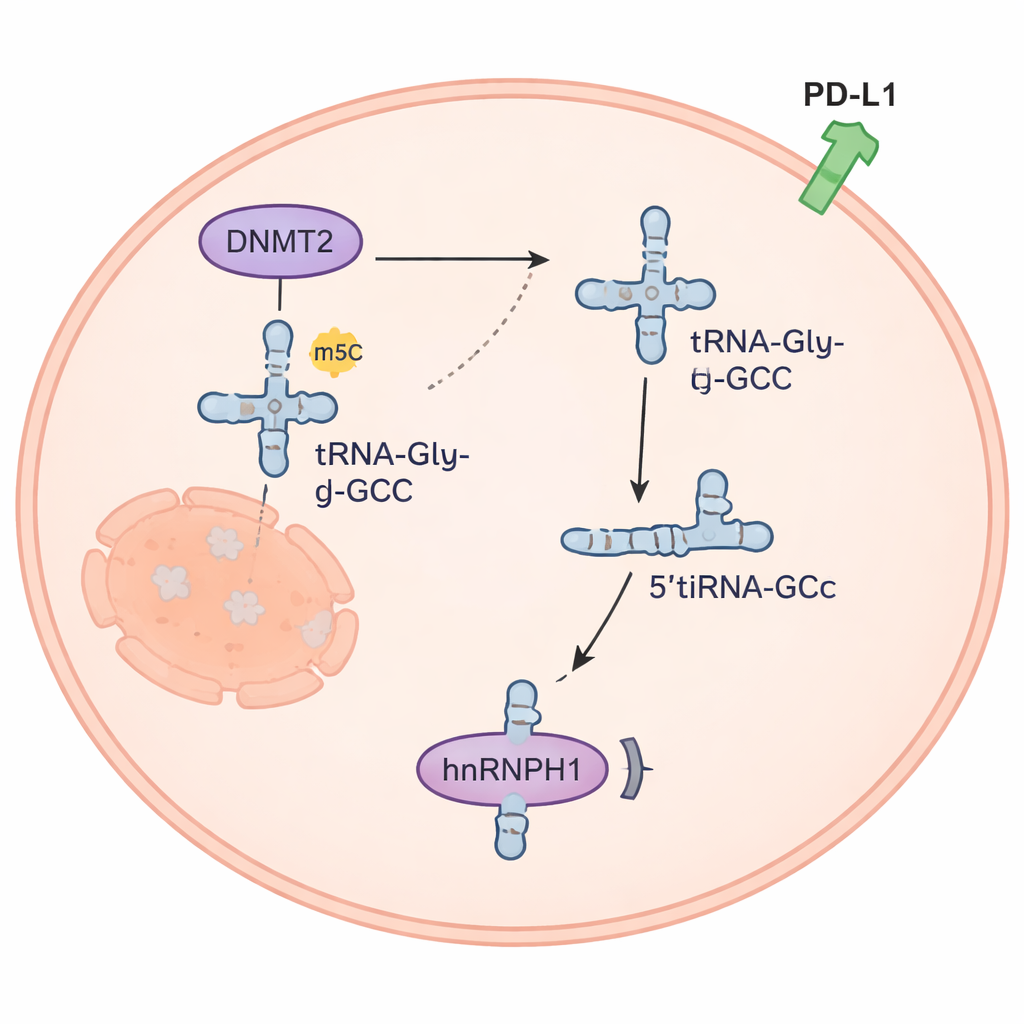
Un diminuto fragmento de ARN reconfigura señales cancerígenas
El fragmento 5’tiRNAGly-GCC resultó ser algo más que despojos moleculares. Era abundante en células de cáncer de tiroides anaplásico pero escaso en células tiroideas normales. Cuando los investigadores elevaron artificialmente sus niveles, las células cancerosas proliferaron más, invadieron más y se volvieron más resistentes a la doxorrubicina; reducir el fragmento produjo el efecto contrario. En ratones, un inhibidor químicamente diseñado de 5’tiRNAGly-GCC ralentizó el crecimiento tumoral, y combinar este inhibidor con doxorrubicina funcionó incluso mejor que cualquiera de los tratamientos por separado. El equipo descubrió que 5’tiRNAGly-GCC se une a una proteína llamada hnRNPH1, reduciendo su cantidad dentro de las células. Como hnRNPH1 normalmente ayuda a mantener a raya los niveles de la proteína relacionada con la respuesta inmune PD-L1, perder hnRNPH1 permite que PD-L1 aumente, un cambio que puede ayudar a los tumores a escapar del ataque inmunitario y está relacionado con la acumulación de células T reguladoras alrededor de los tumores.
Qué significa esto para tratamientos futuros
En términos sencillos, el estudio revela una reacción en cadena: cuando DNMT2 es bajo, ciertos ARNt pierden una marca protectora, se cortan en fragmentos pequeños y uno de esos fragmentos (5’tiRNAGly-GCC) inactiva una proteína que frena a PD-L1. El resultado es un cáncer más agresivo, resistente a fármacos y evasivo frente al sistema inmune. En lugar de intentar aumentar DNMT2 directamente —lo que podría ser arriesgado en otros tejidos— los autores proponen dirigirse al fragmento de ARN nocivo. Los experimentos en ratones con un inhibidor de 5’tiRNAGly-GCC, especialmente cuando se combina con doxorrubicina, ofrecen una prueba preliminar de que interrumpir este circuito microscópico de ARN podría ayudar a domar una de las formas más letales de cáncer tiroideo.
Cita: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Palabras clave: cáncer de tiroides anaplásico, DNMT2, fragmentos de ARNt, quimiorresistencia, PD-L1