Clear Sky Science · es
Revelando a ZNF124 como un nuevo determinante en la neurodegeneración: orquestación de la homeostasis de los fotorreceptores mediante la regulación transcripcional de MSX2
Por qué este hallazgo importa para la visión
La retinosis pigmentaria es una de las principales causas de ceguera hereditaria, y sin embargo en casi el 40 % de los pacientes los médicos aún no pueden identificar el gen defectuoso. Este estudio revela un nuevo actor genético, llamado ZNF124, que ayuda a mantener con vida las células sensibles a la luz en el ojo. Al mostrar cómo una mutación en este gen perturba una cadena de “interruptores” moleculares en la retina, los investigadores abren nuevas vías para el diagnóstico y, potencialmente, para tratamientos dirigidos para personas que están perdiendo la visión.
Una causa oculta de pérdida visual hereditaria
Los investigadores estudiaron una familia numerosa en la que varios niños desarrollaron signos clásicos de retinosis pigmentaria: ceguera nocturna desde edades tempranas, reducción del campo visual periférico y pérdida gradual de la visión central. Exámenes oculares detallados revelaron adelgazamiento de la retina y respuestas eléctricas débiles a la luz, ambos rasgos característicos del daño a los fotorreceptores de bastón y cono. Sin embargo, ninguno de los más de 80 genes conocidos asociados con retinosis pigmentaria mostraba defectos evidentes en estos pacientes, lo que sugería que un gen aún no identificado podría ser responsable de su enfermedad.
Encontrando un interruptor genético defectuoso
Mediante secuenciación del exoma completo, que lee las partes codificantes de las proteínas del ADN, el equipo identificó una mutación rara y no informada previamente en el gen ZNF124. Esta mutación altera la forma en que se empalma el ARN del gen, eliminando unas pocas bases en una unión crítica. Como resultado, la proteína ZNF124 queda truncada y pierde su región de dedos de zinc, una estructura que normalmente se usa para reconocer y unirse a secuencias específicas de ADN. Dado que las proteínas con dedos de zinc suelen actuar como interruptores maestros que activan o reprimen muchos otros genes, un ZNF124 dañado podría tener efectos de gran alcance en las células retinianas.
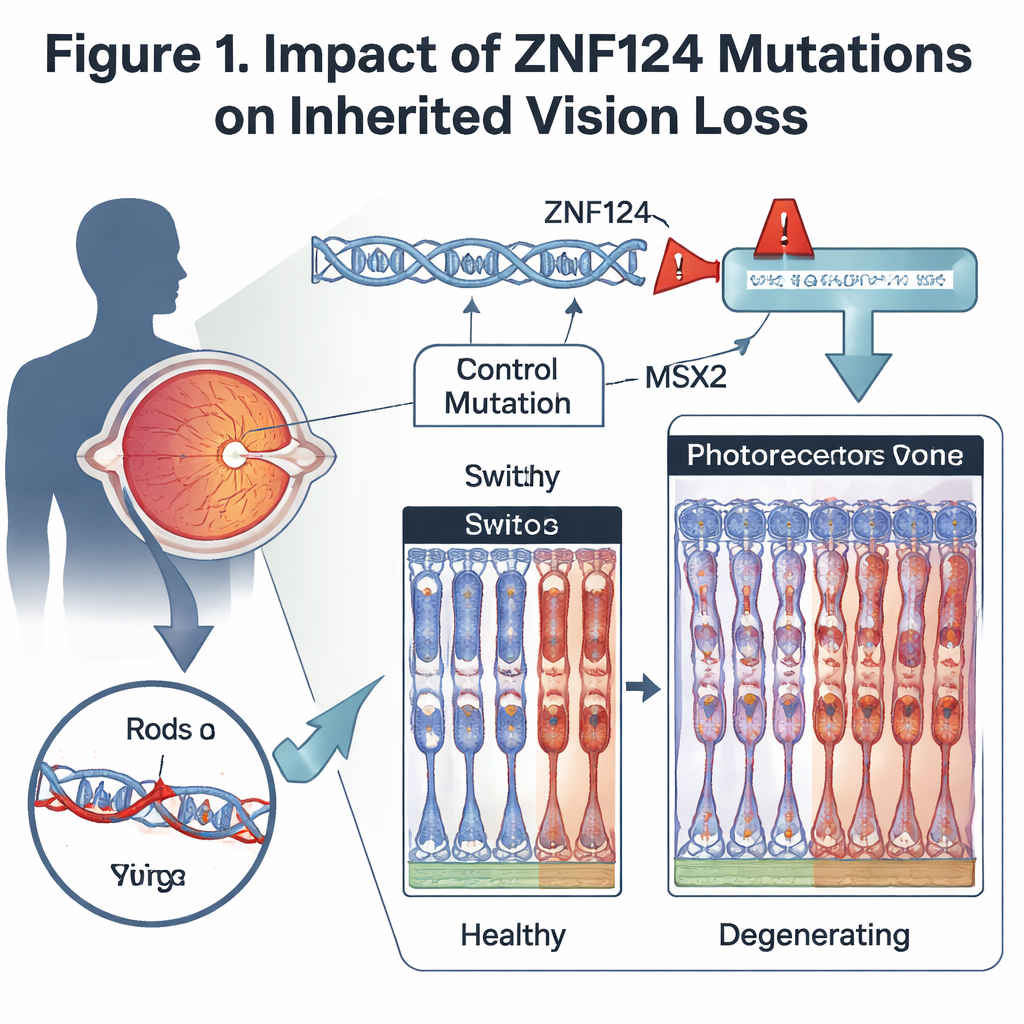
Probando el gen en modelos animales
Para ver cómo la pérdida de este interruptor afecta al ojo, los científicos crearon ratones que carecen de Gm20541, el equivalente murino más cercano a ZNF124, específicamente en la retina. Estos animales desarrollaron problemas visuales dependientes de la edad: sus respuestas eléctricas a la luz tenue y brillante se debilitaron, y el examen microscópico mostró un adelgazamiento progresivo de la capa retiniana que contiene los fotorreceptores. Tanto los bastones, que sostienen la visión nocturna, como los conos, que sostienen la visión diurna y el color, presentaron segmentos externos acortados y pérdida de proteínas visuales clave. Otras células retinianas, como ciertos bipolares, también se redujeron, y las células gliales de sostén se activaron, una respuesta común a una lesión retiniana crónica.
Descubriendo la vía de control ZNF124–MSX2
La siguiente cuestión fue qué genes controla normalmente ZNF124. Utilizando métodos bioquímicos que mapean dónde se sitúan las proteínas sobre el ADN, combinados con lecturas globales de ARN de retinas de ratón, el equipo encontró que ZNF124 se une y activa a otro gen llamado MSX2. En células sanas, ZNF124 se adhiere a una secuencia corta específica en la región “interruptora” de MSX2 y aumenta su actividad. En ratones sin Gm20541, los niveles de MSX2 cayeron a más de la mitad. Cuando los investigadores eliminaron MSX2 específicamente en las células de bastón, esos animales también desarrollaron adelgazamiento de la capa de fotorreceptores y segmentos externos acortados, reflejando los defectos observados en los ratones con la eliminación similar de ZNF124. Esto situó a MSX2 directamente aguas abajo de ZNF124 en una vía esencial para la supervivencia de los fotorreceptores.
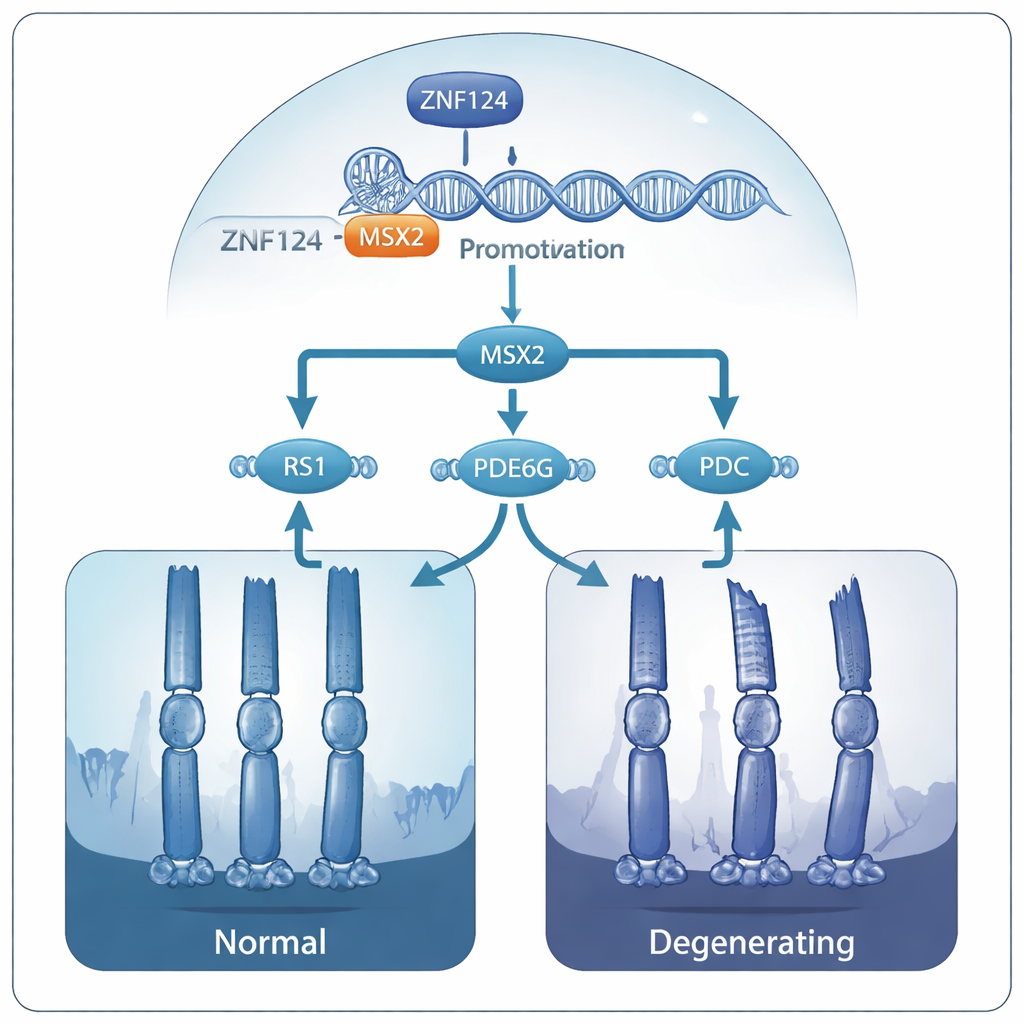
De los interruptores genéticos a fotorreceptores frágiles
Análisis adicionales mostraron que MSX2 a su vez ayuda a mantener varios otros genes ya vinculados a enfermedades retinianas hereditarias: RS1, PDE6G y PDC. Estos genes sostienen la estructura de la retina y la química de la señal visual. Cuando MSX2 se redujo, los tres genes mostraron menor actividad y sus productos proteicos descendieron. Los autores proponen que, en personas con mutaciones dañinas en ZNF124, toda esta cascada se debilita: ZNF124 ya no puede activar completamente a MSX2, MSX2 no sostiene a RS1, PDE6G y PDC, y con el tiempo los fotorreceptores pierden su integridad estructural y mueren, provocando una pérdida progresiva de la visión.
Qué significa esto para pacientes y terapias
Para un público no especializado, el mensaje central es que la retina depende de una jerarquía finamente ajustada de interruptores genéticos. Este trabajo identifica a ZNF124 como un nuevo interruptor de alto nivel cuya falla puede causar ceguera hereditaria a través de una pareja directa aguas abajo, MSX2, y sus genes diana. Clínicamente, ZNF124 puede añadirse ahora a los paneles de pruebas genéticas, ayudando a más familias a recibir diagnósticos precisos. A más largo plazo, terapias que restauren la actividad de ZNF124, MSX2 o de los genes diana afectados podrían ayudar a estabilizar o rescatar las células sensibles a la luz, ofreciendo nueva esperanza a personas con formas de retinosis pigmentaria actualmente sin explicación.
Cita: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
Palabras clave: retinosis pigmentaria, fotorreceptores, ZNF124, MSX2, enfermedad retiniana hereditaria