Clear Sky Science · es
La lisil oxidasa inducida por HIF2α protege el embarazo al remodelar los colágenos en la interfaz feto-materna
Por qué el útero debe prepararse para una nueva llegada
Antes de que un embarazo pueda establecerse, un embrión temprano debe hacer algo notable: incrustarse en la pared del útero y construir un sistema de soporte vital, la placenta. Este artículo explora cómo el tejido materno se remodela silenciosamente para acoger al embrión, centrándose en cómo los niveles bajos de oxígeno y una enzima poco conocida ayudan a preparar el revestimiento uterino. Comprender esta coreografía finamente ajustada puede arrojar luz sobre por qué algunos embarazos fracasan muy pronto y sugerir nuevas maneras de prevenir la infertilidad y las complicaciones gestacionales.
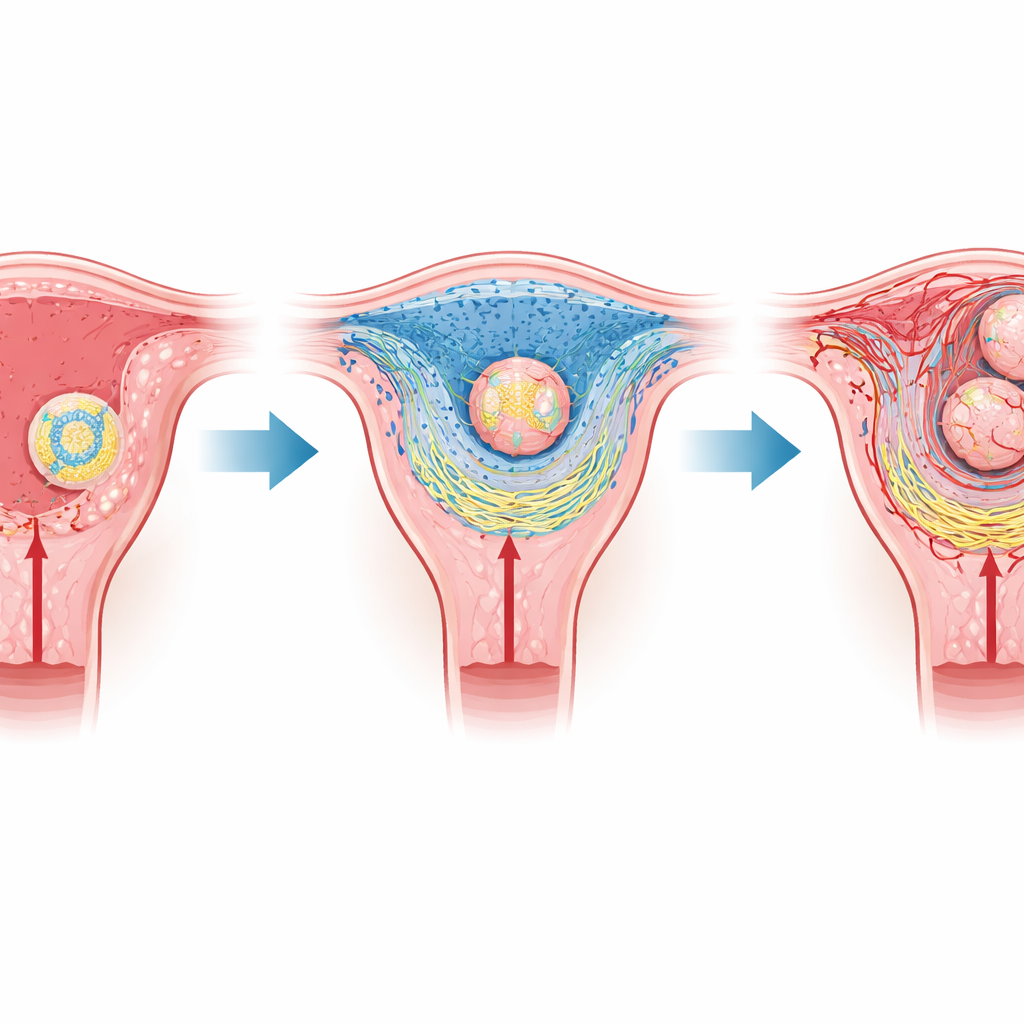
Un encuentro delicado entre madre y embrión
En mamíferos como ratones y humanos, la etapa más temprana del embarazo depende de la implantación, cuando el embrión se adhiere e invade el revestimiento uterino. El embrión está envuelto en una capa de células especializadas que más tarde formarán la placenta, mientras que el tejido materno se transforma en una capa acolchada llamada decidua. Más cerca del embrión se encuentra una región delgada conocida como zona decidual primaria, que carece de vasos sanguíneos y, por tanto, contiene poco oxígeno. Trabajos previos mostraron que este bolsillo de baja oxigenación natural ayuda a desencadenar la implantación, pero no se entendía bien cómo una condición física tan simple podía reorganizar tejidos enteros.
El bajo oxígeno como un interruptor oculto
Los autores usaron una técnica potente llamada transcriptómica espacial, que mapea la actividad génica directamente sobre cortes de tejido, para estudiar úteros de ratón durante los días en que los embriones se adhieren e invaden. Se centraron en una proteína llamada HIF2α, que se activa en condiciones de baja oxigenación y actúa como un interruptor genético. En ratones normales, las células de la zona decidual primaria mostraron una fuerte actividad de genes vinculados al bajo oxígeno y a la construcción del material de andamiaje circundante, incluidos los colágenos que forman la matriz extracelular. Cuando HIF2α se eliminó solo del útero, la disposición general de los tipos celulares parecía sorprendentemente normal. Pero a alta resolución, la red de colágeno estaba desorganizada, la superficie epitelial no se abría correctamente y las células embrionarias tuvieron dificultades para penetrar el tejido materno.
Una enzima que entrecruza el andamiaje
Indagando más, el equipo identificó un actor clave aguas abajo de HIF2α: la lisil oxidasa, o Lox, una enzima que entrecruza químicamente las fibras de colágeno y ayuda a endurecer y estabilizar el tejido. En embarazos normales, los niveles de Lox aumentaron bruscamente alrededor de los embriones precisamente cuando empezaban a invadir. En úteros carentes de HIF2α, la expresión de Lox disminuyó y las fibras de colágeno aparecieron fragmentadas en lugar de formar una malla densa. Para probar la importancia de Lox de forma directa, los investigadores generaron ratones en los que Lox se eliminó solo en el útero. Estas hembras se embarazaron con menos frecuencia, llevaron menos embriones y con frecuencia mostraron signos de pérdida embrionaria y sangrado más adelante en la gestación, aunque los pasos más tempranos de adhesión y engrosamiento tisular parecían inicialmente normales.
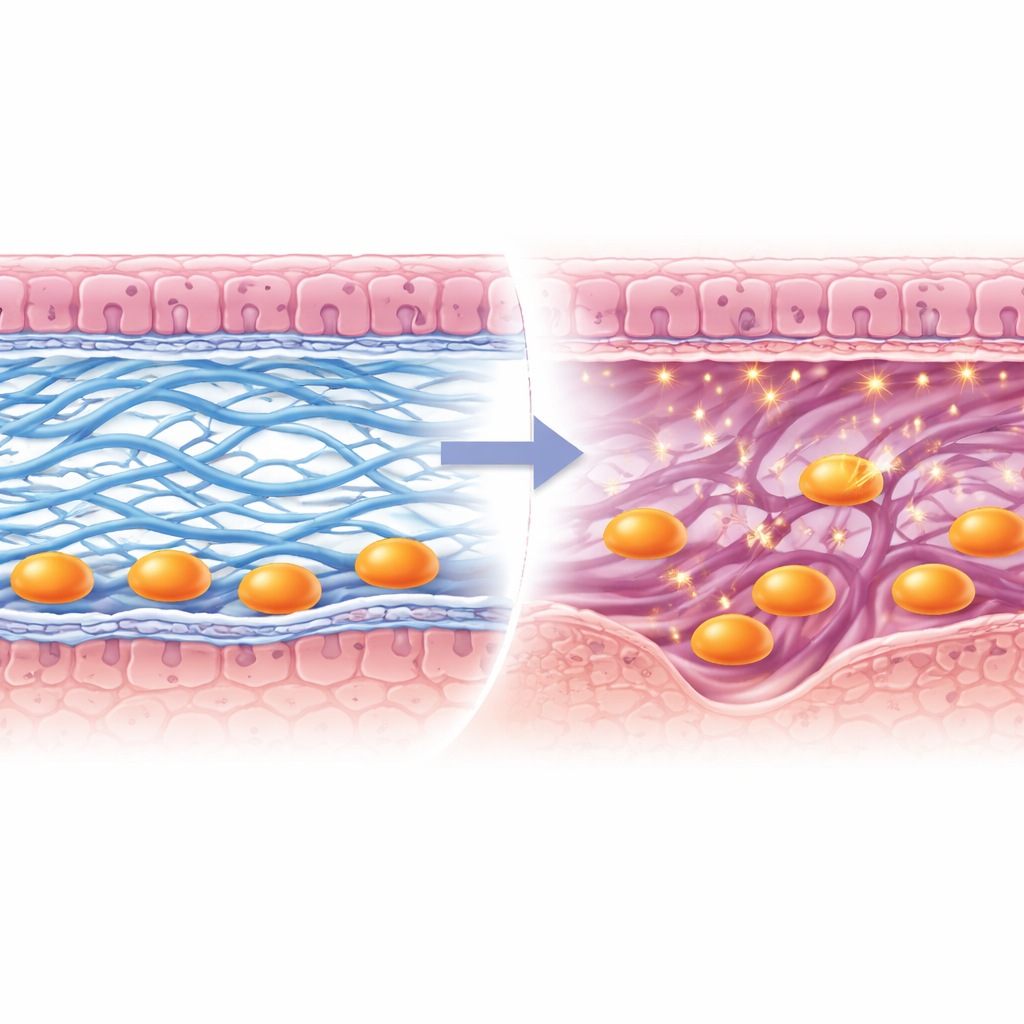
Abrir un camino para la placenta
Imágenes detalladas revelaron qué falló cuando faltaba Lox. Una delgada lámina rica en proteínas llamada membrana basal, que normalmente se descompone para permitir el paso de las células embrionarias, permaneció en gran medida intacta. Las fibras de colágeno tipo I en el estroma subyacente no lograron formar haces robustos y continuos, mientras que el colágeno tipo IV en la membrana basal no se aclaró adecuadamente cerca de las células invasoras. Como resultado, las células trofoblásticas —los pioneros derivados del embrión que construyen la placenta— quedaron atrapadas en la superficie en lugar de abrirse paso en la capa materna. El equipo también encontró que una enzima que corta colágeno, Mmp9, no se activó en estos trofoblastos, lo que dificultó aún más su progreso. Con el tiempo, las estructuras placentarias se formaron de forma deficiente, los embriones crecieron de manera anormal y el éxito del embarazo disminuyó.
Qué significa esto para la salud del embarazo
En conjunto, los hallazgos describen una cadena de eventos en la que el bajo oxígeno en la zona de implantación temprana activa HIF2α, que a su vez aumenta Lox. Lox remodela y entrecruza las fibras de colágeno y ayuda a desmantelar la membrana basal, al tiempo que permite que enzimas como Mmp9 abran un camino. Esta remodelación proporciona tanto un andamiaje estructural como una puerta abierta para que las células trofoblásticas invadan y construyan la placenta. Para un lector general, el mensaje es que el éxito del embarazo depende no solo de embriones sanos y hormonas, sino también del silencioso reequilibrio de la arquitectura tisular materna. Las alteraciones en esta vía hipoxia–HIF2α–Lox podrían estar en la base de algunos casos de infertilidad inexplicada, aborto espontáneo y trastornos vinculados a una invasión placentaria deficiente, lo que sugiere nuevos marcadores diagnósticos y dianas terapéuticas para apoyar el embarazo temprano.
Cita: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Palabras clave: implantación del embrión, matriz extracelular uterina, lisil oxidasa, invasión trofoblástica, desarrollo placentario