Clear Sky Science · es
Dirigir la fosfatasa mitocondrial PGAM5 alivia la ferroptosis y la pancreatitis aguda al aumentar la expresión de FSP1 mediada por NRF2
Por qué importan las células estresadas y los páncreas doloridos
Cuando las células se ven sometidas a demasiada presión, pueden morir de formas que dañan al organismo. Una de esas formas de muerte celular, llamada ferroptosis, está impulsada por el hierro y por reacciones químicas descontroladas que oxidan las grasas de las membranas celulares. Este proceso se ha relacionado con lesiones en órganos, incluida una afección dolorosa y a veces mortífera conocida como pancreatitis aguda. El estudio que sustenta este artículo revela un interruptor de control clave dentro de las mitocondrias —las centrales energéticas de la célula— que puede modular la ferroptosis, y muestra cómo bloquear ese interruptor puede proteger el páncreas en un modelo murino.
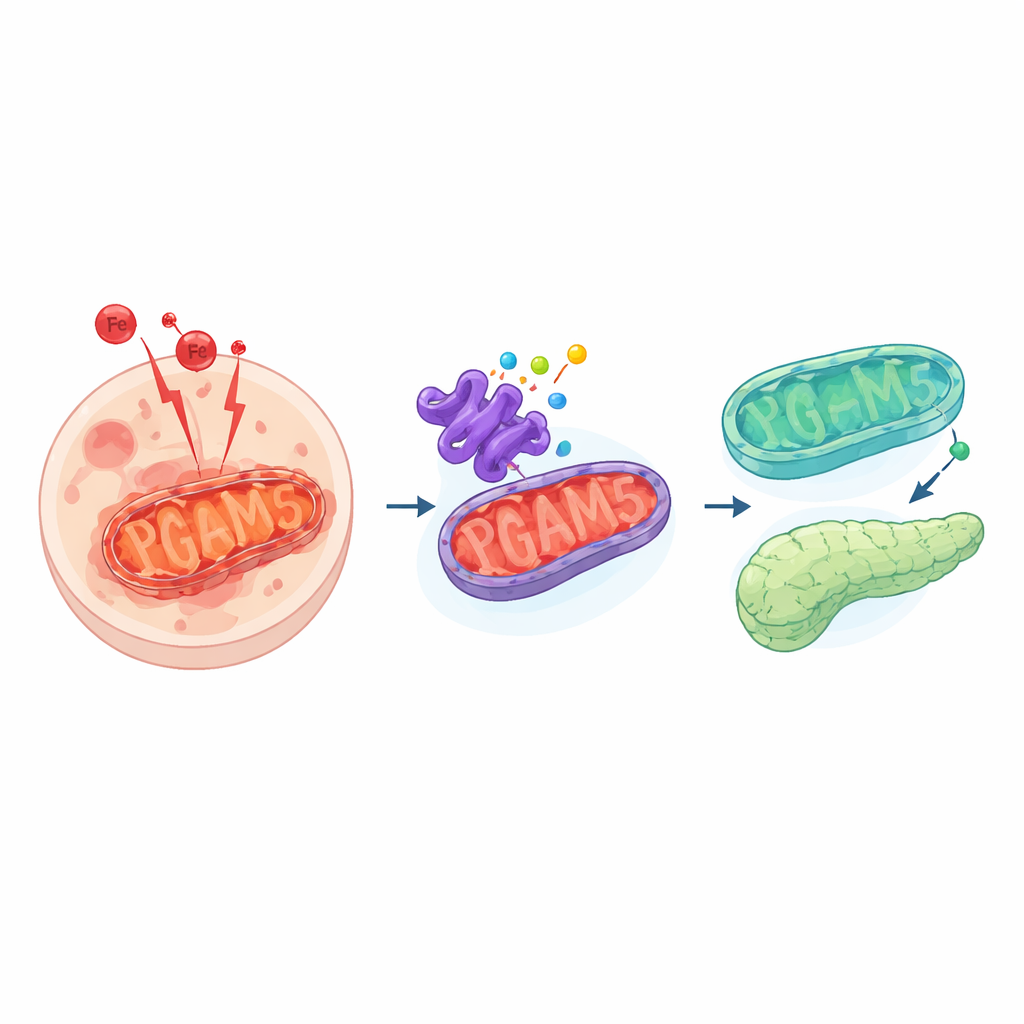
Una forma peligrosa de muerte celular
La ferroptosis es distinta de formas más conocidas de muerte celular como la apoptosis. En lugar de una autodestrucción ordenada, las células que sufren ferroptosis experimentan una tormenta de reacciones impulsadas por el hierro que deterioran las grasas delicadas de sus membranas. Esto genera subproductos tóxicos y agujeros en las membranas que acaban matando a la célula. Normalmente, las células mantienen esto bajo control con sistemas protectores que desintoxican estas moléculas reactivas. Cuando esos sistemas fallan o se ven desbordados, la ferroptosis puede propagar daño por los tejidos, contribuyendo a enfermedades que van desde el cáncer hasta la insuficiencia orgánica.
Un interruptor mitocondrial en la mira
Los investigadores se centraron en una proteína llamada PGAM5, que se localiza en la cara interna de las mitocondrias y actúa como un centro de señalización. PGAM5 ayuda a controlar la forma mitocondrial, responde al estrés e influye en cómo las células manejan la oxidación. Sorprendentemente, cuando el equipo redujo PGAM5 o forzó a las células a producir más, las células resultaron más difíciles de matar por ferroptosis. La inhibición química de PGAM5, la reducción genética y la sobreexpresión disminuyeron la acumulación de subproductos lipídicos dañinos y redujeron la muerte celular provocada por un fármaco que induce ferroptosis. Esto reveló que el sistema está finamente ajustado: tanto la falta como el exceso de PGAM5 empujan a las células hacia un estado más protegido.
Activando un escudo interno
Al profundizar, los autores descubrieron que la influencia de PGAM5 se transmite a través de un eje protector que involucra a otros dos actores: NRF2 y FSP1. NRF2 es un regulador maestro que, cuando está activo en el núcleo, enciende un amplio conjunto de defensas antioxidantes. FSP1 es uno de sus defensores a valle que ayuda a regenerar un antioxidante soluble en grasa, bloqueando el daño lipídico en la membrana celular. Cuando se alteraron los niveles de PGAM5, las células aumentaron tanto el mensaje como las proteínas de NRF2, y NRF2 se trasladó con mayor facilidad del citoplasma al núcleo. Allí, elevó la producción de FSP1. Bloquear FSP1 o NRF2 eliminó la protección y restauró la sensibilidad a la ferroptosis, lo que demuestra que esta cadena PGAM5–NRF2–FSP1 es esencial para la resistencia observada.
El estrés energético como mensajero oculto
El estudio también reveló cómo el estrés mitocondrial se traduce en esta respuesta protectora. Alterar PGAM5 perturbó el equilibrio mitocondrial y desplazó la moneda energética de la célula: la proporción de moléculas de menor energía (AMP y ADP) respecto a la ATP aumentó, señalando estrés energético. Esto, a su vez, activó la enzima sensora de energía AMPK. La AMPK activada modificó directamente a NRF2 de una manera que favoreció su entrada al núcleo, aumentando aún más la producción de FSP1. Cuando se eliminó la AMPK del sistema, NRF2 dejó de acumularse en el núcleo, los niveles de FSP1 cayeron y las células volvieron a sucumbir a la ferroptosis. Así, PGAM5 conecta el estado mitocondrial con una respuesta energética y antioxidante más amplia que protege a las células de la muerte inducida por el hierro.
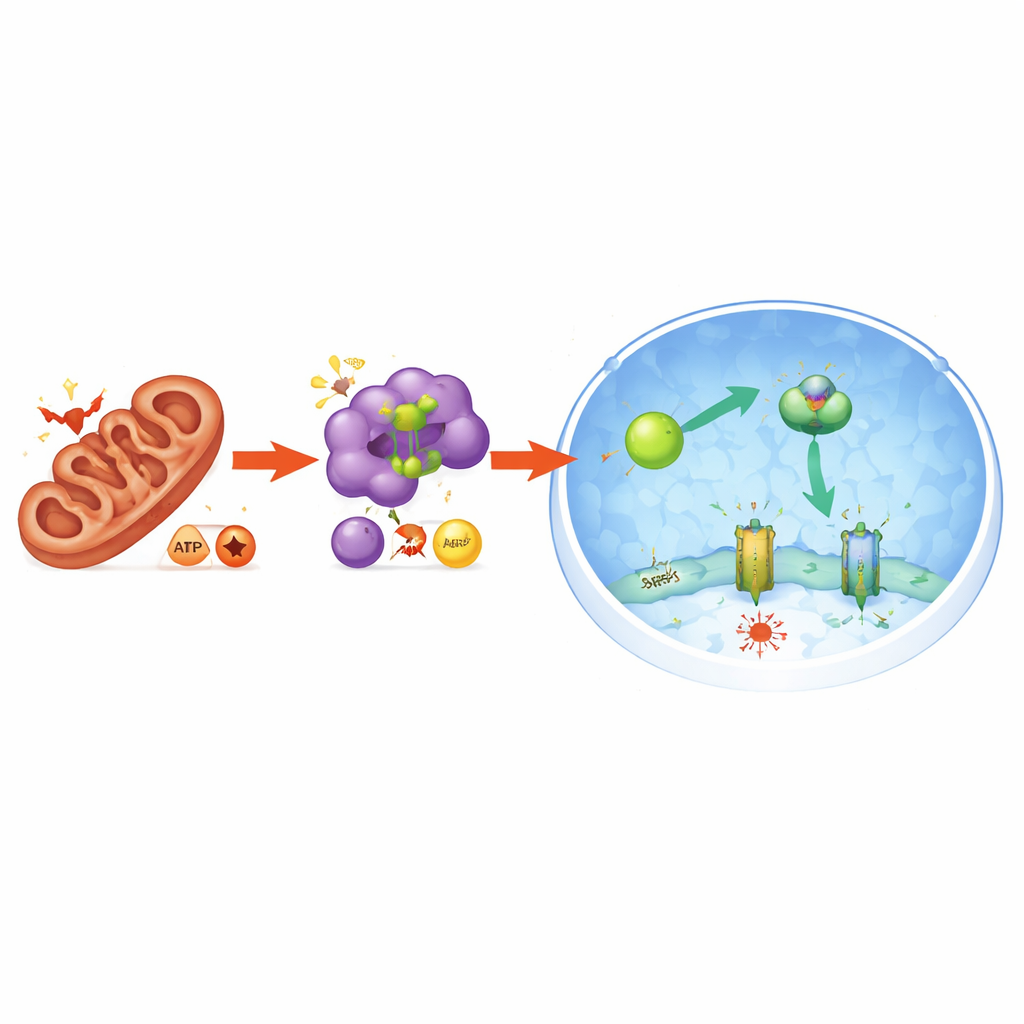
Protegiendo el páncreas en animales vivos
Para comprobar si este mecanismo importa en un órgano completo, los científicos recurrieron a un modelo murino de pancreatitis aguda desencadenada por dosis altas del aminoácido arginina. En este modelo, el páncreas presenta daños extensos, niveles elevados de enzimas sanguíneas que señalan lesión tisular y una oleada de moléculas inflamatorias. También aumentaron con fuerza los marcadores de peroxidación lipídica —una firma de la ferroptosis— en el páncreas. Tratar a los ratones con un compuesto inhibidor de PGAM5 alivió estos síntomas: los marcadores sanguíneos de daño disminuyeron, el tejido pancreático se vio más sano al microscopio y las señales inflamatorias se redujeron. Al mismo tiempo, los marcadores de ferroptosis cayeron, mientras que la actividad de AMPK y los niveles de NRF2 y FSP1 aumentaron en el páncreas, coincidiendo con la vía protectora observada en cultivo celular.
Qué significa esto para tratamientos futuros
En conjunto, el trabajo identifica a PGAM5 como un punto de control central que enlaza el estrés mitocondrial, el estado energético celular y un potente programa antioxidante que bloquea la ferroptosis. Al atenuar la actividad de PGAM5, las células activan AMPK y NRF2, aumentan FSP1 y resisten mejor el daño lipídico inducido por el hierro. En ratones, esta estrategia reduce la lesión pancreática en la pancreatitis aguda. Para el lector no especialista, el mensaje es que los investigadores han hallado un nuevo “interruptor” interno que puede prevenir una forma destructiva de muerte celular. Aunque queda mucho por hacer antes del uso clínico, dirigir PGAM5 o sus socios a valle podría abrir nuevas vías para tratar condiciones en las que la ferroptosis y la disfunción mitocondrial juegan un papel dañino.
Cita: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Palabras clave: ferroptosis, mitocondrias, pancreatitis aguda, estrés oxidativo, muerte celular