Clear Sky Science · es
Ubiquitinación de mH2A1 mediada por UBE3A activa la transcripción de TERT para promover la resistencia a la senescencia en el cáncer de páncreas
Por qué esta investigación importa para los pacientes
El cáncer de páncreas está entre los más letales, en parte porque las células tumorales son extraordinariamente eficaces para eludir los frenos naturales del envejecimiento del organismo. Este estudio descubre un “circuito de sabotaje” molecular oculto que ayuda a las células del cáncer pancreático a mantenerse jóvenes, seguir dividiéndose y resistir los tratamientos. Al comprender este circuito, los investigadores señalan una vía nueva para inducir senescencia en estas células y luego eliminarlas selectivamente, abriendo la puerta a terapias combinadas más inteligentes.
La senescencia como freno tumoral natural
Todas las células llevan un reloj interno que finalmente las hace dejar de dividirse, un proceso conocido como senescencia. En lesiones pancreáticas tempranas, este reloj puede frenar el desarrollo tumoral al forzar a las células precancerosas a retirarse de forma permanente. Muchos tratamientos anticáncer también actúan en parte obligando a las células tumorales a entrar en este estado de envejecimiento. Sin embargo, si estas células senescentes no se eliminan, pueden alimentar la inflamación y favorecer la recaída del cáncer. De ahí surge una idea terapéutica nueva: primero inducir la senescencia en las células cancerosas y luego eliminar esas células envejecidas con fármacos “senolíticos” que son especialmente tóxicos para ellas.
Una enzima promotora del cáncer en el foco
Para encontrar genes que ayudan a las células de cáncer de páncreas a desafiar la senescencia, el equipo analizó grandes bases de datos de pacientes y luego validó sus hallazgos en muestras tumorales y líneas celulares. Identificaron una proteína llamada UBE3A, una enzima que etiqueta a otras proteínas para su destrucción. Los niveles de UBE3A eran mucho más altos en tumores pancreáticos que en el tejido normal circundante, y los pacientes con mayor UBE3A tendían a tener tumores más grandes, más avanzados y peor supervivencia. En células cultivadas, aumentar UBE3A aceleró el crecimiento, redujo marcadores clásicos del envejecimiento celular y disminuyó las secreciones inflamatorias típicas de las células senescentes. Silenciar UBE3A produjo el efecto contrario y, en modelos de ratón, redujo drásticamente el crecimiento tumoral y las metástasis hepáticas. 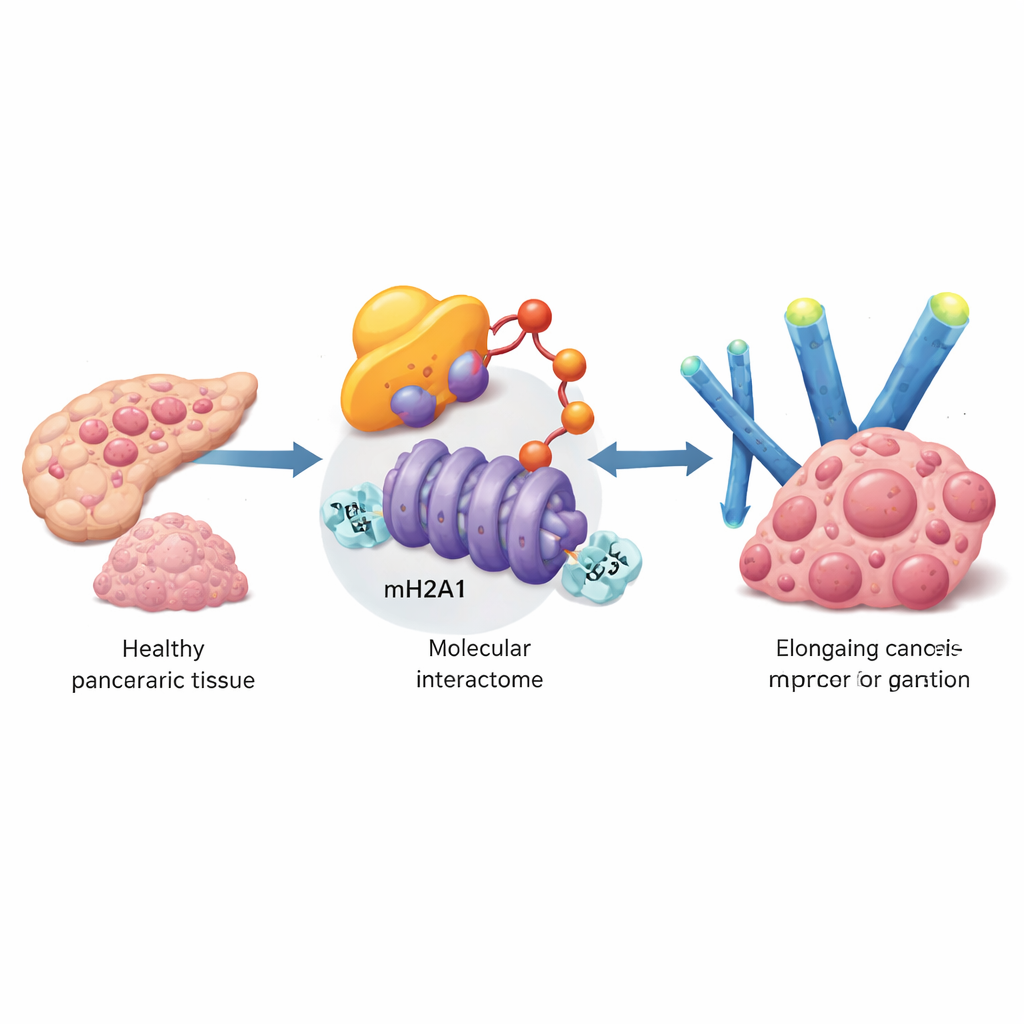
Cómo las células cancerosas borran un freno de la cromatina
Profundizando, los investigadores preguntaron sobre qué moléculas actúa UBE3A. Mediante pantallas avanzadas de espectrometría de masas, hallaron que UBE3A se une y etiqueta químicamente una variante especial de histona llamada macroH2A1 (mH2A1), que ayuda a compactar el ADN y normalmente funciona como un freno sobre la actividad génica. UBE3A añade una cadena de marcas de “destrúyeme” a mH2A1 en una posición específica, provocando su degradación por la maquinaria de eliminación de proteínas de la célula. En los tumores pancreáticos, los niveles de mH2A1 eran menores donde UBE3A estaba alto, y restaurar mH2A1 contrarrestó la capacidad de UBE3A para bloquear la senescencia y promover el crecimiento tumoral. Esto revela un paso clave: las células del cáncer pancreático eliminan una marca protectora de cromatina usando UBE3A para destruir mH2A1.
Desbloqueo de la telomerasa para mantener las células jóvenes
La siguiente pregunta fue qué genes quedan liberados cuando se elimina mH2A1. Combinando secuenciación de ARN y mapas de unión al ADN, el equipo identificó al gen de la telomerasa TERT como un objetivo central. La telomerasa mantiene las tapas protectoras en los extremos de los cromosomas, permitiendo a las células seguir dividiéndose en lugar de entrar en senescencia. El estudio muestra que mH2A1 normalmente se sitúa en una región potenciadora (enhancer) dentro del gen TERT, donde recluta a otra enzima, EZH2, para depositar una marca química represiva en histonas cercanas. Esta combinación mantiene TERT apagado y permite el acortamiento de los telómeros. Cuando UBE3A destruye mH2A1, el complejo represor se disuelve, el enhancer se activa, TERT se enciende, los telómeros se mantienen y las células del cáncer pancreático adquieren resistencia al envejecimiento. Formas mutantes de UBE3A que no pueden etiquetar proteínas, o mH2A1 mutante que no puede ser etiquetada, rompen este circuito y restauran el freno de la senescencia.
Combinar la inducción de senescencia con la limpieza senolítica
Finalmente, los investigadores probaron si esta vía podía explotarse terapéuticamente. Inhibir UBE3A empujó a las células del cáncer pancreático hacia la senescencia y aumentó su dependencia de proteínas anti‑muerte de la familia BCL‑2, una vulnerabilidad conocida de las células senescentes. El equipo combinó entonces la inhibición de UBE3A con ABT‑263, un fármaco senolítico que apunta a estas proteínas de supervivencia. En células en cultivo, la combinación provocó que muchas más células cancerosas sufrieran muerte celular programada que cualquiera de los tratamientos por separado. En modelos de ratón, los tumores con UBE3A reducido se encogieron aún más cuando los animales recibieron ABT‑263, y los marcadores de proliferación intracelular en los tumores disminuyeron notablemente. 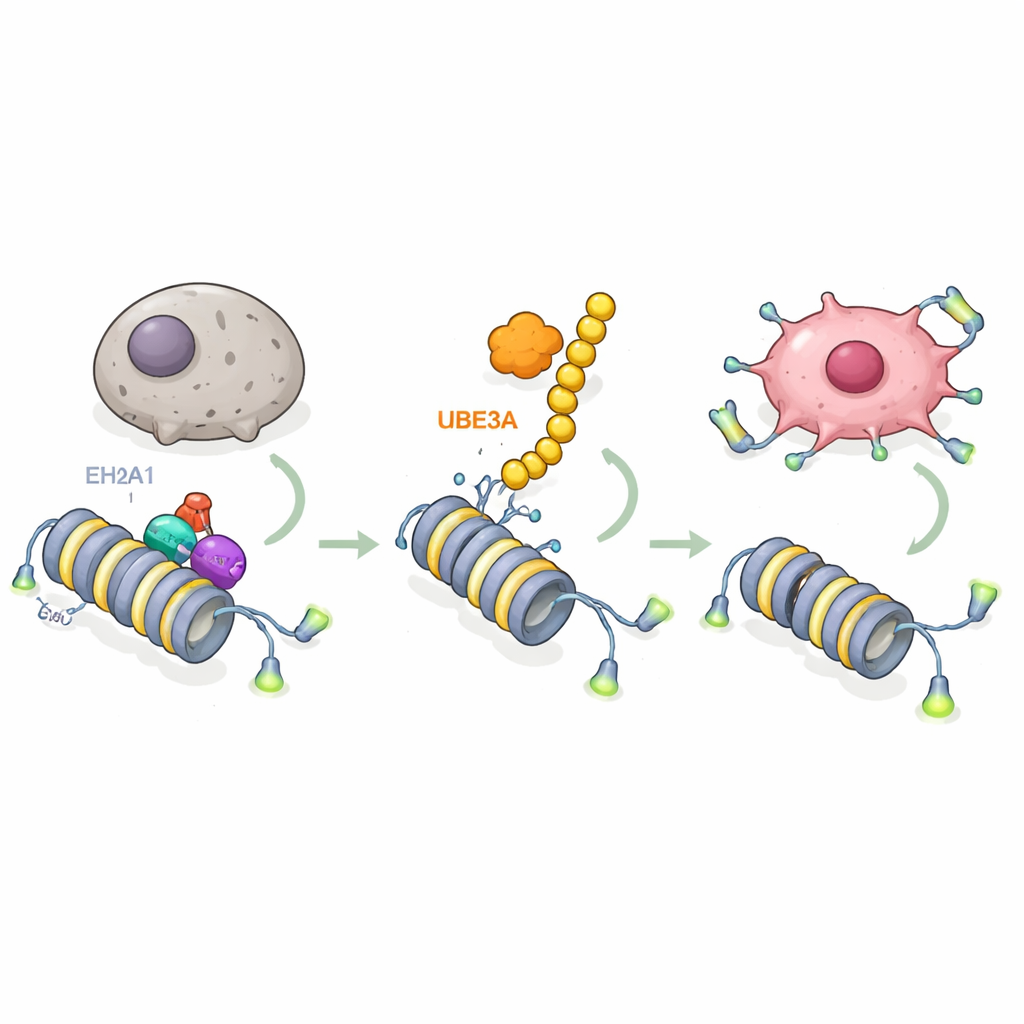
Qué significa esto para tratamientos futuros
Este trabajo revela una cadena detallada de eventos por la cual las células del cáncer pancreático evitan envejecer: UBE3A destruye el freno de la cromatina mH2A1, lo que a su vez levanta la represión del gen de la telomerasa TERT y ayuda a mantener los telómeros, permitiendo que las células sigan dividiéndose. Al dirigir UBE3A, los médicos podrían reactivar el programa natural de envejecimiento celular y luego usar fármacos senolíticos como ABT‑263 para eliminar selectivamente estas células cancerosas envejecidas y vulnerables. Aunque se necesitan más estudios para traducir este mecanismo en terapias para pacientes, el eje UBE3A–mH2A1–TERT ofrece un punto de apoyo prometedor contra uno de los cánceres más resistentes al tratamiento.
Cita: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Palabras clave: cáncer de páncreas, senescencia celular, telomerasa, ligasa de ubiquitina, terapia senolítica