Clear Sky Science · es
Un pequeño inhibidor de la proteína GTPasa ARF1 limita el crecimiento y la metástasis de células de cáncer de hígado y colon
Por qué importa esta investigación
Los cánceres de hígado y colon están entre los tumores más letales, y los tratamientos actuales a menudo reducen los tumores a costa de efectos secundarios severos. Este estudio explora un tipo de fármaco que no simplemente envenena las células que proliferan rápidamente, sino que se introduce en las células cancerosas y separa un “centro de control” proteico del que dependen para crecer y propagarse. Al dirigirse a este centro, el compuesto experimental pretende frenar el crecimiento tumoral preservando al mismo tiempo el tejido sano.
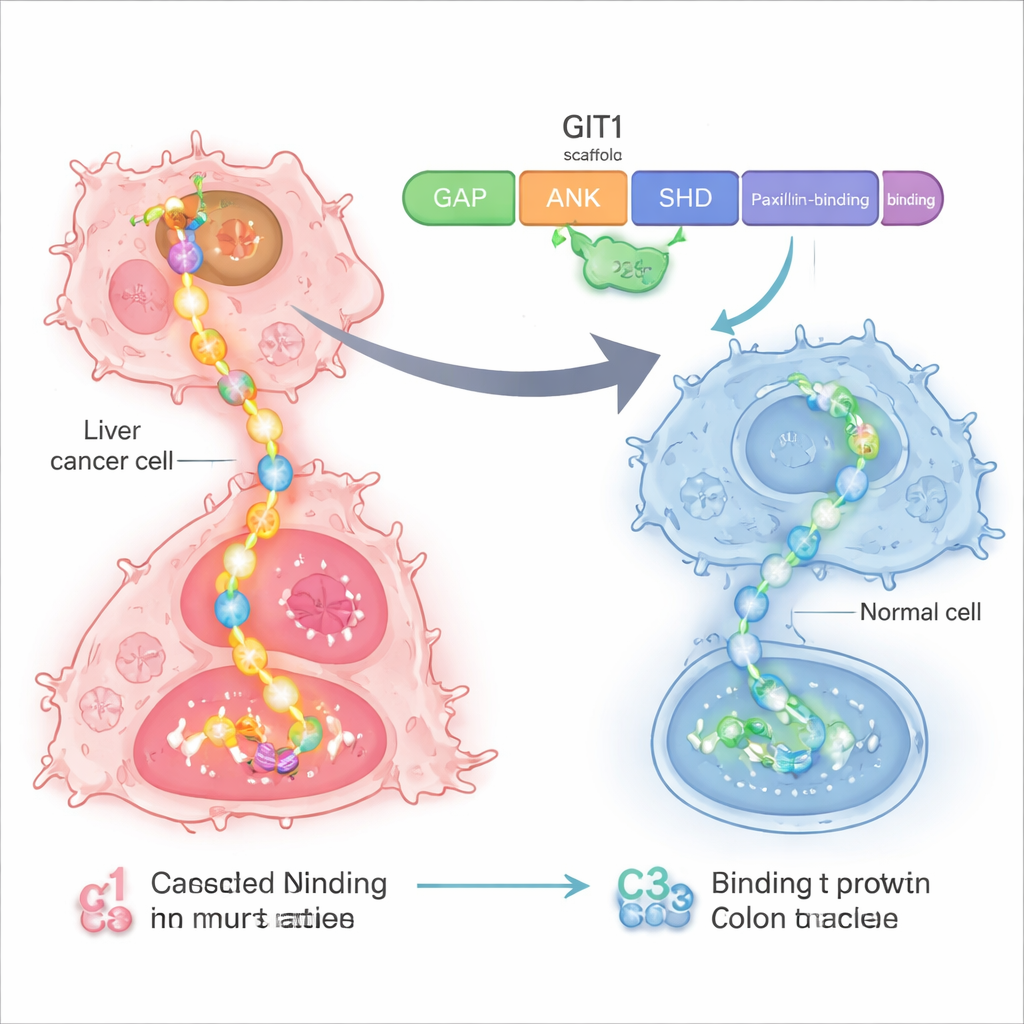
Un centro de control vulnerable dentro de las células cancerosas
Los investigadores se centraron en una proteína llamada GIT1, que actúa como un andamio o regleta dentro de las células. En los cánceres de hígado y colon, GIT1 y su proteína socia MAT2B se producen en exceso. Juntas, ensamblan varios componentes de una vía de crecimiento principal conocida como RAS–RAF–MEK–ERK, una cadena de señales que indica a las células que se dividan y migren. Trabajos previos mostraron que cuando GIT1 y MAT2B son abundantes, los tumores de hígado y colon crecen más rápido y se diseminan con mayor facilidad, y cuando estas proteínas se reducen, el crecimiento canceroso se desacelera. Esto convirtió al andamio GIT1–MAT2B en un objetivo atractivo para una terapia más precisa.
Diseñar una pequeña molécula sin un plano
Un reto clave fue que no se dispone de la estructura cristalográfica tridimensional de GIT1, por lo que el equipo no pudo simplemente “consultar” la forma de la proteína. En su lugar, utilizaron modelado por ordenador para predecir la estructura de una región de GIT1 compuesta por repeticiones de ankyrina, situada cerca de donde se unen MAT2B y otras proteínas de señalización. Luego, evaluaron virtualmente una amplia biblioteca de pequeñas moléculas contra este modelo para ver cuáles podrían unirse a esa área. De nueve candidatos probados en células, una molécula—denominada compuesto 3 (C3)—destacó. C3 se unió específicamente a GIT1, pero no a su pariente cercano GIT2, y redujo la actividad de la señal de crecimiento ERK en varias líneas celulares cancerosas.
Detener la división y la diseminación de las células cancerosas
Cuando las células de cáncer de hígado y colon se trataron con C3, su proliferación se ralentizó y, a dosis más altas, muchas células murieron, mientras que las células no cancerosas de hígado y riñón permanecieron en gran parte intactas. C3 provocó que las células cancerosas se detuvieran en la transición entre las fases G2 y M del ciclo celular, el punto de control justo antes y durante la mitosis cuando una célula se divide en dos. El compuesto también redujo drásticamente la capacidad de las células cancerosas para formar colonias y para migrar a través de un cultivo—dos medidas de laboratorio vinculadas a la reaparición tumoral y la metástasis. A nivel molecular, C3 debilitó las interacciones entre GIT1, MAT2B y las proteínas de la vía RAF–MEK–ERK, lo que condujo a una menor actividad de MEK y ERK y a una reducción del impulsor del ciclo celular ciclina D1.
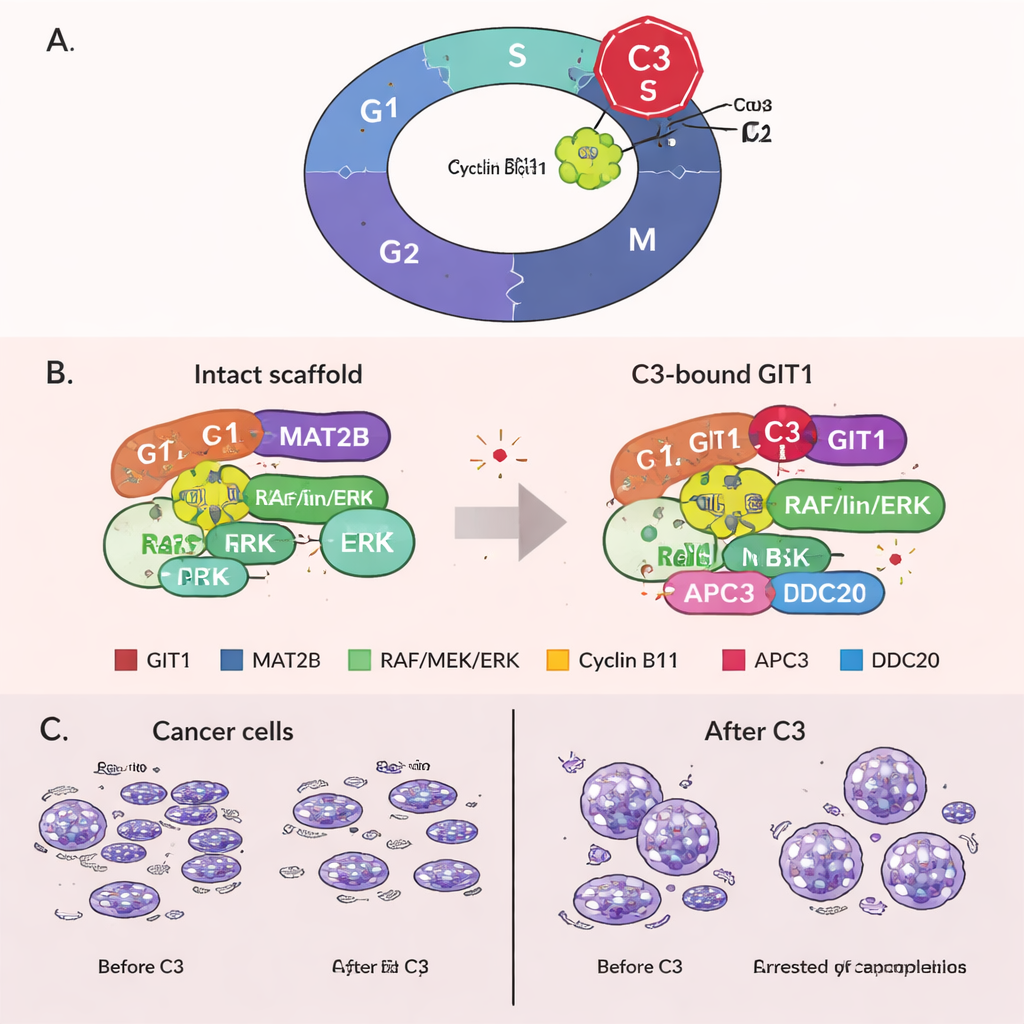
Bloquear las células en mitosis mediante un papel recién descubierto de GIT1
De forma inesperada, el equipo descubrió un nuevo papel de GIT1 en los pasos finales de la división celular. Encontraron que GIT1 se une a la ciclina B1, una proteína que ayuda a impulsar a las células hacia la mitosis, y también a partes de una máquina proteica llamada complejo promotor de la anafase (APC/C), que normalmente marca a la ciclina B1 para su degradación para que las células puedan salir de la mitosis. El tratamiento con C3 fortaleció el vínculo entre GIT1 y la ciclina B1, pero debilitó las conexiones entre GIT1, ciclina B1 y los componentes del APC/C. Como resultado, la ciclina B1 dejó de degradarse eficientemente, sus niveles se mantuvieron altos y las células quedaron atrapadas en mitosis. Este arresto prolongado suele desencadenar la muerte celular, ofreciendo una segunda vía por la que C3 puede matar células cancerosas. Es importante que, cuando GIT1 se redujo experimentalmente, C3 perdió gran parte de su capacidad para aumentar la ciclina B1, bloquear el ciclo celular y suprimir el crecimiento, lo que demuestra que sus efectos dependen realmente de GIT1.
Resultados prometedores en modelos animales
Los investigadores pasaron después a modelos en ratones para ver si C3 podría funcionar en organismos vivos. En ratones con sistema inmune competente y tumores colorrectales implantados, inyecciones de C3 directamente en los tumores ralentizaron enérgicamente su crecimiento sin toxicidad evidente en los órganos principales. En dos modelos adicionales—células humanas de cáncer de colon creciendo en hígados de ratones inmunodeficientes, y células de cáncer de colon de ratón que se habían diseminado al hígado en ratones con sistema inmune competente—C3 administrado por inyección intraperitoneal redujo la carga tumoral y los signos de diseminación. Análisis de sangre y de tejidos sugirieron que los tratamientos fueron bien tolerados, y estudios farmacocinéticos mostraron que los niveles del fármaco en la sangre permanecieron lo suficientemente altos durante varias horas tras la dosificación.
Qué podría significar esto para futuros tratamientos del cáncer
Para un público no especialista, el mensaje clave es que los investigadores han encontrado una forma de atacar el cáncer no apuntando a una sola enzima mutada, sino interrumpiendo un ensamblaje multiproteico del que las células cancerosas dependen tanto para las señales de crecimiento como para la división celular correcta. Su pequeña molécula, C3, se une específicamente a GIT1, reconfigura su red de asociados, atenúa una vía de crecimiento principal y atrapa a las células cancerosas en un atasco letal durante la mitosis. Aunque C3 sigue siendo una herramienta experimental y aún no es un fármaco para pacientes, el trabajo demuestra que dirigirse a proteínas andamio como GIT1 puede abrir una nueva vía para tratar con mayor precisión los cánceres de hígado y colon y, potencialmente, con menos efectos secundarios.
Cita: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Palabras clave: cáncer de hígado, cáncer de colon, terapia dirigida, arresto del ciclo celular, proteína andamio