Clear Sky Science · es
Vesículas extracelulares de células madre rescatan fenotipos celulares y déficits de comportamiento en modelos neuronales y murinos de TEA asociados a SHANK3
Mensajeros diminutos con gran potencial
El trastorno del espectro autista y afecciones relacionadas suelen rastrearse hasta fallos sutiles en cómo las células cerebrales se conectan y comunican, mucho antes de que los síntomas sean visibles. Este estudio explora una idea emergente: que los “paquetes” microscópicos liberados por las células —llamados vesículas extracelulares— podrían tanto propagar cambios nocivos entre neuronas como, si se diseñan adecuadamente, ayudar a revertirlos. Trabajando con neuronas derivadas de células madre humanas y un modelo murino bien establecido, los investigadores examinan cómo estas vesículas influyen en la actividad cerebral en una forma de autismo relacionada con el gen SHANK3, y si las vesículas procedentes de células madre sanas pueden restaurar un funcionamiento y comportamiento cerebral más típicos.
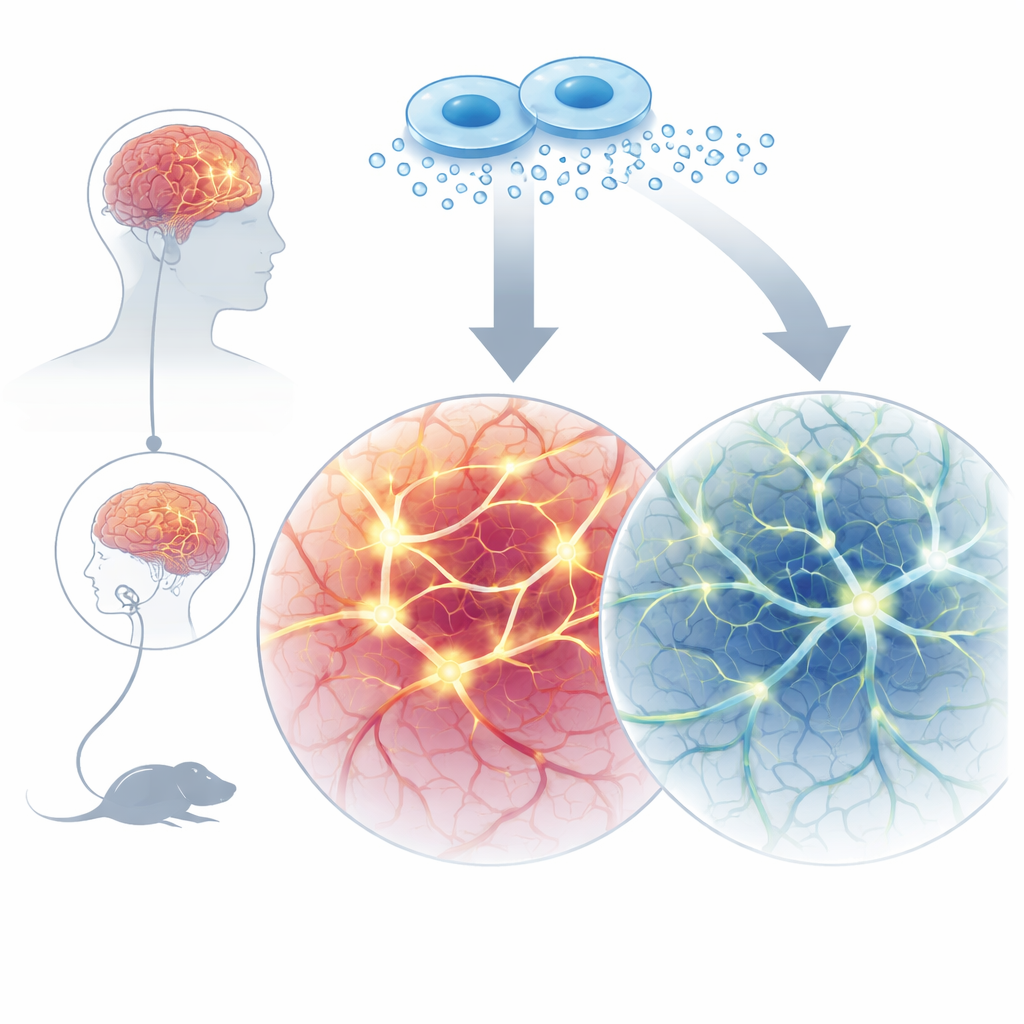
Cuando el cableado cerebral se desarrolla demasiado rápido
Algunas personas con autismo o con el síndrome de Phelan-McDermid presentan alteraciones en un gen llamado SHANK3, que contribuye a organizar los puntos de contacto donde las neuronas se comunican. En trabajos anteriores, el equipo mostró que las neuronas humanas cultivadas a partir de células de un paciente con una mutación en SHANK3 maduraron de forma inusualmente rápida y generaron demasiadas señales eléctricas, un patrón denominado hiperexcitabilidad. Una sobreactividad temprana similar aparece en modelos murinos que carecen de Shank3. Estos hallazgos respaldan la idea de que, durante el desarrollo temprano, ciertas formas de autismo no se caracterizan por una debilidad en los circuitos cerebrales, sino por un auge inicial de conectividad y actividad que luego conduce a un desequilibrio.
Paquetes celulares que pueden propagar problemas
Casi todas las células, incluidas las neuronas, liberan pequeñas vesículas recubiertas por membrana llenas de proteínas, ARN y otras moléculas. Estas vesículas extracelulares actúan como mensajeros, permitiendo a las células influir en sus vecinas. Los investigadores se preguntaron si las vesículas liberadas por neuronas con la mutación SHANK3 podrían portar señales que cambien el comportamiento de neuronas sanas. Cultivaron neuronas corticales humanas tanto de un paciente con la mutación SHANK3 como de un familiar no afectado, recogieron vesículas de cada grupo y luego las “intercambiaron” entre los cultivos. Sorprendentemente, las neuronas sanas expuestas a vesículas de neuronas mutantes SHANK3 empezaron a parecer y comportarse más como las células mutantes: dispararon más potenciales de acción, mostraron mayor actividad espontánea y exhibieron propiedades eléctricas coherentes con la hiperexcitabilidad. En contraste, las neuronas mutantes no mejoraron al tratarse con vesículas de neuronas sanas, lo que sugiere que esas vesículas carecían de un cargamento restaurador suficiente.
Vesículas de células madre como influencia calmante
Dado que las vesículas pueden atravesar barreras biológicas y tienen menos probabilidad de provocar reacciones inmunitarias que las células trasplantadas, son candidatas terapéuticas atractivas. El equipo, por tanto, probó vesículas procedentes de dos fuentes de células madre: células madre mesenquimales (derivadas de médula ósea) y células iPS (células adultas reprogramadas). Cuando estas vesículas de células madre se añadieron repetidamente a neuronas humanas con mutación SHANK3 durante su maduración, el comportamiento neuronal se desplazó hacia la normalidad. Sus corrientes de sodio y potasio disminuyeron, su tendencia a disparar racimos de potenciales de acción se redujo, y la amplitud y frecuencia de sus señales sinápticas se aproximaron a las de las neuronas control. Los análisis proteómicos —estimaciones profundas de las proteínas dentro de las vesículas— mostraron que las vesículas de neuronas mutantes estaban enriquecidas en proteínas estructurales sinápticas y reguladores de la actina vinculados al cableado anómalo, mientras que las vesículas de células madre contenían moléculas asociadas con la poda sináptica, la plasticidad y la homeostasis, como componentes del complemento y factores de crecimiento. Este contraste sugiere por qué un tipo de vesícula agrava la hiperactividad mientras que otro puede contrarrestarla.
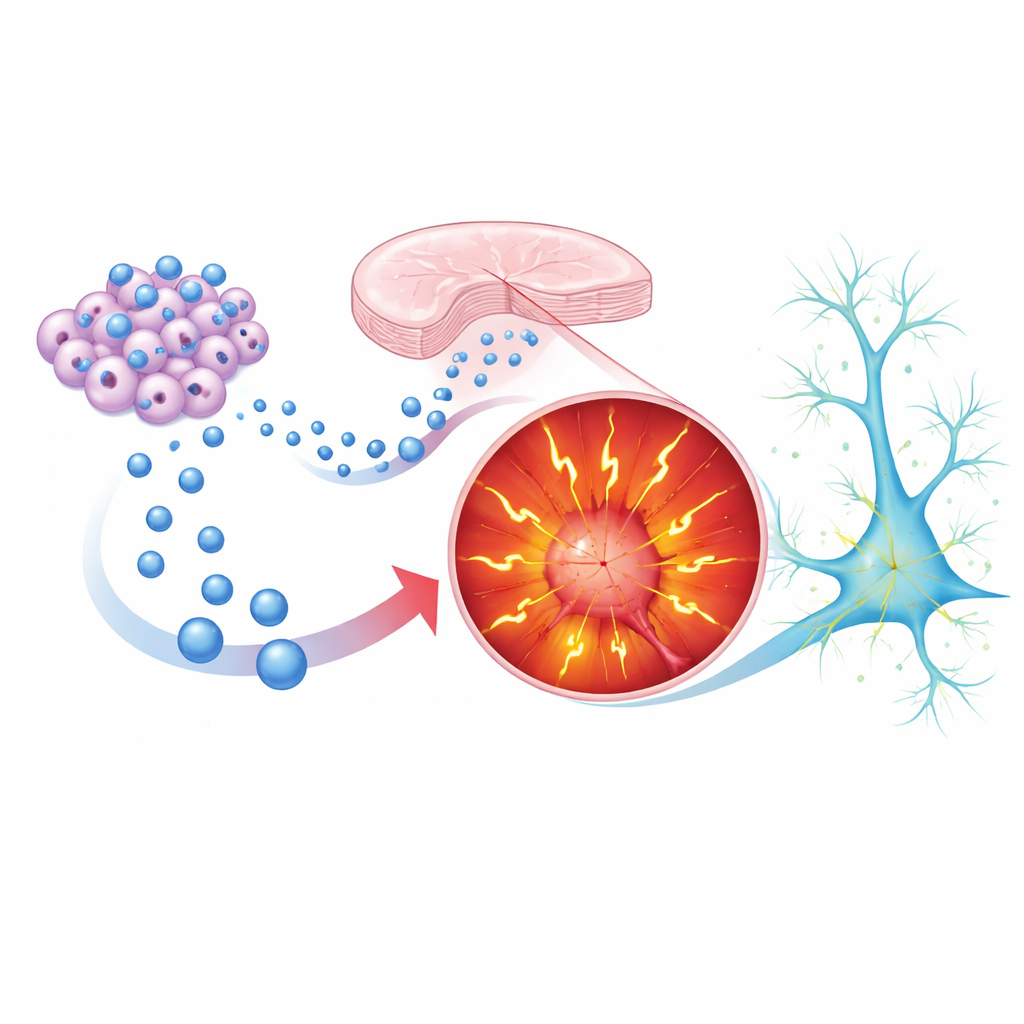
De platos de neuronas al comportamiento vivo
Para averiguar si estos efectos trascienden las placas de laboratorio, los investigadores recurrieron a ratones knockout Shank3B, que muestran rasgos semejantes al autismo. Los machos sin Shank3 mostraron interés normal por otros ratones y por el sexo opuesto, pero tuvieron dificultades con una tarea más sutil: distinguir entre un ratón estresado y uno tranquilo, una aproximación grosera a reconocer los estados emocionales de otros. Los científicos administraron vesículas de células iPS sanas por vía intranasal —desde la primera infancia hasta la etapa juvenil— usando una ruta no invasiva que ya se explora en terapias para el cerebro. En la edad adulta, los ratones knockout tratados recuperaron un patrón claro de preferencia en la prueba de reconocimiento emocional, mientras que su movimiento general permaneció sin cambios. Esto sugiere que las vesículas de células madre ayudaron a ajustar circuitos específicos de procesamiento social en lugar de simplemente aumentar la actividad o el estado de alerta de los animales.
Qué podría significar esto para tratamientos futuros
En conjunto, el estudio presenta a las vesículas extracelulares como mensajeros de doble filo: las vesículas de neuronas deficientes en SHANK3 pueden transmitir rasgos de hiperactividad a células sanas, pero las vesículas de determinadas células madre pueden amortiguar esa sobreactividad y rescatar aspectos del comportamiento en ratones. Para las familias y los clínicos, el trabajo aún no se traduce en una terapia lista para usar, pero apunta a un futuro en el que vesículas personalizadas, cargadas con contenido protector, podrían dirigir suavemente los circuitos cerebrales en desarrollo hacia el equilibrio. Dado que estas vesículas pueden administrarse sin cirugía y producirse a escala a partir de células madre, ofrecen un camino prometedor hacia intervenciones específicas y menos invasivas para el autismo y afecciones del neurodesarrollo relacionadas.
Cita: Choudhary, A., Rosh, I., Hussein, Y. et al. Extracellular vesicles from stem cells rescue cellular phenotypes and behavioral deficits in SHANK3-associated ASD neuronal and mouse models. Cell Death Dis 17, 244 (2026). https://doi.org/10.1038/s41419-026-08474-x
Palabras clave: autismo, SHANK3, vesículas extracelulares, terapia con células madre, neurodesarrollo