Clear Sky Science · es
La inhibición del receptor del factor estimulador de colonias 1 es neuroprotectora para los fotorreceptores en el desprendimiento de retina
Por qué esta investigación importa para la visión
El desprendimiento de retina es una urgencia que puede robar la vista incluso después de una cirugía que reataque con éxito la retina. Gran parte de este daño persistente procede del propio equipo de limpieza inmunitario del organismo, que puede dañar las células sensibles a la luz mientras intenta ayudar. Este estudio en ratones explora si bajar la actividad de un interruptor inmunitario clave, llamado CSF1R, puede proteger estos frágiles fotorreceptores y abrir una nueva vía para preservar la visión.
El equipo de limpieza del ojo y cómo puede volverse contraproducente
Cuando la retina se separa de su capa de soporte, los fotorreceptores pierden de repente acceso al oxígeno y a los nutrientes. Muchas de estas células mueren y el tejido lanza señales de auxilio. Las células inmunitarias locales de la retina, conocidas como microglía, cambian de forma, se desplazan hacia la lesión y aumentan su fagocitosis de restos. Al mismo tiempo, células inmunitarias procedentes del torrente sanguíneo, incluidos distintos tipos de monocitos, invaden la retina. Juntas, intentan limpiar las células muertas e iniciar la reparación. Pero esta reacción beneficiosa también puede excederse, provocando una inflamación adicional que mata fotorreceptores aún viables y empeora la pérdida de visión.
Un fármaco que apunta a un interruptor inmunitario compartido
Tanto la microglía residente como los monocitos entrantes dependen del mismo receptor de superficie, CSF1R, para su supervivencia y función. Los investigadores utilizaron PLX5622, un compuesto administrado como píldora que bloquea CSF1R, para preguntar cómo interferir con este interruptor modifica el comportamiento inmunitario en el desprendimiento de retina. Primero mapearon sus efectos en la sangre y en la retina. En la circulación, un tratamiento breve no cambió el número total de monocitos, pero reequilibró sus subtipos: aumentaron los monocitos “clásicos” proinflamatorios, mientras que disminuyeron los monocitos patrullantes “no clásicos”. En el ojo, PLX5622 agotó de forma eficiente la microglía retiniana y modificó cuántas células inmunitarias derivadas de la sangre entraron en la retina dañada y qué formas y comportamientos adoptaron.
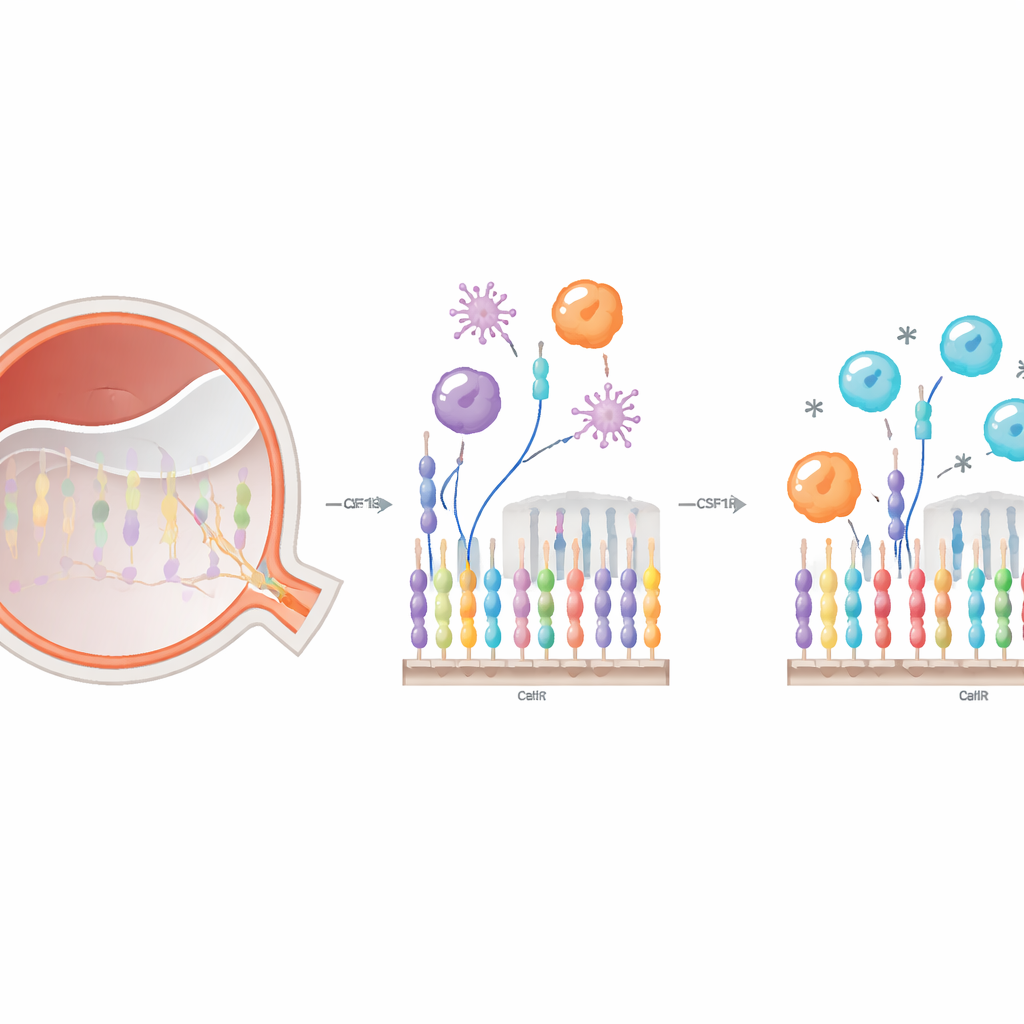
Rastrear células locales y entrantes con etiquetas de color
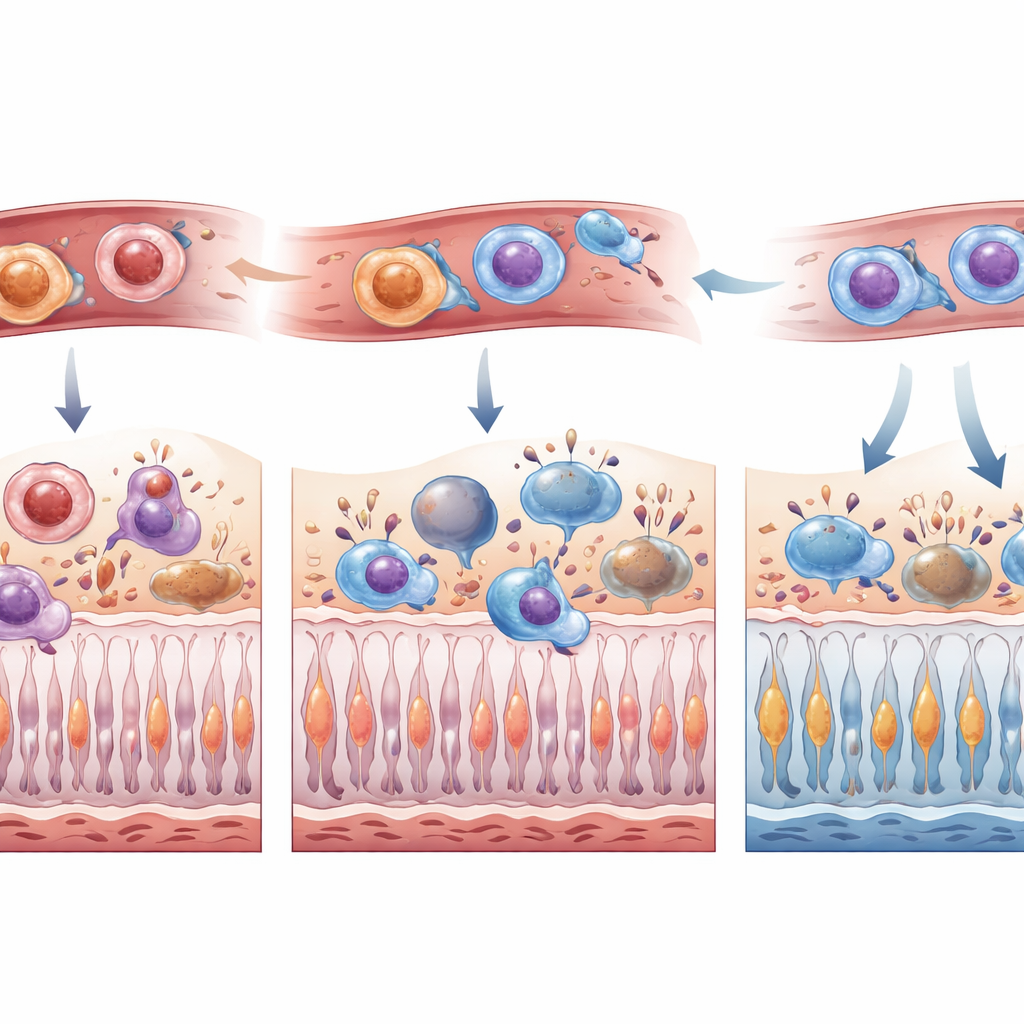
Como la microglía y los monocitos infiltrantes pueden parecer muy similares una vez que entran en la retina, el equipo creó un sistema de ratón con doble etiquetado: la microglía residente brillaba de un color y las células derivadas de médula ósea de otro. Tras inducir un desprendimiento de retina controlado, siguieron adónde se desplazaban estas células y cómo cambiaban durante la primera semana. Sin tratamiento, la microglía se acumuló principalmente en las capas superiores de la retina, mientras que las células derivadas de la médula ósea inundaron especialmente el espacio subretiniano, adoptando con frecuencia una morfología ameboide y altamente fagocítica. Con la inhibición de CSF1R, la microglía quedó notablemente reducida en todas las capas desde temprano, y menos células derivadas de la médula ósea, en particular el tipo ameboide, alcanzaron la retina en los primeros días tras la lesión. Para el día siete, la oleada de células entrantes se había puesto en gran medida al día, lo que sugiere que el bloqueo de CSF1R retrasa en lugar de bloquear de forma permanente su llegada.
Cómo el cambio en el equilibrio inmunitario protege las células sensibles a la luz
Para entender qué significaban estos cambios inmunitarios para la visión, los investigadores contaron los fotorreceptores moribundos y supervivientes en múltiples momentos. En las primeras horas tras el desprendimiento, los animales tratados con PLX5622 presentaron menos fotorreceptores en muerte y más fotorreceptores supervivientes. A la semana, tanto el pretratamiento corto como el tratamiento continuo preservaron el grosor de la capa de fotorreceptores, una medida estructural de supervivencia celular, y redujeron la presencia de células inmunitarias en el espacio subretiniano. Un perfil inmunitario detallado mostró que, a pesar de una caída general en el número total de leucocitos infiltrantes, los que entraron en la retina bajo inhibición de CSF1R tendieron a portar una firma más inflamatoria. Los autores sugieren que esta combinación —menos células, pero más orientadas a una limpieza rápida de restos— podría acelerar la eliminación segura de fotorreceptores moribundos al tiempo que preserva a los vecinos todavía sanos.
Qué podría significar esto para futuros tratamientos
Este trabajo muestra que un inhibidor sistémico de CSF1R puede remodelar tanto las respuestas inmunitarias locales como las circulantes en el desprendimiento de retina y, de forma algo contraintuitiva, que un equipo de limpieza más inflamatorio pero más reducido puede proteger la visión. Al agotar temporalmente la microglía, retrasar la primera oleada de células derivadas de la sangre y cambiar los subtipos de monocitos, PLX5622 creó una ventana temporal en la que se redujo el daño temprano impulsado por la respuesta inmune y sobrevivieron más fotorreceptores. Aunque el estudio se realizó en ratones y el equilibrio entre inflamación útil y dañina difiere entre las enfermedades oculares, estos hallazgos respaldan la inhibición de CSF1R como un punto de partida prometedor para fármacos diseñados para afinar la respuesta inmunitaria y preservar la visión tras una lesión retinal.
Cita: Pastor-Puente, S., Jung, R., Gonzalez-Buendia, L. et al. Colony-stimulating factor 1 receptor inhibition is neuroprotective to photoreceptors in retinal detachment. Cell Death Dis 17, 264 (2026). https://doi.org/10.1038/s41419-026-08470-1
Palabras clave: desprendimiento de retina, microglía, supervivencia de fotorreceptores, neuroinflamación, inhibición de CSF1R